聚焦EULAR 2024 | 中国之声:JAK1抑制剂SHR0302革新中重度活动性类RA患者治疗格局
时间:2024-06-07 11:00:54 热度:37.1℃ 作者:网络
类风湿关节炎(Rheumatoid Arthritis, RA)是以侵袭性、对称性多关节炎为主要临床表现的慢性、全身性自身免疫性疾病。RA的确切发病机制不明,目前认为主要由免疫系统攻击关节形成长期慢性炎症所致。据数据显示,我国RA患病率约为0.42%,患者总数约为500万,男女比约为1:4。我国RA患者在病程1~5年、5~10年、10~15年及≥1年的致残率分别为18.6%、43.5%、48.1%和61.3%。
虽然已多种类风湿关节炎治疗药物,且各种药物的联合应用可以在一定程度上提高患者的应答率,但仍有部分患者使用现有药物治疗应答不佳或因无法耐受毒性反应终止治疗。
SHR0302作为一种高效选择性JAK1抑制剂,可通过抑制JAK1信号传导发挥抗炎和抑制免疫的生物学效应。一项II期研究,在针对活动性类风湿关节炎患者中展示了显著的有效性和安全性。
基于此,在即将召开的2024欧洲风湿病学大会(EULAR)上,来自中国研究学者旨在进一步评估 SHR0302 在对 csDMARDs 反应不佳的中重度活动性 RA 患者中的疗效和安全性。

这项研究是一项多中心、随机、安慰剂对照、双盲III期试验(NCT04333771),纳入符合条件的患者年龄在18-75岁之间,根据2010年ACR/EULAR标准诊断为RA,病状中至重度活动,且对csDMARDs反应不佳,按1:1:1比例随机分配接受安慰剂、4mg或8mg SHR0302每日一次口服治疗,为期24周。分配时,考虑基线时并用的csDMARDs情况(甲氨蝶呤≥15mg/周或来氟米特20mg/天;甲氨蝶呤<15mg/周或来氟米特<20mg/天;或两者均未使用)。
随后,初始分配至安慰剂组的患者转为接受SHR0302剂量4mg 治疗28周,而最初接受SHR0302治疗的患者继续维持原有剂量。主要终点是第24周达到美国风湿病学会20%改善标准(ACR20)的患者比例。
结果显示,共有566名患者被随机分配,所有患者均至少服用了一剂研究药物。基线时,各治疗组的人口统计学特征和疾病特点均衡。其中,524名患者(92.6%)完成了为期24周的治疗,496名患者(87.6%)完成了为期52周的治疗。
第24周时,与安慰剂组(40.4%)相比,服用4mg(70.4%,P<0.0001)和8mg(75.1%,P<0.0001)剂量的SHR0302患者的ACR20反应率明显更高。同样,剂量为 4 mg和 8 mg的 SHR0302 在 ACR50 和 ACR70 反应方面也有显著改善。
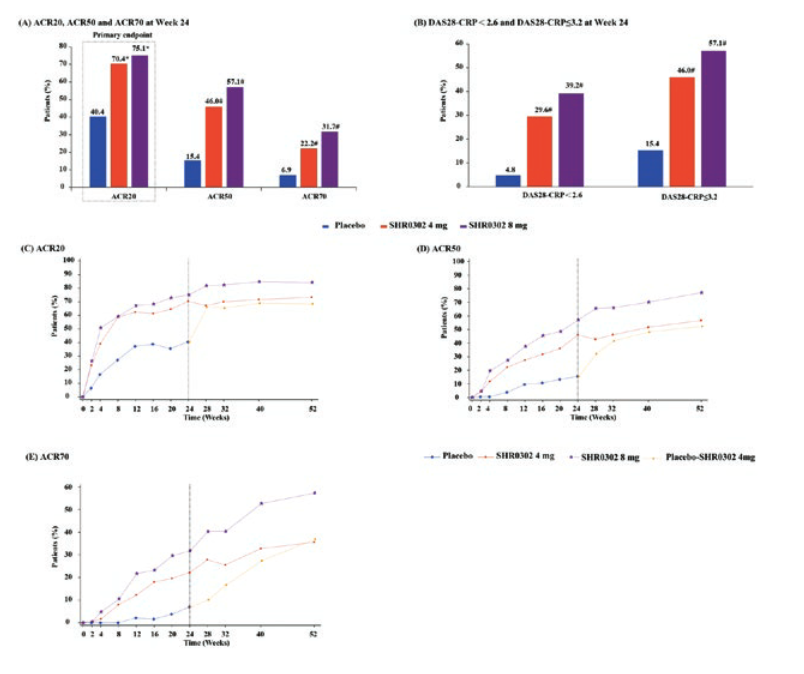
此外,SHR0302起效迅速,第2周时两组SHR0302的ACR20应答患者明显多于安慰剂组。此外,与安慰剂组(4.8% 和 15.4%)相比,SHR0302 4 毫克组(29.6% 和 46.0%, P<0.0001)和 SHR0302 8 毫克组(39.2% 和 57.1%,P<0.0001)在第 24 周达到 DAS28-CRP < 2.6 和 ≤ 3.2 的患者比例明显更高。
第24周时,SHR0302 4mg和8mg组相对于基线的HAQ-DI评分具有显著变化。与安慰剂相比,第24周时SHR0302治疗组SF-36评分同样显示出显著变化,这些改善趋势在额外的28周期间得以持续。
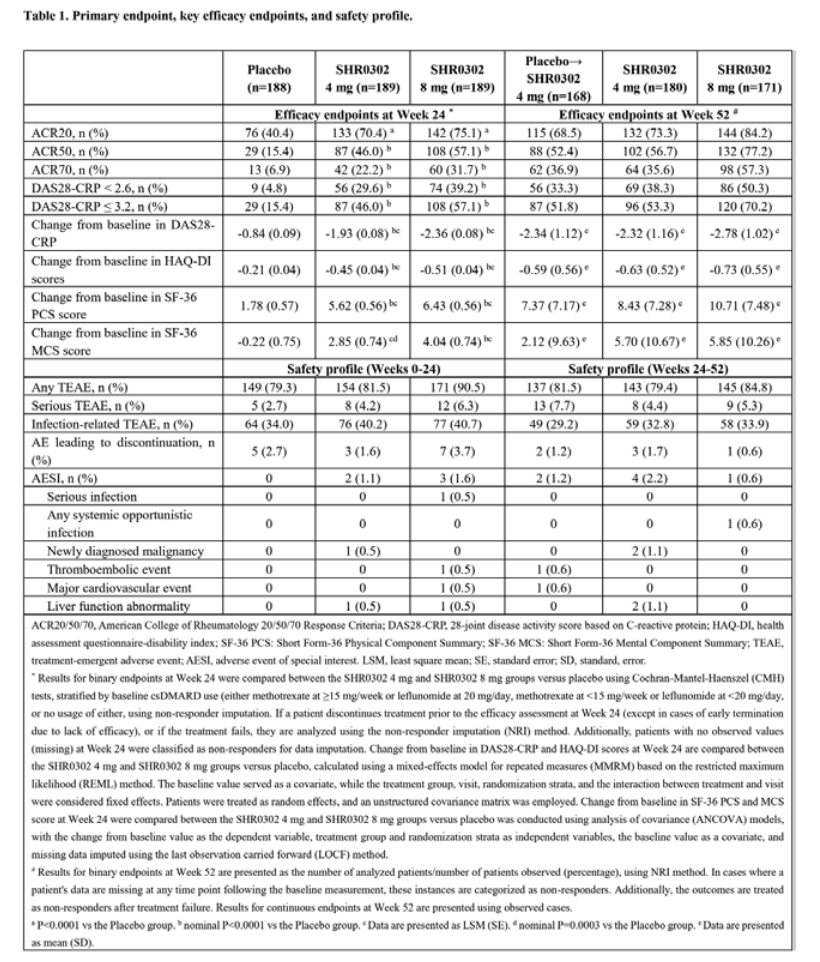
在不良事件方面,在整个24周的治疗期间,SHR0302 4mg组的治疗中出现不良事件(TAEs)发生率为81.5%,8mg组为90.5%,安慰剂组为79.3%。感染相关TAEs在SHR0302组中略高(4mg组为40.2%,8mg组为40.7%),安慰剂组为34.0%。但严重感染和系统性机会性感染的报告较少。此期间,SHR0302 4mg组报告一例新诊断肿瘤,8mg组报告一例血栓栓塞事件和一例重大心血管事件,以及两例肝功能异常(分别在SHR0302 4mg和8mg组)。试验期间,未报告死亡、结核病病例、胃肠穿孔,也未发现新的安全性问题。
总之,两种剂量的 SHR0302(4mg和8mg)在对csDMARDs反应不佳的中至重度活动性RA患者中均展现出显著且持久的临床症状改善,与其他JAK1抑制剂相比未发现新的安全性信号。
参考资料:
A MULTICENTER, RANDOMIZED, PLACEBO-CONTROLLED, DOUBLE-BLIND, PHASE 3 STUDY OF SHR0302, A SELECTIVE JANUS KINASE 1 INHIBITOR, IN PATIENTS WITH ACTIVE RHEUMATOID ARTHRITIS AND INADEQUATE RESPONSE TO CONVENTIONAL SYNTHETIC DISEASE-MODIFYING ANTI-RHEUMATIC DRUGS


