NAT MED | 新辅助帕博利珠单抗、达拉非尼和曲美替尼治疗BRAFV600突变型可切除黑色素瘤:随机2期NeoTrio试验
时间:2024-06-26 13:00:40 热度:37.1℃ 作者:网络
黑色素瘤是一种皮肤癌,BRAF 基因突变是其常见特征,与肿瘤的侵袭性和年轻患者人群相关,靶向治疗和免疫检查点抑制剂是治疗黑色素瘤的两种有效方法,但各有优缺点,靶向治疗(如达拉非尼和曲美替尼)具有快速响应的特点,但易产生耐药性,免疫检查点抑制剂(如帕博利珠单抗)响应率较低,但耐药性较少,且具有长期生存优势,该试验旨在探讨靶向治疗联合免疫检查点抑制剂在可切除的 BRAFV600 突变黑色素瘤中的疗效。

方法
NeoTrio 试验是一项随机、开放标签、多臂的 II 期临床试验,旨在评估新辅助帕博利珠单抗、达拉非尼和曲美替尼在可切除的 BRAFV600 突变黑色素瘤中的疗效,纳入了年龄 ≥ 18 岁,经组织学证实为可切除的 AJCC 第八版分期 IIIB-D 期黑色素瘤,伴有淋巴结疾病(无皮肤转移),BRAFV600 突变阳性,ECOG 体能状态 ≤ 1,具有可测量的疾病,患者按照1:1:1 的比例,通过基于互联网的系统进行分层随机,并根据 BRAFV600E 与非 BRAFV600E 突变进行分层。单药治疗组:帕博利珠单抗 200 mg 静脉注射,每 3 周一次,共 2 个周期;序贯治疗组:达拉非尼 150 mg 口服,每天两次,曲美替尼 2 mg 口服,每天一次,共 7 天,然后帕博利珠单抗 200 mg 静脉注射,每 3 周一次,共 2 个周期;联合治疗组:达拉非尼 150 mg 口服,每天两次,曲美替尼 2 mg 口服,每天一次,共 6 周,同时帕博利珠单抗 200 mg 静脉注射,每 3 周一次,共 2 个周期。所有患者接受 6 周的新辅助治疗,并在新辅助治疗后接受根治性淋巴结清扫术,所有患者接受 42 周(16 个周期)的帕博利珠单抗辅助治疗,每 3 周一次,直至出现毒性反应、撤回知情同意、疾病复发或死亡。主要终点为病理反应率,包括病理完全缓解率(pCR),次要终点为影像学反应(RECIST v1.1)、无复发生存(RFS)、总生存期(OS)、手术结果、安全性、生活质量(HRQOL)和转化研究终点。
研究结果
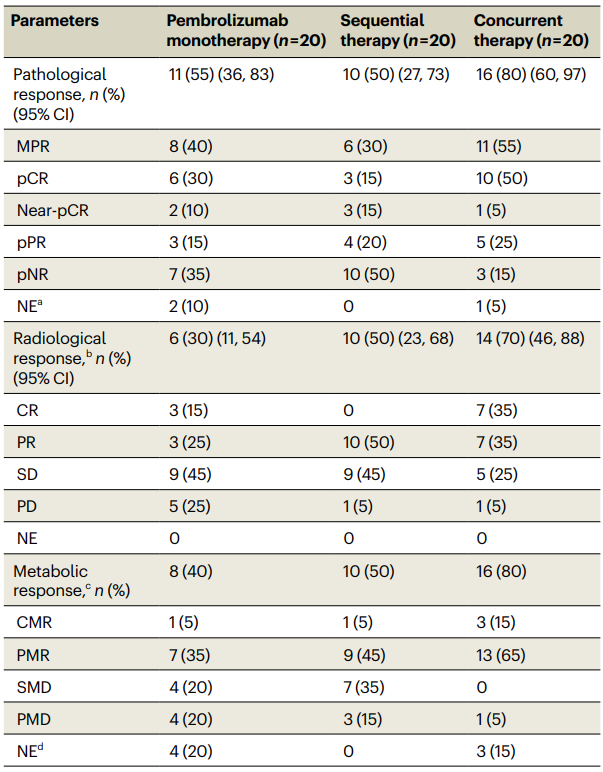
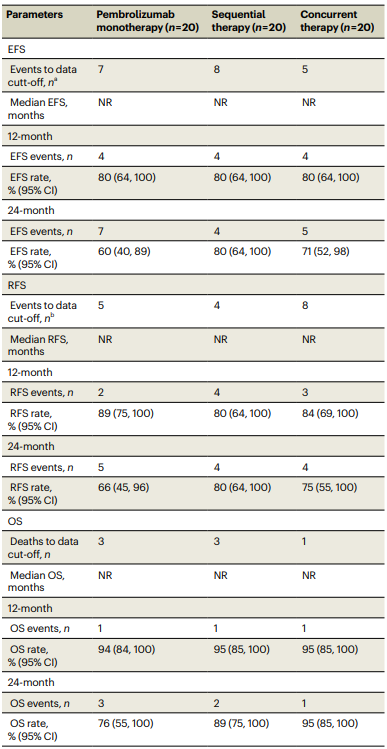
所有治疗方案均达到了主要终点,即病理反应率(≥5%),帕博利珠单抗单药治疗组、序贯治疗组和联合治疗组的病理反应率分别为55%、50% 和 80%,pCR 率分别为 30%、15% 和 50%,客观影像学反应率(CR 或 PR)分别为 30%、50% 和 70%, 2 年 EFS 率分别为 60%、80% 和 71%,2 年 RFS 率分别为 66%、80% 和 75%, 2 年 OS 率分别为 76%、89% 和 95%。主要病理反应者比无主要病理反应者复发率更低,在接受帕博利珠单抗单药治疗的患者中,所有主要病理反应者均未复发,而靶向治疗组的主要病理反应者中各有 1 例复发。
安全性分析
所有治疗组的 TRAEs 发生率很高,在接受新辅助治疗期间影响了 75-100% 的患者,联合治疗组的毒性反应最高,55% 的患者出现了 3/4 级 TRAEs,并有 40% 的患者因 TRAEs 提前终止治疗, 39 名患者(68%)出现了手术并发症,包括 9 例 3/4 级手术不良事件。22 名患者因 TRAEs 中断了新辅助达拉非尼/曲美替尼治疗,其中 19 名来自并发治疗组,导致中断的 TRAEs 等级为 1-3 级,包括发热、寒战和肝酶升高,1 名患者因 3 级肝炎和 3 级药物性肝损伤提前终止新辅助帕博利珠单抗治疗。

结论
NeoTrio 试验表明,将 BRAF 靶向疗法添加到 BRAFV600 突变患者的黑色素瘤新辅助 ICI 中可能会增加毒性并降低治愈潜力,建议黑色素瘤患者在新辅助治疗中不应联合使用免疫治疗和靶向治疗。
原始出处
Long, G.V., Carlino, M.S., Au-Yeung, G. et al. Neoadjuvant pembrolizumab, dabrafenib and trametinib in BRAFV600-mutant resectable melanoma: the randomized phase 2 NeoTrio trial. Nat Med (2024). https://doi.org/10.1038/s41591-024-03077-5.


