Lancet Oncol:一线venetoclax组合与慢性淋巴细胞白血病健康患者的免疫化疗——多中心、开放标签、随机、3期试验的4年随访
时间:2024-07-21 22:01:32 热度:37.1℃ 作者:网络

GAIA/CLL13是一项开放标签、随机、3期研究,在欧洲和中东10个国家的159个地点进行。在GAIA/CLL13试验的初步分析报告中发现,与化疗免疫疗法相比,venetoclax-obinutuzumab-ibrutinib和venetoclax-obinutuzumab-ibrutinib改善了先前未经治疗的慢性淋巴细胞白血病患者的不可检测的微小残留病变(uMRD)率和无进展生存期。然而,目前尚无直接比较不同venetoclax组合的数据。因此,这项为期4年的GAIA/CLL13试验探索性随访分析的目的是评估MRD引导的三联疗法的附加价值,不同CD20抗体对结局的影响,以及治疗结束时MRD的预后价值。
符合条件的患者被随机分配为化疗免疫治疗组,venetoclax-rituximab组,venetoclax-obinutuzumab组和venetoclax-obinutuzumab-ibrutinib组。所有治疗均以28天为周期进行。免疫化疗组共6个周期,65岁以上患者静脉注射苯达莫司汀(90mg/m²,1-2天),65岁或以下的患者静脉注射氟达拉滨(25 mg/m²,1-3天)和静脉注射环磷酰胺(250 mg/m²,1-3天)。静脉注射利妥昔单抗(rituximab)加入化疗(375 mg/m²,第1周期第1天;500 mg/m²,第2-6周期第1天)。
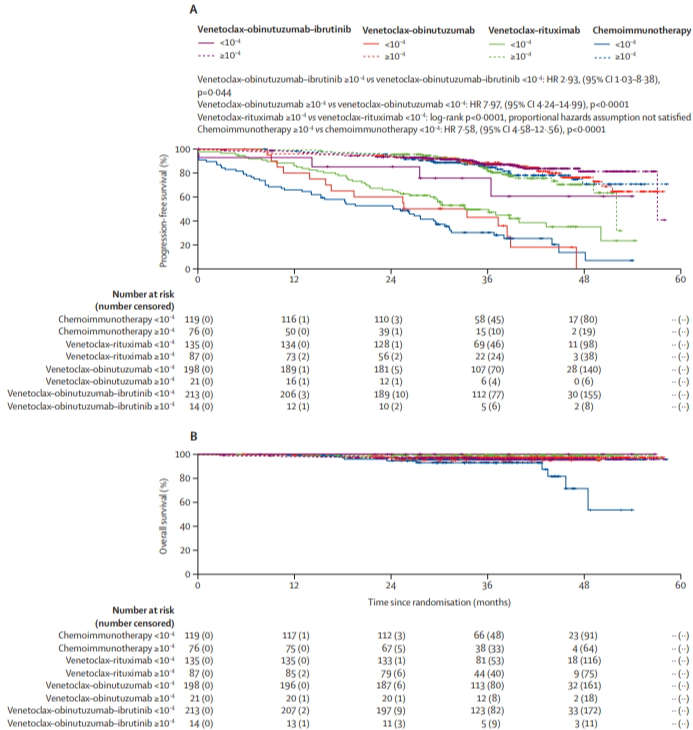
图1:15个月时外周血中可测量的残留疾病状态(慢性淋巴细胞白血病细胞比例)的无进展生存期(A)和总生存期(B)
在实验组中,患者在从第1个周期第22天开始的5周递增期后,每天口服venetoclax400mg 10个周期。在venetoclax-rituximab组中,患者另外接受静脉注射rituximab(第1周期:第1天375mg/m²;第2-6周期:第1天500mg/m²)。在venetoclax-obinutuzumab组中,患者另外接受obinutuzumab静脉注射治疗,(第1周期:第1天100mg,第2天900mg,第8天和第15天1000mg;第2-6周期:第1天1000mg)。在venetoclax-obinutuzumab-ibrutinib组中,患者每日另外接受ibrutinib 420mg口服治疗,从第1个周期的第1天添加,直到连续两次测量(间隔3个月)检测不到MRD时或到第36个周期为止。
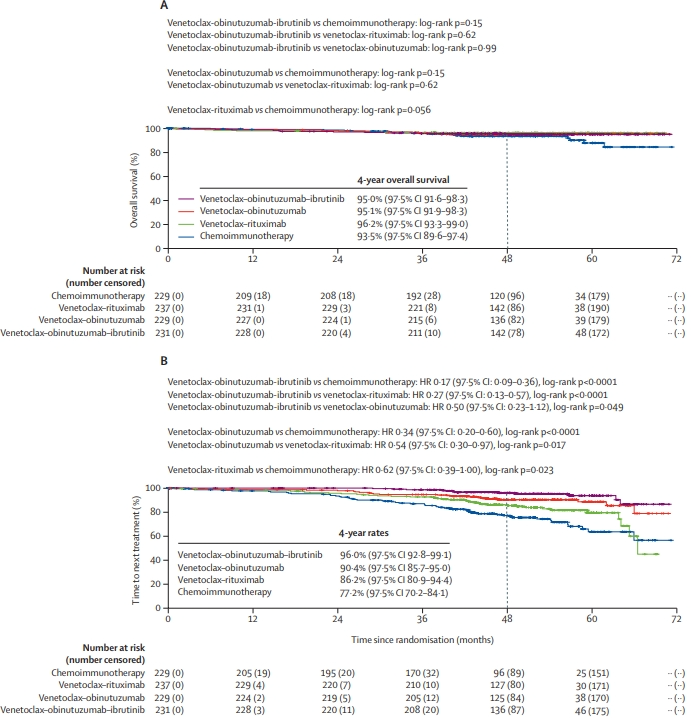
图2:总生存期(A)和下一次治疗时间(B)
计划治疗时间在化疗免疫治疗组为6个周期,venetoclax-rituximab和venetoclax-obinutuzumab组为12个周期,venetoclax-obinutuzumab-ibrutinib组为12-36个周期。主要终点为venetoclax-obinutuzumab-ibrutinib与标准化疗免疫疗法比较时15个月外周血中未检测到的MRD率,以及研究者评估的无进展生存期。这两个主要终点在其他地方都有报道,故本文主要报告对研究人群进行4年随访后更新的无进展生存结果的事后探索性分析。
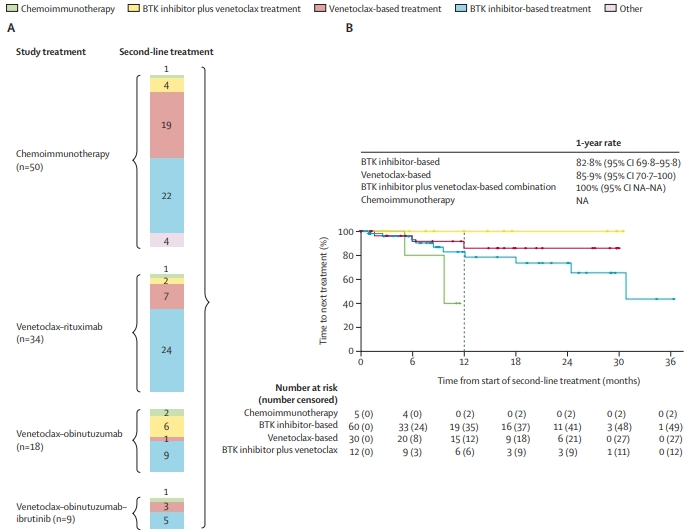
图3:慢性淋巴细胞白血病-型疾病进展的治疗顺序(A)和从二线治疗开始到下一次治疗的时间(B)(n=111)
2016年12月13日到2019年10月13日期间,研究一共筛选了1080例患者,其中926例被随机分配到治疗组(免疫化疗组n=229;Venetoclax-rituximab组n=237;Venetoclax-obinutuzumab组n=229;venetoclax-obinutuzumab-ibrutinib组n=231);平均年龄60.8岁,926例患者中有259例(28%)为女性,667例(72%)为男性(种族和民族数据未报道)。在这次探索性随访分析的数据截止日期,venetoclax-obinutuzumab组患者的无进展生存期明显长于化疗免疫治疗组和venetoclax-rituximab组。venetoclax-obinutuzumab-ibrutinib组的无进展生存期也明显长于化疗免疫治疗组和venetoclax-rituximab组。

图4:暴露调整后的感染和严重感染的发生率(A)和心脏疾病(B),安全分析人群(n=912)
venetoclax-obinutuzumab-ibrutinib组和venetoclax-obinutuzumab组之间的无进展生存期无显著差异,并且venetoclax-rituximab组与化学免疫治疗组的比较不符合比例风险假设。估计venetoclax-obinutuzumab-ibrutinib组的4年无进展生存率为85.5%,venetoclax-obinutuzumab组为81.8%,venetoclax-rituximab组为70.1%,化疗免疫治疗组为62.0%。
最常见的3级或更严重的治疗相关不良事件是中性粒细胞减少(化疗免疫治疗组[53%],Venetoclax-rituximab组[46%],venetoclax-obinutuzumab组[56%],venetoclax-obinutuzumab-ibrutinib组[48%])。研究者确定与研究治疗相关的死亡发生在化学免疫治疗组的3例患者中(败血症、转移性鳞状细胞癌和Richter综合征各1例),venetoclax - rituximab和venetoclax - obinutuzumab组中0例,venetoclax - obinutuzumab - ibrutinib组中4例(急性髓性白血病、真菌性脑炎、小细胞肺癌和中毒性白质脑病各1例)。
总的来说,这项研究经过4年多的随访,发现与化疗免疫疗法和venetoclax - rituximab相比,venetoclax - obinutuzumab和venetoclax - obinutuzumab - ibrutinib在既往未治疗的慢性淋巴细胞白血病患者中显著延长了无进展生存期,因此支持其在该患者组中的使用和进一步评估,同时亦需要考虑到在三联疗法中观察到的更高的毒性。
原始出处:
Fürstenau M, Kater AP, Robrecht S, et al. First-line venetoclax combinations versus chemoimmunotherapy in fit patients with chronic lymphocytic leukaemia (GAIA/CLL13): 4-year follow-up from a multicentre, open-label, randomised, phase 3 trial [published correction appears in Lancet Oncol. 2024 Jul;25(7):e284. doi: 10.1016/S1470-2045(24)00329-2]. Lancet Oncol. 2024;25(6):744-759. doi:10.1016/S1470-2045(24)00196-7

