BLOOD:Menin-MLL1相互作用是nup98重排AML的分子依赖性
时间:2021-10-01 10:01:45 热度:37.1℃ 作者:网络
急性髓系白血病(Acute myeloid leukemia, AML)由11p15染色体上核孔蛋白98 (nucleoporin 98, NUP98)基因易位驱动,是复发和难治性疾病儿童中最常见的基因型,是预后极差的高危人群。NUP98易位产生NUP98融合蛋白,将NUP98的n端结构域与各种c端伴侣结合,这些c端伴侣包括具有同源框结构域的表观遗传修饰和转录因子,如HOX基因,并与急性髓系白血病(AML)的不良预后相关。
先前对NUP98重排恶性血液病建模的研究表明,NUP98- jarid1a、NUP98- nsd1、NUP98- HOXA9和NUP98- hoxd13融合蛋白是白血病发展的潜在驱动因子。虽然这些融合是有效的癌蛋白,但伴随的基因突变,如WT1或FLT3内部串联复制,带来了更糟糕的预后。临床上迫切需要了解nup98融合蛋白驱动白血病发生的机制。
MLL1在nup98融合白血病中是一种分子依赖,因此国外研究团队研究了在nup98融合白血病模型中阻断Menin-MLL1相互作用的疗效。其研究内容发表在BLOOD期刊上。利用NUP98-HOXA9和NUP98-JARID1A融合癌蛋白驱动的小鼠白血病细胞系,他们证明nup98 -融合驱动的白血病对Menin-MLL1抑制剂VTP50469敏感,其IC50与他们之前报道的ml重排和NPM1c白血病细胞相似。
在nup98融合转化的白血病细胞中,抑制Menin-MLL1可上调分化标志物如CD11b,并下调促白血病转录因子如Meis1的表达。他们证明了MLL1和NUP98融合蛋白本身通过一组关键基因从染色质中被驱逐,这些基因对维持恶性表型至关重要。除了这些体外研究外,他们还建立了nup98融合驱动的患者源性异种移植(PDX)模型,以测试Menin-MLL1抑制的体内疗效。
VTP50469治疗显著延长NUP98-NSD1和NUP98-JARID1A白血病小鼠的存活时间。基因表达分析显示,Menin-MLL1抑制同时抑制了一个前白血病基因的表达程序,包括下调HOXA簇,上调组织特异性分化标记物。这些临床前结果表明,Menin-MLL1抑制可能是一种合理的靶向治疗nup98重排白血病患者的方法。
图1:MLL和Menin在nup98重排白血病中具有分子依赖性。
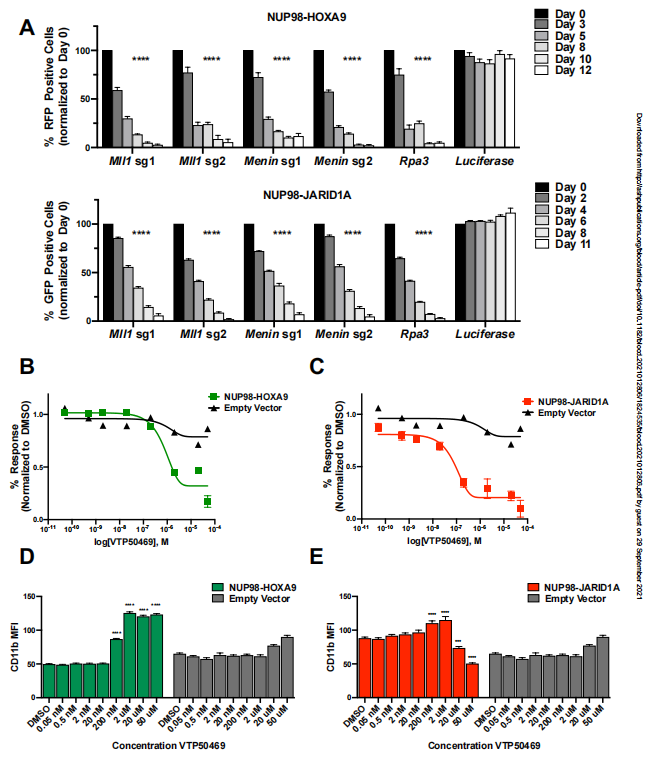
图2:MLL1在VTP50469治疗后从染色质转移到一个关键基因子集。

图3:NUP98融合在VTP50469的一个关键基因子集处理后从染色质分离。
图4:Meis1基因表达的挽救降低了nup98融合白血病对MLL-Menin抑制的敏感性。
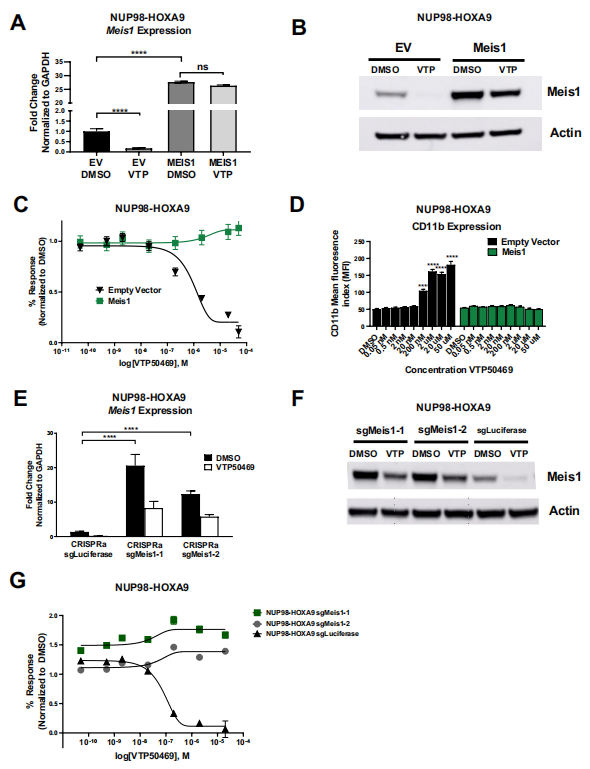
图5:体内小鼠白血病模型和nup98融合白血病患者来源的异种移植模型对MLL-Menin抑制反应。

原始出处:
Emily B Heikamp, Jill A Henrich, Florian Perner, Eric M Wong, Charles Hatton, Yanhe Wen, Sonali P Barwe, Anilkumar Gopalakrishnapillai, Haiming Xu, Hannah Julia Uckelmann, Sumiko Takao, Yaniv Kazansky, Yana Pikman, Gerard M. McGeehan, Edward A Kolb, Alex Kentsis, Scott A. Armstrong; The Menin-MLL1 interaction is a molecular dependency in NUP98-rearranged AML. Blood 2021; blood.2021012806. doi: https://doi.org/10.1182/blood.2021012806


