Science:利用人类大脑类器官,揭示结节性硬化症的起源
时间:2022-01-31 22:18:56 热度:37.1℃ 作者:网络
在一项新的研究中,在大脑类器官的帮助下,来自奥地利科学院和维也纳医科大学等研究机构的研究人员能够确定结节性硬化症(tuberous sclerosis complex, TSC)--一种罕见的神经发育遗传性疾病,是在发育过程中产生的,而不仅仅是在遗传上。通过这些来自患者的人类大脑实验室模型,他们将这种疾病的起源确定为人类特有的尾侧晚期中间神经元祖细胞(caudal late interneuron progenitor, CLIP)。
这些研究结果进一步表明,只有使用人类衍生的大脑类器官模型才能很好地理解影响人类大脑的疾病的病理。相关研究结果发表在2022年1月28日的Science期刊上,论文标题为“Amplification of human interneuron progenitors promotes brain tumors and neurological defects”。
人类大脑的复杂性很大程度上是由于发育涉及到人类独有的过程,其中许多过程仍是我们当前科学知识中的空白。TSC在这方面也不例外,因为长期以来,基于动物模型获得的数据,它被描述为一种主要的遗传性疾病。如今,论文共同通讯作者、奥地利科学院分子生物技术研究所科学主任Jürgen A. Knoblich及其研究团队的突破性研究利用患者衍生的大脑类器官模型来揭开这种罕见的神经发育疾病的神秘面纱。
Knoblich解释说,“我们对TSC根源的研究结果使我们发现了一种人类大脑特有的祖细胞类型。这解释了为什么其他实验室模型不能很好地确定这种疾病的病理。”
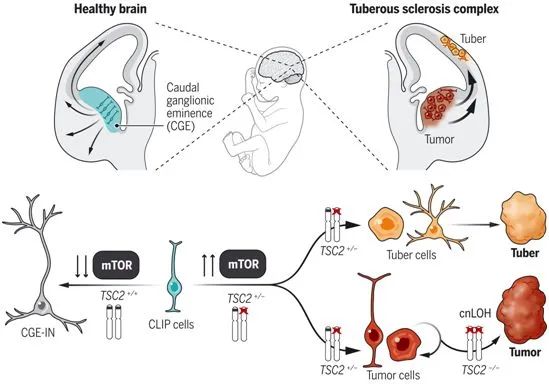
在妊娠中期,尾侧神经节隆起中的CLIP细胞产生迁移到皮层的中间神经元。图片来自Science, 2022, doi:10.1126/science.abf5546。
在许多受影响的患者中,TSC表现为严重的癫痫和精神症状,如自闭症和学习困难。从形态上看,TSC的特点是在患者的大脑中经常发现一些描述明确的迹象。其中,良性肿瘤存在于大脑的一个特定区域,以及大脑皮层中称为“结节(tuber)”的病变。长期以来,这两种形态上的畸变都被归结为遗传原因。然而,对患者样本的分析结果与流行的理论有分歧,主要是关于结节。论文共同通讯作者、奥地利科学院分子生物技术研究所Knoblich团队研究助理Nina Corsini解释说,“为了研究TSC,我们开发了这种疾病的大脑类器官模型:三维细胞培养物,我们用它来模拟大脑,我们可以获取源自任何一名患者的大脑类器官。”
在这项新的研究中,Knoblich团队培养出了源自几名受影响的患者的大脑类器官,这种方法可以研究患者大脑在发育过程中某个阶段存在的分子和细胞机制。论文第一作者Oliver Eichmüller解释说,“通过这种方法,我们发现,就像在患者的大脑中一样,这类大脑类器官长出了肿瘤,并有类似于患者结节的无序区域。”
然而,重现一种疾病的病理生理学特征仅仅是第一步。Eichmüller说,“通过进一步挖掘原因,我们发现这两种异常都是由人类大脑特有的一种细胞类型过度增殖引发的。这些细胞被称为尾侧晚期中间神经元祖细胞,简称CLIP细胞。它们在人类大脑的发育阶段被发现,但在像小鼠这样的动物中没有。”Corsini说,“我们的研究表明,我们的大脑非常复杂,比大多数动物的大脑要复杂得多。”
Knoblich团队不仅将TSC与其他神经发育和神经精神疾病相提并论,而且也将它与影响人类大脑的恶性疾病相提并论,推测这些疾病也可能是由人类特有的发育过程引起的。Knoblich说,“我们在大脑发育和病理方面的人类特有原理的发现也可能适用于迄今为止还没有治疗方法的其他已知疾病。”
2013年因在奥地利科学院分子生物技术研究所建立人类大脑类器官而成为全球头条新闻,Knoblich实验室已将这种技术用于研究人类大脑发育的隐藏过程,以及影响人类大脑的几种疾病。凭借他们目前的发现,Knoblich团队如今能够揭示出神经科学和医学方面的一个未解之谜。
Knoblich说,“我们显然不会止步于此。作为下一步,我们旨在通过进一步调整我们的技术来研究更多的神经精神疾病。我们相信,这种人类衍生的实验室模型将最终帮助我们确定长期以来一直被忽视的人类特有机制。”
参考资料:
Oliver L. Eichmüller et al. Amplification of human interneuron progenitors promotes brain tumors and neurological defects. Science, 2022, doi:10.1126/science.abf5546.


