降胆固醇+消炎:动脉粥样硬化防治两大基石!
时间:2022-10-30 20:33:29 热度:37.1℃ 作者:网络
随着探究深入,动脉粥样硬化的防治理念不断更新。
胆固醇+炎症“融合”理论
作者指出,“没有胆固醇就没有动脉粥样硬化”这句话还有后半句——“没有血管壁的炎症,也难以启动动脉粥样硬化”。
这也是学界所谈的“融合”理论的核心内容,即胆固醇是动脉粥样硬化的致病因子,炎症也是,缺一不可。
值得一提的是,100多年前,现代病理学之父Virchow就指出,动脉粥样硬化是一种胆固醇诱发的慢性炎症。
炎症为何能成为扳机?
作者介绍,炎症不仅可部分替代(supplant)或降级(demote)脂质危险因素,而且炎症反应尚可激活一系列的信号通路,将脂类和其它传统动脉粥样硬化危险因素“融合”起来,以及与免疫失常促进动脉粥样硬化斑块的形成。
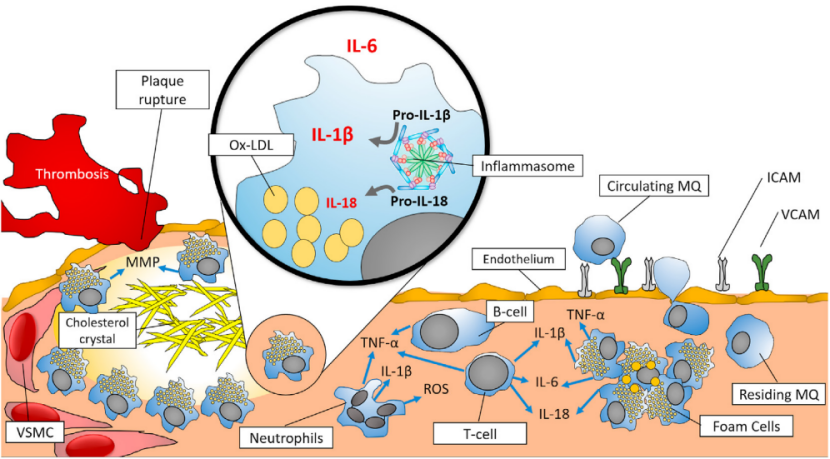
图1 炎症在动脉粥样硬化发生发展的各个阶段都有重要作用
思想决定行为,“融合”概念的提出也推动了临床管理的思变。降低胆固醇与减轻炎症反应,被视为当今动脉粥样硬化性疾病(ASCVD)防治的二大基本策略。
秋水仙碱、卡那单抗的系列抗炎研究也照亮了“融合”理论的前路。
富含甘油三酯脂蛋白及其残粒:ASCVD的独立危险因素
除了炎症,富含甘油三酯脂蛋白及其残粒也逐渐走入眼帘。
既往认为,为除LDL颗粒中的胆固醇具有致动脉粥样硬化作用外,血液中其它脂蛋白颗粒包括乳糜微粒,极低密度脂蛋白及残粒和中密度脂蛋白中的胆固醇因其“荷载”的脂蛋白颗粒较大不具备“穿入”内皮下诱发动脉粥样硬化的能力。
但事实并非如此,新近研究包括遗传学、人群观察及部分干预研究发现,富含甘油三酯脂蛋白及其残粒胆固醇也是ASCVD的独立危险因素。
比如一项对7.3万余人进行的研究,以LDL-C基因型作为对照,发现基因学上残粒胆固醇每上升1mmol/L,患缺血性心脏病的风险增加182%。
我国一项对4871位冠心病胸痛入院患者平均随访5.1年的研究显示,残粒胆固醇可显著预测冠心病并糖尿病前期/糖尿病患者的心血管事件。
临床上残粒胆固醇的水平可以通过检测血甘油三酯水平间接反映,也可直接测定或通过计算的方法获得。
治疗上以贝特类药物,高纯度鱼油等显著降低甘油三酯水平的药物为主要干预措施,其它降胆固醇药物包括他汀类药物和依折麦布均有一定程度的降残粒胆固醇作用。
Lp(a)水平:致动脉粥样硬化风险高于LDL-C
有学者推测,Lp(a)可能具有比LDL-C更强的致动脉粥样硬化特性。
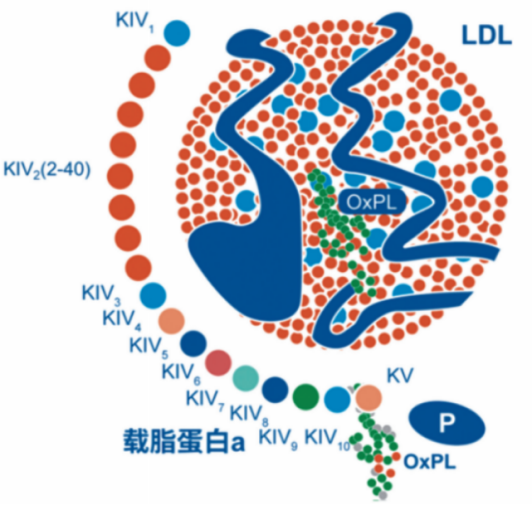
图2 Lp(a)组成结构示意图
首先,Lp(a)可以渗透到动脉内膜,结合细胞外基质的成分,促进巨噬细胞浸润和平滑肌细胞增殖。
其次,Lp(a)具有独特的Apo(a)结构,而Apo(a)正是Lp(a)发挥其独特致动脉粥样硬化作用的关键结构之一。
最后,在所有脂蛋白中,Lp(a)是氧化磷脂的最大结合力载体,氧化磷脂具有重要的促炎、促动脉粥样硬化作用,通过诱导内皮细胞、平滑肌细胞和巨噬细胞的促炎信号激活,引发动脉壁的炎症反应。
近日发布的《脂蛋白(a)与心血管疾病风险关系及临床管理的专家科学建议》指出,Lp(a)升高是冠心病、缺血性脑卒中和钙化性主动脉瓣狭窄的独立危险因素。
并建议在以下人群中检测血清Lp(a)水平:
(1)动脉粥样硬化性心血管病的极高危人群;
(2)有早发心血管病家族史(男性<55岁,女性<65岁);
(3)直系亲属血清Lp(a)水平升高>90mg/dl(200nmol/L);
(4)家族性高胆固醇血症或其他遗传性血脂异常;
(5)钙化性主动脉瓣狭窄患者。
同时建议,一般人群一生中至少应测量一次Lp(a)。
关于Lp(a)致心血管风险增高的切点值,不同国家指南和共识中的推荐并不一致,使用较多的是50mg/dl。
根据中国人群的现有研究数据,这份建议倾向于支持将30mg/dl作为风险增加的切点。
斑块侵蚀:急性冠脉综合征发病的重要病理生理学机制
斑块侵蚀的现代认识包括:
(1)由于他汀类药物的广泛应用,斑块侵蚀已替代斑块破裂成为急性冠脉综合征发病的最常见的病理生理学机制;
(2)斑块侵蚀是完全不同于斑块破裂的一种特殊病变,发生机制可能更为复杂,患者人群更为年轻,管腔面积较大,尸检结果多呈现内皮细胞大面积脱落而非狭窄;
(3)ST段抬高型心肌梗死多数是由斑块破裂造成的,非ST段抬高型ACS绝大多数是由斑块侵蚀引发;
(4)从影像学上看,斑块侵蚀多数都是白色血栓,血栓负荷较小;破裂斑块则多数是红色血栓,血栓负荷较大;
(5)光学相干断层扫描是在体识别血栓和血栓相关病变的最佳手段,在诊断ACS患者侵蚀斑块上具有的重要价值;
(6)ACS患者的个体化治疗十分重要,传统的抗斑块破裂的治疗均可用于斑块侵蚀,但由斑块侵蚀引起的急性冠脉综合征更倾向于保守药物治疗而非血运重建,β受体阻滞剂、他汀类药物、依折麦布和PCSK9抑制剂治疗显示出更好的前景。


