指南更新 | NSCLC恶性浆膜腔积液分子病理检测中国专家共识
时间:2023-01-12 12:01:41 热度:37.1℃ 作者:网络

摘要
精准分子分型是非小细胞肺癌精准治疗的基础和前提,但很多患者常无法获取足够的肿瘤组织进行分子病理诊断。晚期非小细胞肺癌患者常易出现恶性浆膜腔积液,可替代组织样本用于分子检测,但尚需进一步规范。本专家组参考国内外文献数据、结合临床实践经验,基于中国国情以及国内检测方法和治疗药物的可及性,经专家组专家反复讨论制定了此共识,以期指导和规范我国非小细胞肺癌恶性浆膜腔积液样本的分子病理检测。
肺癌是我国发病率和病死率较高的恶性肿瘤,按组织学类型不同分为小细胞肺癌和非小细胞肺癌(NSCLC),其中NSCLC约占85%。近10余年来,靶向治疗和免疫治疗药物的研发及临床应用极大地改善了晚期NSCLC的生存现状。因此,基于分子标志物筛选靶向治疗和/或免疫治疗的潜在获益人群显得尤为重要;准确、快速、全面地对NSCLC患者进行分子分型是其后续临床精准治疗的关键。随着临床需求的增加,分子病理检测技术近年来发展迅速,多种不同的检测技术已获批用于临床分子诊断。但是由于真实世界样本的可及性与不同类型检测平台的特点,需根据临床需求和检测目的选择合适的样本类型及检测方法。肿瘤组织样本一般被认为是分子病理检测的首选和“金标准”,但对于晚期NSCLC并非所有患者均能顺利获得检测所需的肿瘤组织样本。晚期NSCLC患者,常易在胸腔、腹腔和心包腔内聚集过多液体,这些部位的积液统称为浆膜腔积液。从浆膜腔积液中分离出细胞沉渣和/或上清液亦可用于NSCLC分子病理检测。实践证明该方法与组织样本分子检测结果相比具有较高的一致性,因此利用浆膜腔积液进行分子病理检测具有重要的临床应用价值和广泛的临床应用前景。然而,我国目前尚缺乏浆膜腔积液用于NSCLC分子检测系统全面的临床实践指导,因此本专家组结合国内外相关文献及临床实践经验,对浆膜腔积液分子病理检测的临床意义、适用人群、样本类型、检测前处理、常用检测方法及推荐检测流程等进行归纳总结并提出了指导性建议,以期能够最大限度地提高我国NSCLC患者浆膜腔积液临床检测应用的统一认识及分子检测流程的规范化。
一、NSCLC
分子病理检测的临床意义
NSCLC患者分子病理检测的内容主要包括靶向治疗相关标志物检测和免疫治疗相关标志物检测两个方面。靶向治疗相关标志物均为NSCLC发生发展中的驱动基因变异,变异形式主要包括突变、融合和扩增。中国人群以表皮生长因子受体(EGFR)突变(45%~55%)、KRAS突变(8%~10%)和间变性淋巴瘤激酶(ALK)融合(5%~8%)最为常见,目前已有多种针对EGFR突变和ALK融合的酪氨酸激酶抑制剂(TKI)获批用于临床靶向治疗,针对KRAS G12C突变的TKI药物也已在美国获批上市。除此之外,针对NSCLC少见基因变异,包括ROS1、RET、BRAF、MET、HER2、NTRK等基因变异的TKI药物也已获批用于临床治疗或在临床试验中取得了令人瞩目的疗效。鉴于存在恶性浆膜腔积液的NSCLC患者已是晚期,专家组强烈推荐对这类患者应同时进行NSCLC常见和少见基因变异检测,以全面筛选可能存在的靶点基因。免疫治疗相关标志物目前临床分子检测主要包括PD-L1蛋白表达和肿瘤突变负荷(TMB)检测,多个临床研究发现,PD-L1高表达或TMB高的NSCLC患者更易从抗PD-1/PD-L1免疫治疗中获益,因此,推荐对拟进行抗PD-1/PD-L1抑制剂治疗的患者检测PD-L1和TMB状态以评估其接受免疫治疗的可行性及疗效。
二、浆膜腔积液用于NSCLC
分子病理检测的优势
组织样本是NSCLC患者进行分子病理检测的首选,但是晚期NSCLC患者常较难获取组织样本,尤其是靶向治疗后耐药的患者。即使通过组织活检获得肿瘤组织,也可能会因为肿瘤细胞比例低或数量太少等原因无法完成后续分子检测,有研究通过回顾性分析发现,20%~30%的晚期NSCLC患者的组织样本无法满足二代测序检测的质控需求。当组织学样本不可及或质控不合格时,可使用浆膜腔积液样本作为替代进行分子病理检测。多个对比研究发现,从浆膜腔积液中分离出细胞沉渣进行分子病理检测得到的结果与组织样本相比具有较高的一致性。另外,从浆膜腔积液上清中分离出的游离核酸(cfDNA和cfRNA)也可用于分子检测,细胞沉渣和上清液两者可以互相补充,联合应用进行检测能够极大地提高分子诊断的准确性。除此之外,与组织样本相比,浆膜腔积液样本进行分子病理检测还具有以下优点:
(1)获取简单易行,无需特殊设备;
(2)胸腔积液和腹腔积液一般样本量较大,多能够提供足够的样本用于检测;
(3)NSCLC伴多发转移的患者,浆膜腔积液中的肿瘤细胞或游离核酸可能来源于多个病灶,对其进行分子检测可最大限度降低肿瘤间异质性的影响;
(4)晚期NSCLC患者有肿瘤占位往往会持续产生浆膜腔积液,可连续重复取样进行动态分子检测,以更好地评估疗效和预后。需要注意的是,虽然利用浆膜腔积液中分离出的细胞沉渣样本检测PD-L1和TMB与组织样本相比具有较高的一致性,但是有研究报道受肿瘤异质性及分期等影响,细胞学样本PD-L1免疫组织化学(IHC)阳性表达率常高于肿瘤组织样本,其一致性还需要大样本比对研究。另外,虽有研究报道利用浆膜腔积液上清中的cfDNA检测TMB的可行性,但其与免疫治疗疗效的相关性尚需更多临床研究进一步明确。
三、浆膜腔积液用于NSCLC
分子病理检测的适用人群
存在恶性浆膜腔积液的NSCLC患者已是晚期,不再适用于手术治疗,内科药物治疗是主要的手段,靶向治疗和免疫治疗可能能够延长这类患者的无进展生存期和总生存期,但需要进行分子检测筛选可能获益的人群,因此,当组织样本不可及或质控不合格时,推荐以下NSCLC患者利用浆膜腔积液进行分子病理检测。
1. 拟接受靶向治疗的NSCLC患者:存在恶性浆膜腔积液的NSCLC患者在接受靶向治疗前应进行靶点基因变异检测,当组织样本不可及或质控不合格时,强烈推荐使用浆膜腔积液对《非小细胞肺癌分子病理检测临床实践指南(2021版)》推荐的基因,包括必检基因EGFR、ALK、ROS1、MET,和扩展基因HER2、BRAF、RET、KRAS、NTRK进行检测,以精准筛选靶向治疗的潜在获益人群。
2.靶向治疗后耐药的NSCLC患者:对于TKI治疗后耐药的NSCLC患者,明确其耐药原因是后续调整治疗方案的重要依据,常见的TKI治疗耐药原因包括靶点构象改变(如EGFR突变的患者经过第一代或者第二代EGFR-TKI治疗后继发出现EGFR T790M突变,ALK融合的患者经过ALK-TKI治疗后继发出现ALK激酶域突变等)、旁路激活(如MET扩增、HER2扩增、KRAS突变及BRAF突变等)和表型转化(如肺腺癌TKI治疗后小细胞癌转化或鳞癌转化)。但此类患者二次活检风险较大,有相当一部分患者无法或不愿进行再次活检。相比于组织学样本,浆膜腔积液获取方便,因此强烈推荐靶向治疗耐药的存在恶性浆膜腔积液的NSCLC患者利用浆膜腔积液进行分子病理检测以探究其耐药的原因。
3. 拟接受免疫治疗的NSCLC患者:药物相关性研究发现,在晚期NSCLC中,PD-L1蛋白表达水平以及TMB状态均与抗PD-1/PD-L1免疫治疗的疗效呈正相关,因此,当组织学样本不可及或质控不合格时,推荐对拟接受抗PD-1/PD-L1抑制剂治疗的NSCLC患者进行PD-L1和TMB检测。
四、浆膜腔积液用于NSCLC
分子病理检测的常用标本类型
浆膜腔积液经过离心处理后,可以分为细胞沉渣和上清液两部分,两部分均可用于分子病理检测,若细胞沉渣中肿瘤细胞数量和比例合适,推荐首选细胞沉渣进行检测,细胞沉渣根据后续样本制作方式的不同,又可以分为细胞蜡块、液基和涂片样本。
1.细胞蜡块:细胞蜡块是在完成细胞病理学诊断的基础上进一步进行分子病理检测的良好介质。常用细胞蜡块的制作方法有直接离心固定凝集细胞蜡块法、琼脂凝集细胞蜡块法、血浆凝血酶凝集细胞蜡块法等,其制作效果差异不大,均可采用,推荐使用直接离心固定凝集细胞蜡块法。另外,制作成的细胞蜡块样本在进行分子病理检测前,需要进行肿瘤细胞比例及数量的评估,确保其满足分子病理检测的质控要求。
2.液基样本:细胞沉渣量不足以完成蜡块包埋制作的情况下,在液基涂片中对肿瘤细胞比例及数量进行评估,确保其满足分子病理检测质控要求的前提下,强烈推荐使用现存液基样本提取核酸进行分子检测,固定液可以使用乙醇、甲醇等,但是不同固定液是否会对分子病理的检测结果准确性产生影响尚需深入研究探索。因浆膜腔积液常表现为血性积液,其中含有大量的蛋白、红细胞、炎性细胞等可能会影响诊断和基因检测,而使用液基样本可有效改善血性浆膜腔积液带来的假阴性和假阳性。此外,如需IHC或荧光原位杂交(FISH)检测,液基样本还可以制备涂片进行检测,但需结合已经染色的涂片,注意评估肿瘤细胞数量,镜下正确区分肿瘤细胞和非肿瘤细胞。
3. 涂片样本(包括传统涂片和液基涂片):无法制作细胞蜡块且现存液基样本不可及时,已经染色用于诊断的传统涂片和液基涂片,若肿瘤细胞比例及数量满足分子检测要求时也可完成分子检测,如可通过宏观切割或者显微切割的方式将涂片上的细胞刮取下来收集后用于核酸提取及相应分子检测。
4. 上清液:细胞沉渣中肿瘤细胞比例太低或数量太少时推荐使用浆膜腔积液样本分离得到的上清液进行分子病理检测。需要注意上清液中游离核酸的含量常较低,检测结果特异度高但灵敏度较差。基于细胞沉渣和上清液的特点,必要时可将浆膜腔积液中分离出的细胞沉渣与上清液联合应用于分子病理检测,以保证检测结果的准确性。
五、浆膜腔积液分子检测前
处理及质控节点
为保证分子病理检测能够顺利完成并且检测结果真实可靠,专家组推荐按照下列流程对NSCLC患者的浆膜腔积液样本进行检测前质控(图1)。
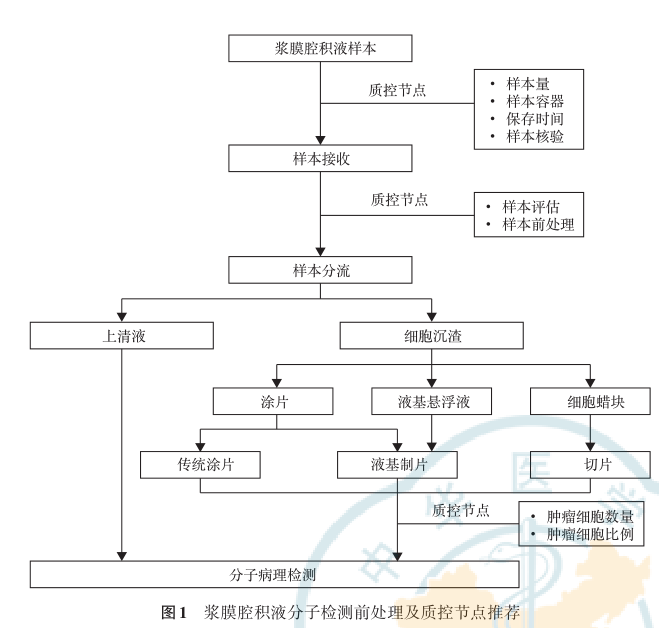
质控节点1:样本的接收。由于不同浆膜腔积液样本中肿瘤细胞含量不尽相同,基于分子病理检测的需要,推荐临床尽可能取100 mL以上送检,若临床无法满足要求,则送检全部样本。样本尽量应用无菌送检瓶,推荐使用硬质密闭容器,不建议使用引流袋等软质容器。强烈推荐浆膜腔积液在离体后应立即送细胞学室进行后续处理,暂时不能送检者推荐将样本冷藏在4 ℃冰箱内尽快完成送检。接收样本时要核对申请单和样本信息,推荐样本和申请单之间应至少核对2种标识,申请单除了患者基本信息之外,应填写与申请项目相关的临床资料,注明样本名称、送检时间、医师签名等项目。
质控节点2:样本的分流制片。浆膜腔积液在处理前须对样本进行评估,评估内容推荐包括样本离体时间、取样部位、样本总量、颜色、浑浊度及是否有沉淀或凝固等内容。合格的样本进行离心前可进行样本静置(有利于提高肿瘤检出率),分离细胞沉渣和上清液后,评估细胞沉渣的量,吸取沉淀物进行涂片,剩余用于包埋细胞蜡块;也可分作两管进行离心,一管用于制作涂片,一管用于制作细胞蜡块。
质控节点3:肿瘤细胞比例及数量评估。使用涂片或者细胞蜡块的切片评估肿瘤细胞,若需提取核酸进行分子检测,肿瘤细胞比例推荐不小于20%,涂片或细胞蜡块切片评估符合质控要求时,可利用液基样本或细胞蜡块提取核酸进行检测,当液基或细胞蜡块不可及时,可刮取涂片上细胞进行检测,必要时可选择性刮取以富集肿瘤细胞。若进行IHC或FISH检测,需制作相应的涂胶白片,且需评估肿瘤细胞数量是否达到了检测项目准确判读所要求的标准。
六、浆膜腔积液
分子病理检测的常用方法
目前NSCLC分子检测常用方法包括Sanger测序、FISH、IHC、即时荧光定量PCR、数字PCR、二代测序等,每种检测方法都有各自的技术特点及优缺点(表1),在实际检测中需结合浆膜腔积液样本的类型、检测目的及实验室条件选择合适的检测方法,必要时可进行多平台检测互补和验证。
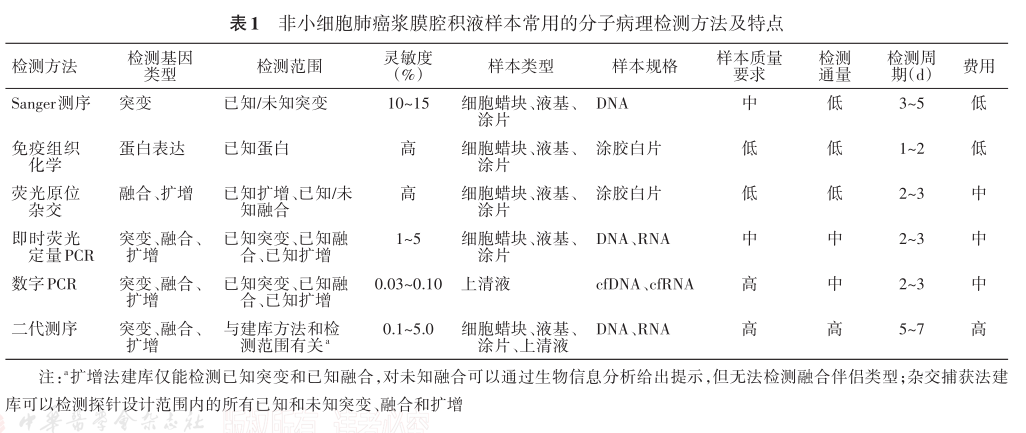
表1 非小细胞肺癌浆膜腔积液样本常用的分子病理检测方法及特点
七、浆膜腔积液
分子病理检测的优化策略
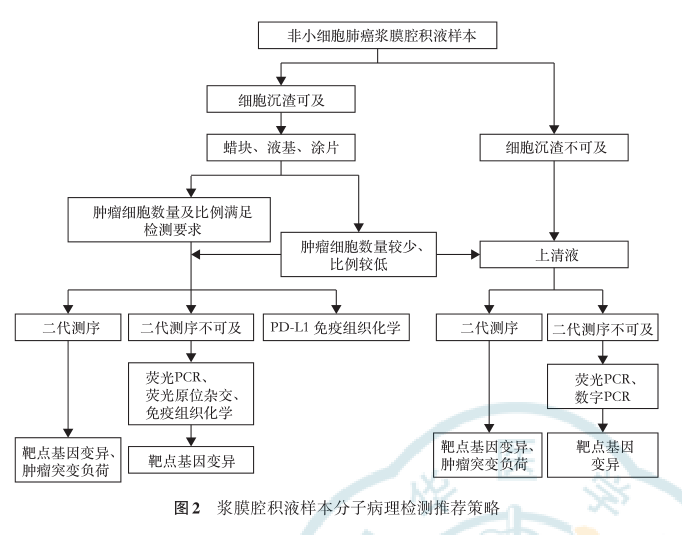
多种平台可以利用浆膜腔积液样本进行分子病理检测,其中,Sanger测序虽然是基因突变检测的“金标准”,但是因其灵敏度较差,不推荐作为NSCLC变异检测的常用方法。其他检测平台各具优缺点,结合临床实践经验和文献报道本共识推荐通过以下检测策略对NSCLC患者的恶性浆膜腔积液样本进行分子病理检测(图2)。浆膜腔积液样本离心处理后,如细胞沉渣量足够,推荐包埋细胞蜡块后进行靶点基因变异检测,可同时切片进行PD-L1 IHC检测,需注意PCR等传统检测平台和二代测序检测的优缺点(表1),根据临床需求及实验室条件选择最合适平台进行检测。对于二代测序平台,根据核酸提取物的不同可分为DNA二代测序和RNA二代测序,推荐首选DNA二代测序平台,RNA二代测序平台可作为靶点基因阴性/罕见融合病例的补充或明确检测结果的手段。需注意每种检测方法的局限性,必要时可多个平台联合应用。若细胞沉渣不足以包埋成蜡块,则可使用液基或涂片样本进行分子病理检测。若细胞沉渣不可及,推荐选取上清液进行检测,但需注意使用二代测序检测cfDNA TMB对NSCLC患者免疫治疗疗效的预测作用尚需更多前瞻性临床研究证实。另外,如上清液中未检出驱动基因变异,仍需要进行组织检测以排除液体活检假阴性的可能。对于细胞沉渣可及但经过细胞学评估肿瘤细胞数量较少(如少于100个细胞)或肿瘤比例较低(如低于20%)的样本,专家组推荐利用细胞沉渣和上清液同时或序贯进行分子病理检测,以最大限度筛选精准治疗的潜在获益人群。
八、浆膜腔积液
用于分子病理检测的注意事项
1. 浆膜腔积液样本在进行分子病理检测前均需由经过系统细胞病理学培训的医师进行肿瘤细胞数量及比例评估,并根据评估结果、检测目的及样本质量等因素选择合适的样本类型和检测方法。
2. 分子病理实验室利用浆膜腔积液开展分子检测需建立行之有效的质量控制体系,并定期开展室内质控和室间质控,以保证检测平台的稳定性和检测结果的可靠性。
3. 目前分子病理检测平台众多,但每种检测方法都有其优缺点,得到阴性结果时需要分析是否存在因检测方法的局限性或所用的浆膜腔积液特点导致的假阴性结果。另外,浆膜腔积液如固定不及时或保存时间过长等原因也可能会出现假阳性结果(如二代测序检出大量低频突变、IHC染色不均一等),必要时建议使用其他平台进行多维度验证。
4. 建立流畅的临床病理沟通平台,推荐组建由不同专家(包括临床医师、病理学家、分子病理学家、遗传学家和生物信息学家等)组成的分子肿瘤专家委员会,以有效对疑难病例或者特殊病例进行及时沟通交流,寻找最优解决策略。
非小细胞肺癌恶性浆膜腔积液分子病理检测中国专家共识要点见表2。


免责声明 本文中公布的临床实践共识内容由专家组成员依据现有医学证据及临床实践经验共同讨论形成,以帮助相关人员进行非小细胞肺癌恶性浆膜腔积液分子病理检测。其中的内容可能不够全面或不够充分。医学知识发展迅速,在本共识产生到发表期间均可能出现新的证据,而这些可能并没有体现在本共识中。另外,因检测流程复杂、实验室条件差异以及患者之间存在个体差异等影响检测决策或结果,因此,本共识中内容的采用应结合检测条件、政策许可以及专业人员的专业知识独立判断。对本共识内容的使用是自愿的。专家组成员明确否认对文中所提及的任何产品具有商业性目的。专家组对因使用本共识内容而造成的或与之相关的任何人身伤害或财产损失,或任何错误或遗漏不承担责任
作者:中华医学会病理学分会细胞学组
执笔人:李卫华(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院 北京协和医学院 肿瘤医院病理科,北京 100021)
通信作者:
张智慧(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院 北京协和医学院 肿瘤医院病理科,北京 100021),Email:[email protected];
刘东戈(北京医院病理科 国家老年医学中心 中国医学科学院老年医学研究院,北京 100730),Email:[email protected];
金木兰(首都医科大学附属北京朝阳医院病理科,北京100020),Email:[email protected]
非小细胞肺癌恶性浆膜腔积液分子病理检测
中国专家共识专家组成员
(按单位名称汉语拼音字母顺序排列)
北京医院病理科(刘东戈);复旦大学附属肿瘤医院病理科(平波);广东省人民医院病理科(梅平);国家癌症中心 中国医学科学院 北京协和医学院 肿瘤医院病理科(李卫华、张智慧);哈尔滨医科大学附属第一医院病理科(吴鹤);河南省人民医院病理科(胡爱侠);首都医科大学附属北京朝阳医院病理科(金木兰);首都医科大学附属北京胸科医院(车南颖);四川省肿瘤医院病理科(刘洋)
引用请注明:
来源:中华病理学杂志, 2022,51(12):1198-1204.
DOI: 10.3760/cma.j.cn112151-20220517-00424
(本共识获授权转载自微信公众号“ 中华病理学杂志”2023-01-03,未经授权,不得转载。)
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


