Nature Medicine观点文章 | 人类细胞图谱对医学的影响
时间:2023-01-23 18:01:47 热度:37.1℃ 作者:网络
细胞图谱有望提供基因、疾病和治疗之间“缺失的一环”。通过识别特定的细胞类型、状态、通路和疾病相关基因作用的环境,人们将在细胞和组织水平上了解疾病的机制,并可以利用这种理解来开发强大的疾病诊断方法;确定有希望的新药物靶点;预测其疗效、毒性和耐药机制;并开发从癌症疗法到再生医学的新疗法。
近日,剑桥大学团队联合Genentech公司团队在Nature Medicine上发表观点文章“Impact of the Human Cell Atlas on medicine”,展望了细胞图谱影响医学未来的潜力,并描述了过去十年中,该领域研究进展如何在常见复杂疾病、传染病(包括COVID-19)、罕见疾病和癌症中实现这一潜力。
 疾病发生是由于细胞状态改变以及细胞生态系统异常所导致的——这种改变或异常受到遗传因素和环境因素的驱动。为了深入了解疾病发生机制,发现并提供新的治疗方法,研究人员需要了解细胞内部信息,及其在健康和疾病中的相互作用。虽然几十年来,人们一直在朝这个方向努力,但技术挑战限制了人们更大规模、更精密尺度和更高分辨率来探究人类疾病的能力。
疾病发生是由于细胞状态改变以及细胞生态系统异常所导致的——这种改变或异常受到遗传因素和环境因素的驱动。为了深入了解疾病发生机制,发现并提供新的治疗方法,研究人员需要了解细胞内部信息,及其在健康和疾病中的相互作用。虽然几十年来,人们一直在朝这个方向努力,但技术挑战限制了人们更大规模、更精密尺度和更高分辨率来探究人类疾病的能力。
过去十年中,单细胞和空间基因组学的技术突破为健康和疾病领域的细胞和组织图谱研究开辟了道路,并影响了医学的各个方面。这些突破包括了解疾病基因起作用的细胞类型和通路,在细胞和多细胞水平上破译疾病发生和进展机制,定义疾病监测和诊断的新特征,发现和开发新的分子、基因和细胞疗法,并跟踪它们对患者的影响。
由于只有参照健康才能充分理解疾病,反之亦然,实现这一愿景将需要所有人类细胞的综合参考图谱,作为理解人类健康和诊断、监测和治疗疾病的基础。绘制人类细胞图谱带来了重大的管理和技术挑战,国际人类细胞图谱(HCA)计划正在应对这些挑战。
自单细胞分析方法出现不到10年,HCA推出5年以来,该领域在提供人类健康相关发现方面取得了巨大进步,并迅速开发和应用了新方法来解决医疗问题。在这里,我们探讨了细胞图谱加速生物医学发展的关键方式及其未来潜力。
了解疾病生物学:从基因到细胞、通路和组织
1.从疾病相关基因到作用细胞
遗传变异——无论是常见的还是罕见的——都可能会增加患病风险。人类遗传学研究已经确定了超过10万个与不同人类特征相关的遗传变异,但要了解这些变异在疾病中的作用,还必须了解其表达和作用细胞。在罕见疾病中,相关细胞类型可能是未知的,甚至是未发现的。在常见复杂疾病中,来自全基因组关联研究(GWAS)和全表型关联研究的候选位点通常位于非编码区域,这些区域难以连接到受影响的蛋白质编码基因、作用细胞或功能细胞。此外,即使常见和罕见疾病具有相似的临床表型,也可能是不同基因变异的结果,因此在通路或细胞水平上识别共同机制更具挑战性。
细胞图谱提供了一种解决这些挑战的方法。(图1)在罕见的孟德尔遗传疾病中,通过健康组织图谱发现了新细胞类型,包括罕见细胞,它们独特地表达关键疾病基因,甚至纠正了长期以来的假设。例如,肺离子细胞——在气管细胞图谱中发现的一种新型罕见细胞类型——是表达CFTR8、9的主要细胞类型,CFTR8、9是囊性纤维化的致病基因。特别是,对人类发育细胞图谱(HDCA)的研究可以揭示出生时表现的孟德尔遗传性疾病,例如发育中与成人肠神经系统中不同结肠病变体的细胞起源,或21三体对骨髓造血干细胞及其生态位的影响。
在常见的复杂疾病中,类似的分析在许多炎症、自身免疫、神经退行性疾病、呼吸、纤维化和其他疾病中,使用相关组织的健康和疾病图谱,揭示了新的关联。由于大多数风险变异位于非编码区域,整合GWAS汇总统计数据、细胞谱和染色质数据,以及细胞染色质和RNA的联合谱,可以进一步促进并发现此类关联。由于常见疾病基因通常具有多效性,更广泛的跨组织图谱有助于更好地解读它们在全身的影响。最后,图谱还允许研究人员从个体风险基因的水平转移到它们所参与的模块和通路,从而帮助破译基因功能,发现因果过程,并在通路水平上分析具有相似发病率的疾病,即使潜在的基因是不同的。
2.重塑疾病组织中的细胞组成和多细胞结构
细胞内在和细胞外在的变化在发病机制中都起着关键作用,并且可以作为治疗的靶标,但细胞内部通路的变化和细胞组成的变化在批量分析中往往会混淆。细胞图谱提供的细胞分辨率和越来越大的空间分辨率对此进行了区分,并允许在健康和疾病之间进行更准确和敏感的比较,如 IBD、哮喘、肺纤维化、类风湿性关节炎、糖尿病肾病、心肌病、阿尔茨海默病和许多其他常见疾病。
组分和细胞内在表达变化都可以在多种细胞类型之间进行协调,从而导致疾病中多细胞群落的转变。例如,将克罗恩病患者回肠中的细胞组成与健康参考图谱进行比较,确定了一个独特的免疫和基质细胞多细胞群落。与健康参照的比较也有助于破译驱动这些协调细胞群落的机制,以及它们组成细胞内的基因通路。例如,与健康组织相比,牛皮癣皮肤损伤的特征是特定类别的巨噬细胞和血管内皮细胞的扩张,它们分别通过趋化因子CXCL8及其受体ACKR1相互作用。最后,计算方法可以恢复多细胞基因通路,其中细胞内在通路在跨样本或物理生态位的多种不同细胞类型之间进行协调。
3.绘制肿瘤中恶性细胞和微环境细胞
细胞和空间基因组图谱也正在改变人们对癌症生物学的理解。将实体瘤与健康参考进行比较分析有助于绘制其生物学复杂性——将恶性区室中的遗传和表观遗传变异与肿瘤微环境中的细胞多样性相结合,有助于确定相关的疾病机制和治疗干预的机会,以及耐药机制,还可以预测对治疗反应的细胞群落,以及成人和儿童肿瘤的细胞起源。
图1: 人类细胞图谱的潜在医学影响和面临的挑战。左图,从细胞图谱中得出的关于疾病机制、诊断和治疗的重要见解。右图,影响医疗的关键技术和基本障碍,包括多样性、数据可用性和了解疾病进展。
诊断和治疗:对新临床方法的单细胞洞察
1.走向高分辨率细胞和组织诊断的未来
单细胞测序(如全血细胞计数(CBC)和白细胞计数)联合组织病理学,对体内所有细胞类型及其在疾病中作用的了解将改变普通诊断工具的未来。健康参考图谱、疾病图谱以及基础实验室和计算方法应允许开发具有更高分辨率和更广泛分子范围的新检测方法,以及改进对个体患者结果的解释(图1)。
对于CBC,我们设想未来的“CBC 2.0”,是一个有核血细胞的高分辨率图谱,可用于每种疾病。目前,丰富且不断增长的人类参考图谱涵盖了数千个个体和数千万个细胞,包括多种疾病的外周血单核细胞图谱和多种组织中的免疫细胞图谱。
这样的参考可以形成新的诊断分析和更好的解释基础,将外周细胞的特征与健康和疾病组织中的细胞特征联系起来。令人兴奋的是,血液免疫细胞图谱的单细胞分析开始为我们对治疗反应和预后的理解提供信息,包括已经确定肿瘤中抗PD1反应的血液相关开创性研究。
对于组织病理学这一医学主力军,我们设想将传统的H&E染色技术升级至H&E2.0技术。在未来H&E2.0的版本中,临床医生可以将单细胞转录组数据、空间转录组数据叠加在一张标准组织切片H&E染色图上,统一基因组学和组织学信息以辅助诊断,甚至可以通过针对空间数据的机器学习算法模型构建来预测H&E染色样本的分子图谱。这在单基因和多基因IBD中得到了很好地验证。目前的算法已经能够将低分辨率方法反卷积到单细胞分辨率,投射空间表达未直接检测的基因,并恢复组织中可重复的空间分子特征。 如果有足够的数据,算法还可以将分子图谱和组织学相互映射,目的是根据组织学预测表达,从而形成H&E 2.0方法的基础。
早期研究已开始显示此类未来分析的潜在影响,以及图谱如何提供必要的工具来解释为什么治疗在细胞和组织水平上对患者有效或无效,预测潜在的靶向毒性、疗效以及内在和获得性耐药的潜在机制。首先,根据表达治疗靶点的细胞类型,健康参考对于预测分子和细胞疗法的靶向毒性风险具有无可估量的价值。例如,近期一项研究表明,CD19在壁细胞、血管平滑肌细胞和血脑屏障周细胞中的表达可能解释CD19靶向嵌合抗原受体T细胞的神经毒性。用于安全评估关键模型(如大鼠和猕猴)的跨物种参考图谱将是无价的。对于癌症的反应和耐药性,分析肿瘤中的恶性和免疫细胞,引流淋巴结或外周可以帮助监测反应并提供耐药性的信息,例如,抗PD-L1治疗或化疗的反应。
2.用于药物发现的高分辨率和大规模并行方法
对于分子药物发现,参考图谱、单细胞和空间基因组学通过耦合丰富、复杂和可解释的分子谱表型(可能与患者细胞相关),为所需细胞状态的高分辨率表型筛选开辟了道路筛选。扰动序列筛选(具有单细胞基因组学读数的汇集遗传筛选)已经表征了大量基因、与常见复杂疾病相关非编码变异的扰动对单细胞谱的影响以及癌症和发育障碍中的编码变异,并且可以在细胞培养或共培养、类器官或动物模型中进行。同时,带有scRNA-seq的聚焦小分子筛选也开始进行。此外,机器学习算法可以越来越多地针对此类数据进行训练,以生成模型来预测同一细胞环境中一个或多个基因的额外扰动或新生物环境中相同扰动的影响。
对于再生医学和细胞治疗,单细胞图谱增强了我们在人类组织中恢复再生机制作为治疗靶点的能力,帮助药物发现开发更好的类器官模型,并定义更好的工程细胞疗法。在不同情况下,与参考图谱的比较首先有助于定义所需的靶标状态,然后有助于筛选达到该状态的细胞或类器官,最后有助于监测细胞治疗对人类患者的影响和状态。例如,在生成人体衍生模型时,健康和疾病参考图谱有助于比较模型和人体组织,识别缺失的细胞组分,并预测分子机制以改进模型,如帕金森病治疗、引入自闭症相关基因变异的脑类器官模型、肠道肠样培养物、胸腺T细胞和子宫内膜类器官模型。 此外,对于体内组织重编程,参考图谱有助于推断分化机制并评估治疗是否具有预期效果。最后,对于工程化细胞疗法,扰动序列方法有助于筛选可产生治疗所需细胞状态的扰动,单细胞分析有助于在对患者进行治疗之前,以及在对普通疾病和癌症的T细胞治疗之后,对所产生的效果进行描述。
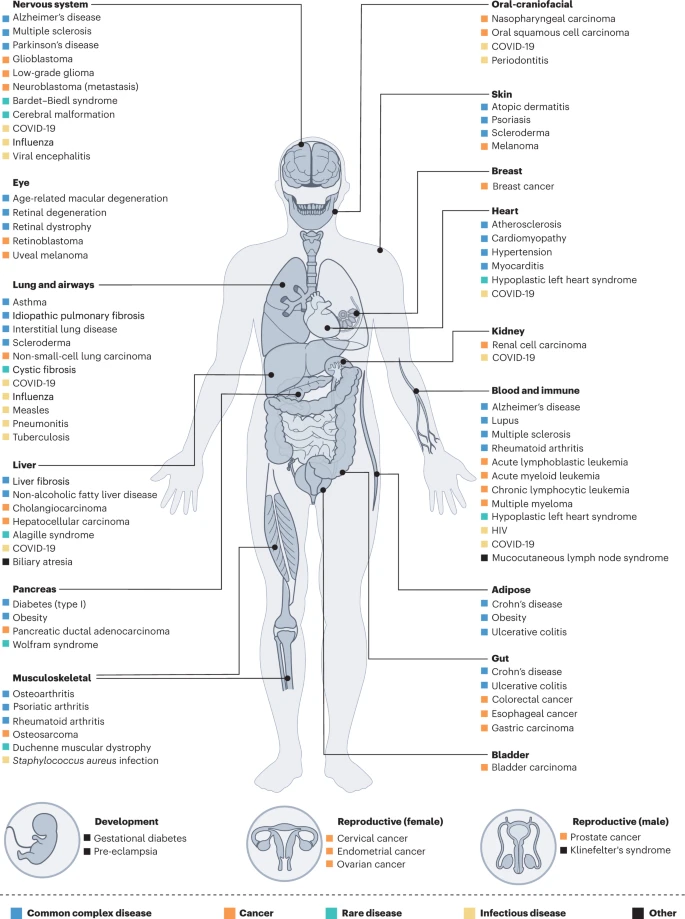
图2:HCA已收集到广泛的器官和疾病组织的单细胞图谱。上图展示健康组织中关键器官和系统(粗体),以及与不同组织相关的常见复杂疾病(蓝色)、肿瘤(橙色)、罕见疾病(绿色)、传染性疾病(黄色),或其他问题(黑色)。
细胞图谱在医学中面临的挑战
为了实现细胞图谱在医学中的变革潜力,需要克服技术、实践和基础方面的重大挑战(图1)。首先,我们必须确保细胞图谱能够造福全人类,实现这一目标的方法是绘制反映人类多样性(从祖先到地理)的健康和疾病图谱,并让全球各地精通这些方法的科学家参与进来。这一直是人类细胞图谱计划自成立以来的核心目标。
为了在现实环境中有效部署,实验室方法需要具有足够的成本效益和稳健性,以增强筛选和采用的能力,包括在资源贫乏的地区。实验室和诊所之间的联系也需要进一步加强,包括建立更多具有丰富元数据的生物样本库资源,对来自临床注释和不同队列的样本进行大规模分析,以及开发更好的实验方法来利用样本库样本,尤其是福尔马林固定样本的石蜡包埋问题,仍然与许多单细胞方法不兼容。
在关键的计算挑战中,需要开放数据来反映人类多样性以训练计算模型,同时适当保护患者隐私;从静态快照解码细胞动力学的方法;用于高效搜索靶标基因、细胞状态和细胞类型的算法和平台;以及实验室和计算之间的快速迭代,以设计用于筛选和治疗的人类来源类器官和细胞。
其他挑战更为根本。首先,虽然传统表达谱分析能够获得分子机制与疾病治疗的潜在关联,但是证明基因、信号通路、细胞状态的致病作用仍然需要更为直接的证据。在遗传筛选或人类遗传队列和临床试验中使用单细胞和空间基因组学,进行因果推断,将有助于实现我们对疾病的理解从相关性到因果性的质的飞跃。此外,虽然细胞图谱揭示了疾病发展过程中的许多变化,但它们通常侧重于疾病的发生,而不是预后和进展。纵向研究可以应对这一挑战,但需要长期投入。更广泛地说,细胞图谱是我们战胜疾病的武器库中的一个重要工具,但不是灵丹妙药。就像人类基因组计划对医学的影响,计划本身并没有“解决”疾病,而是为生物医学的许多领域奠定了关键基础。
结 论
单细胞和空间图谱的不断发展,改变了我们在细胞和组织水平上对不同疾病的理解,并为诊断学、药物发现和新治疗途径的发展提供了信息。这对COVID-19等新疾病,癌症等长期疾病以及罕见和常见复杂疾病都产生了影响。这一进展在很大程度上是由实验技术和计算算法的兴起所推动的,这些技术适用于生物医学各个阶段的研究,包括从了解机制到诊断和治疗疾病。随着测序技术、细胞操作和空间分析方面的技术进步,以及在规模和分辨率上迅速增长(成本下降),使得收集临床工作所需的跨性别、年龄、血统和人口统计学的不同参考图谱成为可能,同时,它们还能够在人类患者体内和患者之间进行大规模采样,这对于了解和监测疾病以及对药物发现至关重要的筛选实验是所必需的。这将有助于实现人类细胞图谱的目标:形成一个参考图谱,作为了解人类健康以及诊断、监测和治疗疾病的基础。


