西安交大王福ACS Nano:基于Toehold的CRISPR-dCas9转录激活系统用于肿瘤和糖尿病小鼠模型的时空可控基因治疗
时间:2025-04-04 12:11:59 热度:37.1℃ 作者:网络
【研究背景】
基因编辑技术代表了基因工程的一个革命性突破,为研究不同的生命过程和各种疾病提供了一个平台。CRISPR-Cas系统已被广泛用作基因组编辑工具,其中基于CRISPR-dCas9的转录激活系统作为一种有前景的基因治疗方法,正被广泛用于疾病治疗研究等领域。然而,如何实现对CRISPR-dCas9转录激活系统的有效时空控制限制了其广泛应用。近日,西安交通大学王福团队在美国化学学会旗下期刊《ACS Nano》上发表题为“Toehold-Based CRISPR-dCas9 Transcriptional Activation Platform for Spatiotemporally Controllable Gene Therapy in Tumor and Diabetic Mouse Models”的研究。该研究提出了一个miRNA响应的CRISPR-dCas9转录激活(mCTA)系统。该系统能够对哺乳动物细胞中内源性miRNA做出特异性响应,通过调控Fluc、DTA、PDX-1等不同的功能基因从而实现深层组织成像、肿瘤治疗及调节糖尿病小鼠血糖稳态等功能,为实现CRISPR-dCas9的有效时空调控提供了新方案。
【主要内容】
该研究创新性地将可编程的Toehold开关与dCas9-VPR连接,构建出mCTA系统,希望通过miRNA调控dCas9-VPR的表达。当特异性miRNA存在时,dCas9-VPR顺利表达,进而激活整个基因调控系统。通过对下游基因的替换,实现深层组织成像、肿瘤治疗及调节糖尿病小鼠血糖稳态等不同功能。
研究团队首先对系统的可行性进行验证,证实了mCTA系统确实对目标miRNA有响应;然后对系统的质粒配比、浓度依赖性响应、特异性、对内源性miRNA的响应等都做了相关验证,实现了系统的全方位优化(图1)。

图1. mCTA系统的验证与优化
随后研究评估了该系统的深层组织成像能力。下游基因选择荧光素酶基因Fluc,通过水动力注射法将mCTA系统递送到小鼠肝脏,然后进行体内生物发光成像(图2A)。结果表明,Fluc仅在引入外源性miR-21和m21CTA时在肝脏中显著表达(图2B,D),这表明miR-21激活了m21CTA系统。为了进一步证实mCTA系统对内源性miRNA的应答能力,我们创建了m122CTA系统。该系统由肝脏特异性miRNA-122控制。图像结果显示,由于内源性miR-122在肝脏中的特异性高表达,表现出稳健的发光信号。相比之下,m9CTA组与对照7*TRE-Fluc组无显著差异(图2C,E),进一步证实了mCTA的深部组织成像能力。
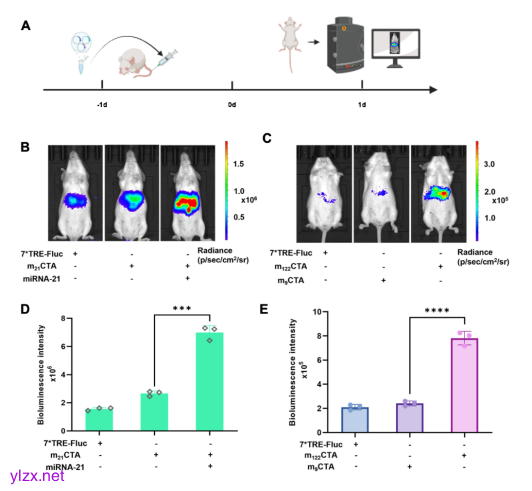
图2. mCTA系统深层组织成像能力的验证
接下来研究人员评估了mCTA系统在肿瘤治疗中的能力(图3)。首先在4T1乳腺癌细胞中验证了mCTA系统通过调控DTA基因抑制细胞迁移的能力,然后通过瘤内注射mCTA系统在小鼠皮下瘤模型中评估该系统应用于肿瘤治疗的能力。结果显示,m21CTA系统可以显著抑制肿瘤生长,这为 mCTA系统在肿瘤治疗中的应用提供了证据。
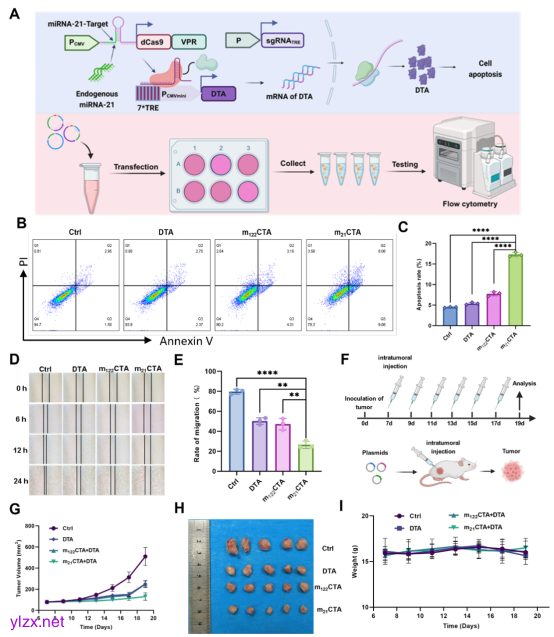
图3. m21CTA系统在肿瘤治疗中的应用
最后研究人员将该系统应用于糖尿病小鼠的治疗(图4)。首先通过STZ造模糖尿病模型小鼠,通过免疫组化、血液生化指标等证实糖尿病小鼠的构建成功。然后通过水动力法将系统质粒递送至小鼠肝脏,并记录治疗过程中小鼠的血糖变化。用 m122CTA系统处理的小鼠血糖指数明显下降,而用m21CTA处理的对照小鼠的血糖没有出现类似的下降。这一观察结果表明mCTA系统具有通过调控PDX-1基因调节糖尿病小鼠血糖稳态的能力。
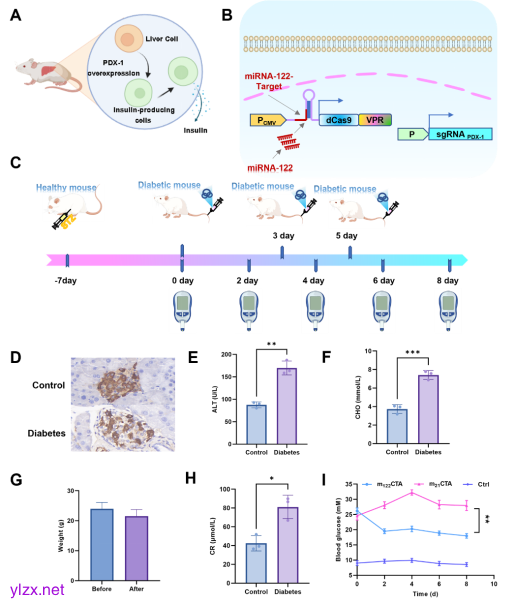
图4. m122CTA系统在糖尿病小鼠模型中的治疗应用
【小结】
该研究开发了一种可编程的miRNA控制的CRISPR-dCas9系统,实现了时空可控的目的基因激活。通过调控不同的下游基因如DTA或PDX-1,在癌症和糖尿病等多种场景中显示其治疗功能。该研究提供了一种通用策略,可应用于其他CRISPR-Cas系统,将有助于促进疾病诊疗在基因调控水平的提升。该研究论文第一作者为课题组博士生胡冲和博士后施潇蕊,通讯作者为西安交通大学王福教授。本研究得到了国家自然科学基金、陕西省自然科学基金等项目资助。
原文链接:


