《2022中国系统性红斑狼疮患者生殖与妊娠管理指南》解读
时间:2023-08-11 13:32:23 热度:37.1℃ 作者:网络
系统性红斑狼疮(SLE)是一种以育龄期女性为主要发病人群的系统性自身免疫病。近年来,随着SLE诊治水平的不断提升,SLE 患者的存活率显著改善,患病20年的存活率已超过60%,我国SLE 患者的长期存活率与国际水平相当,这使其婚嫁和生育成为临床医生无法回避的重大临床问题之一,生儿育女享受家庭幸福生活亦成为广大SLE 患者的强烈需求。
但由于妊娠与SLE病情之间复杂的相互作用,导致SLE患者妊娠期易出现病情复发或加重,SLE 患者妊娠后发生相关并发症如复发性流产、胚胎停育、早产、胎儿先天性心脏传导阻滞(CHB)、胎儿宫内生长受限(FGR)、胎死宫内等均显著高于非SLE患者,且与非SLE患者相比,SLE孕产妇的病死率升高超过20倍[1-2]。因此,如何提高妊娠成功率、改善母胎转归是SLE患者管理所面临的重要挑战之一。
为加强SLE患者的生殖与妊娠管理,规范SLE患者围妊娠期的监测与治疗,提高其妊娠成功率、降低母婴病死率,在国家皮肤与免疫疾病临床医学研究中心、国家妇产疾病临床医学研究中心、中国风湿免疫病相关生殖及妊娠研究委员会、国家风湿病数据中心、中国系统性红斑狼疮研究协作组共同组织和领导下,2022年11月我国发布了首部“中国系统性红斑狼疮患者生殖与妊娠管理指南”[3]。
该指南紧密围绕SLE妊娠相关重要临床问题和场景,以循证证据为基础,以多学科协作方式,严格按照指南制订程序,共形成13条推荐意见,涉及孕前准备、妊娠期疾病监测与治疗、胎儿监测与并发症诊治、产后随访与哺乳注意事项及新生儿监护的母婴全程管理。本文将对该指南的主要推荐内容进行解读,以使读者更好地理解和掌握其核心内容。
1 孕前准备
由于SLE患者妊娠过程中并发症的发生率显著高于同龄非SLE女性,总体而言,SLE患者的妊娠属于病理性妊娠。因此,SLE患者的妊娠必须是有计划的,计划妊娠、孕前全面细致的风险评估及危险分层是成功妊娠的关键。一般来说,SLE患者的孕前准备工作应始于避孕措施的选择。
1.1 SLE患者避孕措施的选择
所有育龄期SLE患者无论有无生育需求,在计划妊娠前均应采取严格的避孕措施,以避免非计划妊娠。SLE患者可采取的避孕措施包括宫内节育器、工具避孕、口服避孕药及皮下埋植避孕药等。
工具避孕可作为所有SLE患者的基础避孕措施,但单独工具避孕通常达不到严格避孕的效果,应配合其他避孕措施同时使用。
病情稳定的SLE患者服用含雌、孕激素的复合口服避孕药并不增加SLE病情的复发风险,但对于抗磷脂抗体(APLs)阳性、肾病综合征及既往有血栓病史的患者,不建议口服含雌激素成分的避孕药。
1.2 孕前妊娠风险评估
有生育需求的SLE患者应常规接受孕前咨询及妊娠风险评估。孕前评估内容不仅包括既往妊娠史和既往妊娠转归(如妊娠合并症的发生情况)等,还包括与妊娠转归密切相关的合并疾病相关表现,如是否出现抗磷脂抗体综合征(APS)相关临床表现等。
目前,患者SLE疾病活动情况、一些与妊娠和胎儿转归密切相关的特殊抗体及用药情况,是否合并存在其他影响妊娠转归的共患疾病如高血压、糖尿病和甲状腺疾病等均是孕前疾病评估与妊娠风险评估的重要内容。对这些风险因素的正确评估不仅为制订合理的妊娠计划提供了依据,也为患者及家属理解可能发生的不良事件提供了依据。
由于一些治疗SLE的药物存在致畸风险,在备孕之前患者需停用一定的时间,才能将其致畸风险降至最低。因此,指南建议女性SLE患者在备孕期应停用沙利度胺、甲氨蝶呤、吗替麦考酚酯、环磷酰胺、来氟米特等药物,其中沙利度胺、甲氨蝶呤和吗替麦考酚酯应停用3 个月,环磷酰胺应停用6个月[4-5]。来氟米特可经肝肠循环被再吸收,停药后2年方可自然消除,因此建议应用螯合剂消胆胺(8 g,3 次/d,连续11 d)清除后停药6 个月方可备孕[6]。
指南对男性SLE患者备孕前药物停用也给出了详细推荐,如男性SLE患者在备孕前应停用环磷酰胺至少12周,停用沙利度胺至少4周。男性SLE患者在备孕期推荐使用的药物为羟氯喹和硫唑嘌呤。
1.3 可选择的辅助生殖措施
药物暴露、环境因素及重要器官损害等多种因素可能导致SLE患者的生育能力衰减,因此一些低生育能力的SLE患者希望通过辅助生殖措施助孕。研究显示,使用辅助生殖技术可增加低生育能力SLE患者的妊娠成功率,其获益高于风险。
因此,指南指出SLE患者使用辅助生殖技术的适应证包括:
(1)符合不育症诊断标准者;
(2)符合体外受精胚胎移植指征者。
但进行体外受精胚胎移植时采取的控制性卵巢刺激措施会使血清雌二醇水平明显高于生理状态,可能诱发SLE活动及增加动静脉血栓形成的风险。
因此在使用该辅助生殖技术期间,对于APLs阳性但不满足2006年悉尼修订APS分类标准的患者,建议使用预防剂量的低分子肝素治疗;对于符合APS分类标准的患者,建议使用治疗剂量的低分子肝素治疗。
指南建议在刺激卵巢时使用低分子肝素,在取卵前24~36 h停用低分子肝素,取卵后继续使用低分子肝素。若未发生妊娠,该治疗方案一直持续至血清雌二醇水平恢复或接近生理状态。
2 妊娠时机选择
SLE患者妊娠的最佳时机选择和禁忌证是避免妊娠期SLE疾病活动、实现成功妊娠的重要因素。根据被广泛认可的临床专家共识,指南推荐SLE 患者在同时满足下述条件时方可考虑妊娠:
SLE 病情稳定≥6个月、口服泼尼松≤15 mg/d(或等效剂量的非含氟类糖皮质激素)、停用可能致畸的药物(如环磷酰胺、甲氨蝶呤、吗替麦考酚酯、来氟米特、雷公藤等)至所需时间、24 h 尿蛋白定量≤0.5 g且无重要脏器损害。
SLE患者妊娠前合并晚期肾病(慢性肾脏病Ⅳ~Ⅴ期),妊娠后将增加肾功能进一步恶化的风险,有可能导致患者在妊娠期或产后接受肾脏替代治疗[7]。
SLE患者合并严重肺间质病变将导致肺活量显著降低,当用力肺活量<1 L时发生妊娠期不良事件显著增加。基于临床共识建议,当用力肺活量<1 L时,建议患者避免妊娠或考虑终止妊娠[8]。
心力衰竭失代偿期显著增加孕妇死亡风险,因此,指南指出存在下述任意情况之一者则不推荐妊娠:肺动脉高压(PAH)、重度限制性肺疾病[如用力肺活量<1 L、严重心力衰竭、慢性肾衰竭(血肌酐≥247 μmol/L)]、既往严重子痫或子痫前期以及难以控制的HELLP 综合征导致胎儿丢失、既往6 个月曾出现SLE疾病活动、卒中等。
3 妊娠后随访与病情监测
鉴于SLE患者妊娠期间病情的复杂多变性,由风湿免疫科医师主导的多学科协作更利于SLE患者的妊娠管理。
指南推荐妊娠28周前每4周随诊1次,自第28周始每2周随诊1次;在明确妊娠后,需行胎儿彩色多普勒超声检查,明确胎儿的确切胎龄。风湿免疫科随访的目的是及时发现病情变化和脏器损害,对SLE患者的病情进行准确判断;产科随访的目的是监测胎儿的生长情况及是否发生畸形。
这里需强调的是,如果风湿免疫科或产科医生判断患者病情发生变化或并发症的潜在风险显著升高,则应缩短随访时间间隔,以尽早发现病情变化及并发症,并给予积极治疗。
表1列出了风湿免疫科和产科在SLE患者不同孕周的随访频率和随访内容,为制订个体化随访计划提供了详细指导。
表1 SLE患者妊娠期随访频率和随访内容
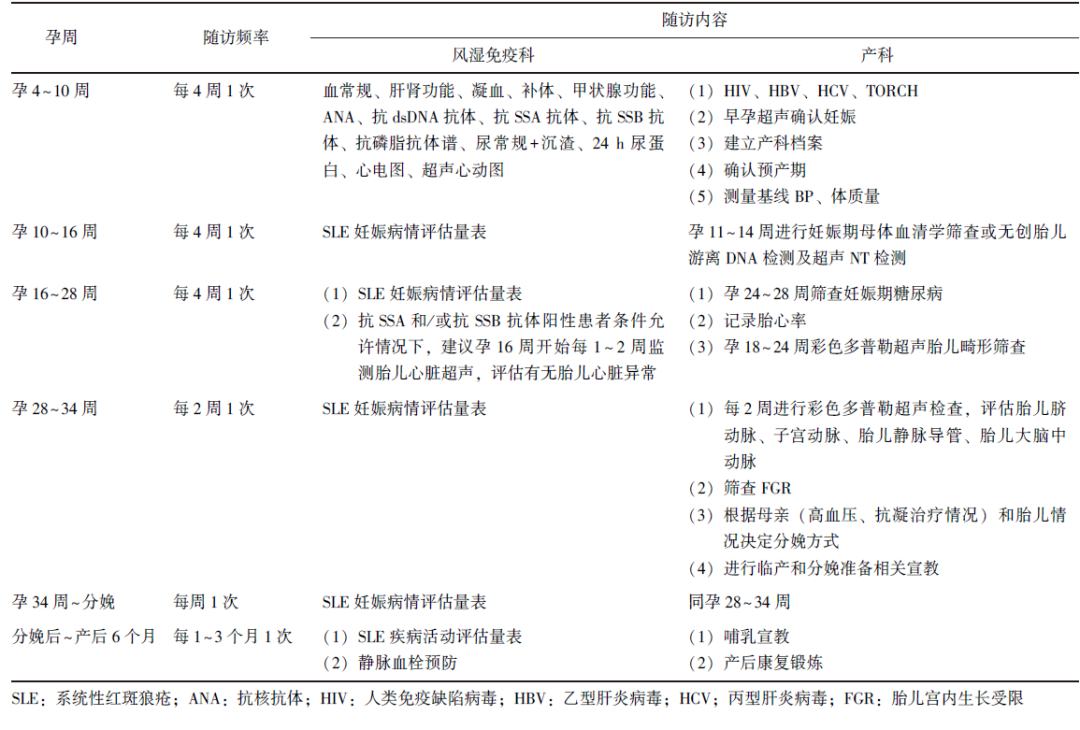
4 妊娠期间药物使用原则
大多数SLE患者在备孕和妊娠期间均需使用一定的药物维持病情稳定,因此如何选择对胎儿安全的药物十分重要。妊娠期间使用的药物涉及糖皮质激素、传统合成的免疫抑制剂及近年来逐渐开始在临床使用的生物制剂类免疫抑制剂(表2)。
表2 SLE患者妊娠期和哺乳期药物应用
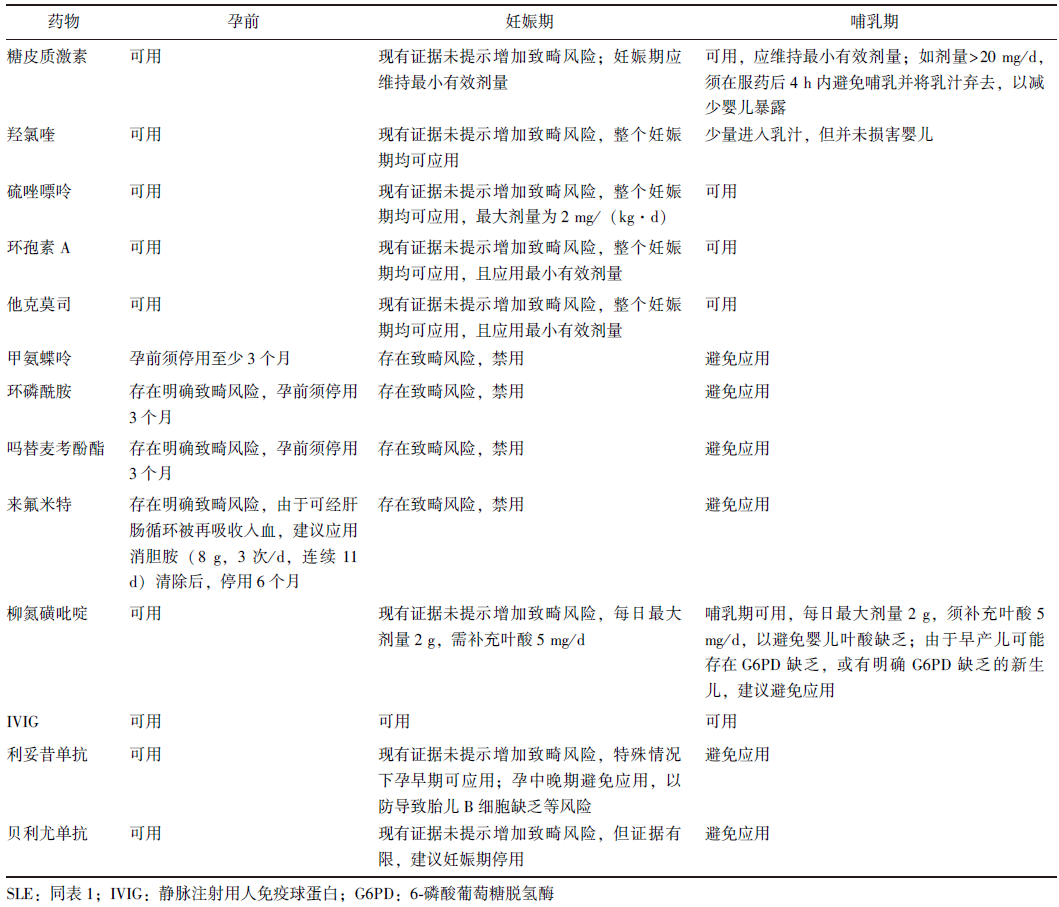
糖皮质激素是控制SLE病情的基础药物,大多数SLE患者使用低剂量的非含氟类糖皮质激素使病情得到控制后进入妊娠阶段,糖皮质激素的合理使用对患者和胎儿获得良好妊娠结局至关重要。
胎盘中的11β-羟类固醇脱氢酶可降解非含氟类糖皮质激素,因此醋酸泼尼松剂量小于20 mg/d时基本不进入胎儿循环,妊娠期使用小剂量糖皮质激素是安全的[9-10]。但糖皮质激素可增加妊娠期高血压、糖尿病、感染、胎儿发育迟缓、胎膜早破等风险,因此应尽量使用可控制病情的最小剂量,建议泼尼松维持剂量≤15 mg/d(或等效其他非含氟类糖皮质激素)。对于孕前病情稳定的SLE患者,妊娠后无需额外增加糖皮质激素剂量。
羟氯喹可降低SLE妊娠患者的疾病活动度及复发风险,改善其妊娠结局,并在预防子痫前期及胎儿心脏传导阻滞方面发挥作用,且对胎儿及新生儿无明显不良影响[11-15]。因此,如无禁忌,妊娠期间可安全使用,建议使用剂量为0.2 g,每日2次。
SLE患者妊娠期间使用硫唑嘌呤和钙调磷酸酶抑制剂(环孢素A、他克莫司)可降低疾病的复发风险,有助于控制病情并改善胎儿结局,同时未发现其致胎儿畸形,如病情需要可考虑使用。妊娠中晚期使用环磷酰胺并未显著增加胎儿致畸风险[16],在SLE病情重度活动或危及生命且常规治疗效果不佳时,经与患者及其家属充分沟通后可考虑应用。
贝利尤单抗、泰它西普和利妥昔单抗的妊娠期安全性相关研究数据有限,妊娠期间应尽量避免使用,仅当对患者的潜在获益大于风险时,仔细权衡利弊后方可考虑应用。
5 妊娠期间疾病复发或加重的治疗
妊娠期间雌激素水平显著升高可增加SLE患者的病情复发风险或使原有疾病加重。SLE患者妊娠期及产后3个月病情复发比例明显增加,复发率为25%~65%[17-18],显著高于非妊娠期SLE患者,因此在妊娠期间和产后1年内不仅需对患者病情进行严密监测,还需对疾病活动度和严重程度进行准确判断,此二者是决定选择恰当治疗的关键。
SLE患者出现下述情况中的任何一项均提示疾病活动:
(1)原有脏器损害加重;
(2)新发脏器受损;
(3)须增加糖皮质激素和/或免疫抑制剂的剂量和种类以控制病情。
因此,指南建议SLE患者妊娠期间应遵循以下原则对疾病进行管理。
5.1 按照病情严重程度分层治疗
虽然妊娠期间大多数患者的病情复发为轻度,表现为皮疹、关节炎、轻度贫血、轻度血小板减少、少量尿蛋白、补体减低等,但近30%的患者可出现严重复发,尤其是一些重要脏器受累,导致不良妊娠结局,因此根据疾病复发或加重的严重程度分层精准治疗是提高SLE患者妊娠成功率、减少药物不良反应的关键。指南指出:
(1)对于病情轻度活动者,推荐使用小剂量非含氟类糖皮质激素(泼尼松≤20 mg/d)治疗,可联用免疫抑制剂,以减少糖皮质激素在妊娠期的累积剂量,降低发生长期不良反应的风险;
(2)对于病情中重度活动者,推荐使用相当于泼尼松1 mg/(kg·d)的非含氟类糖皮质激素或甲泼尼龙冲击治疗,同时联合免疫抑制剂治疗。
与常规治疗剂量的糖皮质激素相比,大剂量糖皮质激素冲击治疗可快速控制病情,其不良反应发生率并未显著升高。因此,使用糖皮质激素和免疫抑制剂时应根据患者疾病活动度、妊娠周数等对剂量进行酌情调整。大于10 mg/d泼尼松(或相当剂量)的糖皮质激素剂量可增加早产、胎膜早破和FGR的发生风险[19],因此病情控制后应尽快将糖皮质激素减至最小有效剂量。静脉注射用人免疫球蛋白(IVIG)是妊娠期可选择应用的治疗方案,以改善部分SLE患者的血液系统及肾脏损害。
5.2 妊娠期狼疮肾炎的治疗
狼疮肾炎是妊娠期疾病复发时最常出现的脏器损害。75%妊娠期复发的SLE患者可合并狼疮肾炎,妊娠期间及产后1年内发生狼疮肾炎的风险显著增高,复发率约为30%[20],既往患有狼疮肾炎的患者,妊娠期间狼疮肾炎的复发风险更高。
活动性狼疮肾炎是预测不良妊娠结局的重要指标。妊娠期间出现活动性狼疮肾炎者,其狼疮病情恶化、胎儿丢失、子痫前期或子痫、早产、FGR等不良妊娠发生率均明显升高。
指南推荐:对于轻度狼疮肾炎活动者,应使用相当于泼尼松<0.5 mg/(kg·d)的非含氟类糖皮质激素,可联合使用妊娠期可使用的传统免疫抑制剂;对于中重度狼疮肾炎活动者,可口服或静脉输注大剂量糖皮质激素或甲泼尼龙冲击治疗、IVIG及联合使用妊娠期可使用的传统免疫抑制剂,同时可予β受体阻滞剂、钙离子拮抗剂控制血压,但血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂类药物可能导致不可逆性胎儿肾功能损伤、胎儿丢失及潜在的致畸作用,妊娠期应禁用。
5.3 妊娠期合并血小板减少的治疗
SLE患者妊娠期血小板减少的发生率为23%~54%,可发生于妊娠各个时期,包括产后。除SLE疾病活动、血栓性微血管病可导致妊娠期发生血小板减少外,妊娠期高血压性疾病(子痫前期/子痫、HELLP综合征)、感染及药物因素亦可造成患者血小板减少。
因此,指南建议结合患者的血小板减少程度和是否出现出血相关的临床表现、孕龄、SLE 疾病活动度及既往药物治疗史等综合判断后予以治疗。
糖皮质激素、IVIG可作为一线治疗,IVIG推荐用法为400 mg/(kg·d),用药3~5 d,如有必要,2周后可重复应用。对于重度血小板减低合并严重、危及生命的出血风险,可考虑静脉输注甲泼尼龙冲击治疗;对糖皮质激素依赖或抵抗者,可考虑重组人血小板生成素或联合钙调磷酸酶抑制剂(环孢素A、他克莫司)、硫唑嘌呤等妊娠期可应用的免疫抑制剂。
值得注意的是,SLE相关血小板减少的治疗目标是维持安全水平的血小板计数以防止发生出血,而非使血小板计数恢复正常,有时也很难通过治疗使血小板达到正常水平。
通常血小板计数>50×109/L时,经阴道分娩是安全的;SLE患者临近分娩需硬膜外麻醉下行剖宫产时,在应用标准方案治疗后,如血小板计数仍低于安全手术要求,可考虑术前输注血小板至安全水平后再行手术治疗。
5.4 妊娠期出现肺动脉高压或原有肺动脉高压加重的治疗
近年来,尽管对PAH的深入认识及靶向药物的广泛应用,妊娠合并PAH的病死率有所降低,但仍高达5%~23%[21],且妊娠期并发症多发,因此建议合并PAH者避免妊娠。
妊娠期间雌激素水平升高对血流动力学的影响为PAH患者围产期极易发生心源性休克,因此妊娠期间出现PAH或原有PAH加重的SLE患者,其妊娠期病死率显著升高[22],主要死因为右心衰竭、心源性猝死、PAH危象、子痫前期和感染。
因此,指南建议妊娠期出现PAH或原有PAH加重者应在孕22周前终止妊娠;如继续妊娠,建议转至专业的PAH诊治中心进行评估、治疗和密切随访。
指南推荐妊娠期间治疗PAH可考虑使用的药物包括:
前列环素类似物和/或磷酸二酯酶5抑制剂(西地那非、他达拉非)及前列环素类似物(伊洛前列素、曲前列尼尔)。内皮素受体拮抗剂、鸟苷酸环化酶激动剂等具有明确致畸风险,不建议妊娠期应用。
6 合并抗磷脂抗体阳性或产科抗磷脂抗体综合征的妊娠期管理
APLs阳性对SLE患者的妊娠转归具有深远影响,不仅与早期复发流产密切相关,也与妊娠中晚期胎盘功能障碍和胎儿死亡关系密切,因此在SLE患者妊娠过程中对APLs阳性患者进行分层管理是妊娠成功的关键之一。
对于APLs 阳性的SLE 患者,其妊娠期管理应根据既往有无病理性妊娠史、血栓史及APLs 阳性类型进行分层,制订个体化治疗方案,推荐使用低剂量阿司匹林和/或低分子肝素进行治疗;若无禁忌证或不耐受,推荐妊娠期全程服用羟氯喹。
指南推荐的分层治疗方案如下:
(1)既往无血栓病史的早期反复流产或晚期妊娠丢失的APLs 阳性SLE患者,建议在尝试受孕时开始应用低剂量阿司匹林治疗(50~100 mg/d),并在证实宫内孕后开始使用预防剂量的低分子肝素治疗;
(2)既往无血栓病史但出现胎盘功能不全相关早产的APS 患者,建议妊娠早期开始使用阿司匹林(50~100 mg/d),同时联用预防剂量低分子肝素治疗并持续整个妊娠期,当阿司匹林治疗失败或当胎盘检查提示大量蜕膜细胞炎症或血管病变和/或血栓形成时,建议阿司匹林联合治疗剂量的低分子肝素抗凝治疗;
(3)既往有血栓病史的APS患者,在妊娠期应接受治疗剂量的低分子肝素抗凝治疗,如合并病理性妊娠史,建议在妊娠期采用治疗剂量的低分子肝素联合阿司匹林治疗;
(4)对于临床无相关表现的APLs阳性SLE患者,建议单用阿司匹林(50~100 mg/d)治疗即可;
(5)对于经规范的阿司匹林联合低分子肝素抗凝治疗后仍发生不良妊娠结局的难治性产科APS 患者,建议妊娠前使用阿司匹林和羟氯喹联合治疗,妊娠前3个月可考虑加用小剂量(≤10 mg/d)泼尼松或同等剂量的非含氟类糖皮质激素。静脉应用丙种球蛋白、治疗性血浆置换可能为有效治疗手段,但大剂量糖皮质激素和其他细胞毒性药物(如环孢素A等)等对此类人群无效,且在一些患者中还存在副作用,不推荐应用。
对于临床表现未达到2006年悉尼修订的APS分类标准者,如存在连续2次不明原因流产、3次及以上非连续不明原因流产、晚发型子痫前期、胎盘早剥、晚期早产,具有符合产科APS分类标准的APLs实验室检测结果的非标准产科APS患者,存在再次出现病理性妊娠的风险,建议参照产科APS标准治疗(阿司匹林联合低分子肝素),以改善患者妊娠结局。
7 SLE患者胎儿心脏损害的识别和防治
超过半数的SLE患者体内可检测到抗SSA抗体和/或抗SSB抗体,一些患者体内还可检测到抗RNP抗体。自妊娠16周起,这些抗体即可通过胎盘的主动转运,透过胎盘屏障进入胎儿循环系统,造成抗体介导的胎儿心脏损害,其对心脏的损害包括心律失常、心内膜弹力纤维增生、瓣膜损害、扩张型心肌病等[22]。
心律失常中最常见的表现为房室传导阻滞(AVB),部分Ⅰ度和Ⅱ度AVB经治疗后可恢复,部分患者可进展至Ⅲ度AVB,其预后不良,10%~29%的Ⅲ度AVB胎儿发生宫内死亡,63%~93%的胎儿出生后需植入永久性心脏起搏器[23]。
抗SSA抗体和/或抗SSB抗体阳性的SLE患者首次妊娠发生胎儿心脏损害的概率为1%~2%,合并甲状腺功能减低者更易出现。
抗SSA抗体和/或抗SSB抗体阳性孕妇的胎儿均应视为发生心脏异常的高危胎儿,应进行筛查。胎儿超声心动图能够早期识别并诊断胎儿心脏损害,是目前最常用且有效的筛查方式。
推荐对抗SSA抗体和/或抗SSB抗体阳性的孕妇,自妊娠16周起常规行胎儿心脏超声心动图检查,每2周1次,直至26~28周。
推荐采用频谱多普勒测量房室传导时间(即AV间期),如AV 间期≥140 ms则提示可能出现传导异常,可考虑给予干预或密切监测,缩短至每周行超声心动图检查;如AV间期≥150 ms则可诊断为Ⅰ度AVB,需积极治疗,以免进展至Ⅲ度AVB。
对于胎儿超声心动图发现为Ⅰ度AVB者,建议予以地塞米松口服治疗,每日4~8 mg,治疗1~2周。如进展为Ⅲ度AVB则停用地塞米松;如恢复窦性心律或维持稳定,则考虑地塞米松减量至每日4 mg 维持,以防病情进展。
对于Ⅲ度AVB者,多项关于胎儿AVB的回顾性研究显示地塞米松治疗无效,因此不推荐使用。发生过妊娠期胎儿心脏损害的女性,后续妊娠再次发生胎儿心脏损害的概率显著增至17%~19%,羟氯喹可在一定程度上预防CHB的发生。
因此,指南建议SLE患者妊娠前服用羟氯喹以降低抗SSA抗体和/或抗SSB抗体相关胎儿心脏损害的发生率及再发生率,推荐剂量为400 mg/d。
8 早期识别妊娠期并发症
SLE患者的重要妊娠并发症包括胎膜早破、早产、FGR、子痫前期/子痫、产褥期感染等,其发生率较普通人群高2倍;血栓事件、血小板减少、妊娠期糖尿病、高血压、PAH、肾功能受损等并发症亦均显著高于普通人群,因此提前预警、早期识别、及时干预是防治严重妊娠期并发症的关键。
SLE妊娠患者早产的发生率为20.8%,胎膜早破是早产的主要原因[24],狼疮肾炎和SLE疾病活动是发生早产最强的预测因素[25],高血压、蛋白尿及APLs阳性亦与早产相关。
FGR在SLE患者妊娠期间较为常见,发生率为11%~29%,尤其是狼疮肾炎患者[26]。FGR与围产期胎儿病死率、儿童短期和长期神经系统并发症发生风险增加相关[27]。胎儿脐动脉血流超声检查有助于早期识别FGR,并预测其转归。
子痫前期和子痫是严重的产科并发症,SLE患者子痫前期和子痫的发生率均显著高于普通人群,已知狼疮肾炎、血小板减少、补体水平降低、补体调节蛋白基因突变及APLs阳性均是SLE患者发生子痫前期的危险因素。
一项纳入32 217例妊娠女性的系统评价研究显示,子痫前期发病的高风险患者妊娠期应用阿司匹林可使子痫前期风险降低24%[28]。因此,指南推荐合并上述高危因素的SLE患者,妊娠16周前开始服用阿司匹林以降低子痫前期的发生风险,建议特定情况下(高龄产妇、多个APLs阳性或LAC阳性、辅助生殖妊娠等),除阿司匹林外亦可使用低分子肝素,剂量和疗程应根据患者个体情况制订。
9 分娩方式选择及相关糖皮质激素剂量调整
SLE 疾病本身并非剖宫产指征,分娩方式的选择应根据患者的个体情况由产科医生决定。对于病情稳定的患者,如果胎儿已发育成熟,指南建议孕39周即终止妊娠,如无剖宫产指征,建议采取阴道试产;接受阿司匹林治疗的患者在孕36周后考虑停药,以降低阿司匹林相关围术期出血风险;接受低分子肝素治疗的患者建议在分娩前12~24 h停药,分娩后如无明显出血,应尽早恢复原剂量低分子肝素治疗。
SLE疾病活动可诱发妊娠期高血压,尤其合并狼疮肾炎者。当高血压控制欠佳,进展为重度妊娠期高血压、子痫前期/子痫或HELLP 综合征时,及时终止妊娠可挽救母体生命。当SLE患者并发肺部疾患、神经精神异常时,亦可显著增加不良妊娠结局的发生率,当出现母体弥漫性肺部受累以致呼吸衰竭或出现神经精神异常、脑血管意外事件时,母亲病死率显著升高[29],故应考虑及时终止妊娠。
SLE合并PAH者在妊娠期病情可进一步恶化,尤其在妊娠中晚期。同时,SLE患者可在妊娠期新发PAH,当病情进展至中重度时,母亲病死率则显著升高。当尿蛋白进行性升高或24 h尿蛋白定量≥3 g时,均提示SLE病情难以控制,可能导致不良母胎结局,应考虑及时终止妊娠,以缓解SLE 疾病活动对母体产生的不良影响。
因此,指南建议出现下述任一情况时,应尽早终止妊娠:
妊娠前3个月即出现明显的SLE疾病活动、SLE 病情严重危及母体安全、妊娠期监测发现胎盘功能低下危及胎儿健康、重度妊娠期高血压、精神和/或神经异常、脑血管意外事件、弥漫性肺部疾病伴呼吸衰竭、重度PAH、24 h 尿蛋白定量≥3 g。
由于大多数SLE患者使用糖皮质激素维持病情稳定后进入妊娠过程,因此在因病情变化需提前终止妊娠或病情稳定自然分娩时,均需对糖皮质激素剂量进行调整。
如患者因病情需要在妊娠34周前、预计1周内计划分娩时,均应接受含氟类糖皮质激素促胎肺成熟治疗,建议分娩前>24 h应用地塞米松5 mg或6 mg肌肉注射,每12小时1次,连续4次,或倍他米松12 mg,肌内注射,每天1次,连续2 d[30]。
对于病情稳定且口服糖皮质激素剂量≤泼尼松5 mg/d(或等效剂量其他糖皮质激素)的患者,行人工流产、中期引产、正常分娩或剖宫产手术时,建议继续使用原剂量糖皮质激素[31]。
当长期口服糖皮质激素剂量大于泼尼松5 mg/d(或等效剂量其他糖皮质激素)或存在临床库欣综合征时,建议根据手术对人体产生的应激程度补充围术期糖皮质激素剂量,以预防肾上腺皮质功能不全。
对于行人工流产、中期引产手术或正常分娩者,在原糖皮质激素基础上,手术当日或产程启动时服用泼尼松5 mg或静脉注射氢化可的松25 mg,次日恢复原口服剂量即可;对于行剖宫产术者,在原糖皮质激素剂量的基础上,手术当日于术前或术中增加静脉注射氢化可的松50~75 mg,术后次日改为增加静脉注射氢化可的松20 mg,每8小时1次,术后第3天恢复原口服维持剂量即可[32]。
10 SLE 患者哺乳注意事项
哺乳对母婴的益处已众所周知,指南推荐SLE患者本人有意愿且无禁忌证时,鼓励哺乳。但SLE患者产后1年内疾病复发的风险明显升高,因此建议产后继续应用分娩前的治疗药物,以减少产后疾病复发风险。
一般来说,妊娠期间可安全使用的药物也可以在哺乳期使用(表2)。口服小剂量糖皮质激素不会对婴儿造成不良影响,建议口服泼尼松<20 mg/d(或同等剂量糖皮质激素)者正常母乳喂养;如口服泼尼松≥20 mg/d(或同等剂量糖皮质激素)时,母乳中可能会检测到极少量糖皮质激素存在,为减少婴儿糖皮质激素暴露的风险,建议将服药4 h内的乳汁弃去,服药4 h后再行哺乳。
服用羟氯喹、硫唑嘌呤、环孢素A和他克莫司的产妇可以哺乳,必要时监测血药浓度。但环磷酰胺、吗替麦考酚酯、来氟米特、甲氨蝶呤对婴儿发育可能产生影响,且缺乏相关安全性研究数据,建议哺乳期禁用。利妥昔单抗、贝利尤单抗等生物制剂的相关研究数据有限,哺乳期应尽量避免应用。
11 新生儿狼疮综合征的识别与治疗
新生儿狼疮综合征(NLS)是一种少见的被动获得性自身免疫病,发生在血清抗SSA抗体、抗SSB抗体或抗U1核糖核蛋白抗体阳性的SLE女性所生的后代,可引起皮肤损害、心脏损害、肝胆系统受损和血细胞减少等。
绝大多数患儿病变较轻且具有自限性,随着患儿年龄增大,来自母体的自身抗体逐渐被清除,除心脏传导阻滞外的其他症状及体征可逐渐消失,无需治疗。
据文献报道,出生后9个月仅10%的NLS患儿仍存在抗SSA抗体。皮肤、肝胆、血液和神经系统受累者,多数患儿在6~8个月内症状可自行好转,无需进一步治疗,其并发症不常见。对于发生心脏异常的婴幼儿,建议转入儿童心脏病专科医院及时诊治;对于发生Ⅲ度CHB的患儿,绝大多数需植入永久性心脏起搏器;对于发生皮肤病变的患儿,可使用防晒霜,避免暴露于紫外线。
当患儿肝胆系统受损严重或持续时,可予糖皮质激素1~2 mg/(kg·d),5 d后逐渐减量;当患儿出现贫血或血小板减少且伴有症状时,可输注血制品予以纠正;当患儿出现难治性贫血或血小板减少时,可予糖皮质激素1~2 mg/(kg·d),持续用药5 d,或IVIG 1 g/(kg·d),持续用药1~2 d。
12 产后监测
由于SLE患者产后疾病复发风险明显升高,产后6周即有疾病复发风险,而产后6个月和12个月的疾病活动度更高,因此指南建议在产后6~12个月内密切随访和控制疾病活动度[33]。
分娩前服用糖皮质激素、羟氯喹、硫唑嘌呤、钙调磷酸酶抑制剂的患者,分娩后应继续用药,并根据SLE病情酌情调整用药,以防止或减少疾病复发。对于分娩时病情稳定的患者,指南推荐产后维持原治疗方案,产后4~6周随访,行SLE病情评估后酌情调整治疗方案,并密切随诊至产后6~12个月。
由于SLE患者产后血液处于高凝状态,其产褥期为发生静脉血栓栓塞事件的高风险期,应根据患者APLs情况、血栓风险、既往血栓史和分娩方式等进行全面评估,根据患者发生血栓栓塞事件的风险制订治疗策略。因此,指南建议APLs阳性者应在产后12~24 h重新启动抗凝治疗,预防性抗凝治疗持续至产后4~6周;既往有血栓病史者恢复原长期抗凝治疗方案。
13 新生儿疫苗接种计划
SLE 患者所生新生儿的免疫系统可能受母亲所接受的免疫抑制剂、生物制剂及母体所携带的自身抗体影响,使其免疫系统处于一定程度的抑制状态,其能否如期接种疫苗实现人工主动免疫是非常重要的临床问题。
本指南参照“国际新生儿疫苗接种指南”和“我国特殊健康状态儿童预防接种专家共识”相关内容[34],建议SLE患者所生新生儿在无合并先天性免疫缺陷且无疫苗成分过敏等禁忌证时,考虑常规接种灭活疫苗,无需延迟;建议孕中晚期、哺乳期接受生物制剂治疗的SLE患者所生新生儿,应在出生后至少6个月内避免接种减毒活疫苗,包括口服轮状病毒疫苗、脊髓灰质炎疫苗、麻风腮三联疫苗、卡介苗等,以免发生播散性感染。
14 小结
综上,《2022中国系统性红斑狼疮患者生殖与妊娠管理指南》对SLE患者妊娠所有阶段的相关事项均给出了详实的指导意见和推荐建议,涉及内容广泛,密切结合临床实际,可操作性强,适合我国国情,必将对规范我国SLE患者围妊娠期管理发挥重要指导作用。
参考文献
[1]Clowse ME,Jamison M,Myers E,et al. A national study of the complications of lupus in pregnancy[J]. Am J Obstet Gynecol,2008,199: 127.e1-e6.
[2]Wu J,Ma J,Bao C,et al. Pregnancy outcomes among Chinese women with and without systemic lupus erythematosus: a retrospective cohort study[J]. BMJ Open,2018,8:e020909.
[3]国家皮肤与免疫疾病临床医学研究中心, 国家妇产疾病临床医学研究中心, 中国风湿免疫病相关生殖及妊娠研究委员会, 等.2022中国系统性红斑狼疮患者生殖与妊娠管理指南[J].中华内科杂志, 2022, 61:1184-1205.
[4]Winter RW,Larsen MD,Magnussen B,et al. Birth outcomes after preconception paternal exposure to methotrexate: a nationwide cohort study[J].Reprod Toxicol,2017,74: 219-223.
[5]Wallenius M,Lie E,Daltveit AK,et al. No excess risks in offspring with paternal preconception exposure to disease-modifying antirheumatic drugs. Arthritis Rheumatol[J].Arthritis Rheumatol,2015,67:296-301.
[6]张文,李懿莎,刘冬舟,等. 风湿性疾病患者围妊娠期药物使用规范[J]. 中华内科杂志,2021,60: 946-953.
[7]Jones DC,Hayslett JP. Outcome of pregnancy in women with moderate or severe renal insufficiency[J]. N Engl J Med,1996,335: 226-232.
[8]King TE. Restrictive lung disease in pregnancy[J]. Clin Chest Med,1992,13: 607-622.
[9]Park-Wyllie L,Mazzotta P,Pastuszak A,et al. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies[J].Teratology,2000,62: 385-392.
[10]Carmichael SL,Shaw GM,Ma C,et al. Maternal corticosteroid use and orofacial clefts. Am J Obstet Gynecol,2007,197:585.e1-e7.
[11]Diav-Citrin O,Blyakhman S,Shechtman S,et al. Pregn-ancy outcome following in utero exposure to hydroxychloroquine: a prospective comparative observational study[J]. Reprod Toxicol,2013,39:58-62.
[12]郝冬林,徐东,刘晶,等,羟氯喹对系统性红斑狼疮妊娠患者疗效及安全性的前瞻性研究[J].中华医学杂志,2014,94:981-982.
[13]Eudy AM,Siega-Riz AM,Engel SM,et al.Effect of pregnancy on disease flares in patients with systemic lupus erythematosus[J].Ann Rheum Dis,2018,77:855-860.
[14]Klinger G,Morad Y,Westall CA,et al. Ocular toxicity and antenatal exposure to chloroquine or hydroxychloroquine for rheumatic diseases[J].Lancet,2001,358:813-814.
[15]Osadchy A,Ratnapalan T,Koren G. Ocular toxicity in children exposed in utero to antimalarial drugs: review of the literature[J]. J Rheumatol,2011,38: 2504-2508.
[16]Murthy RK,Theriault RL,Barnett CM,et al. Outcomes of children exposed in utero to chemotherapy for breast cancer[J]. Breast Cancer Res,2014,16:500.
[17]Carvalheiras G,Vita P,Marta S,et al. Pregnancy and systemic lupus erythematosus: review of clinical features and outcome of 51 pregnancies at a single institution[J].Clin Rev Allergy Immunol,2010,38:302-306.
[18]Petri M,Howard D,Repke J. Frequency of lupus flare in pregnancy. The Hopkins Lupus Pregnancy Center experience[J].Arthritis Rheum,1991,34:1538-1545.
[19]Porta S,Danza A,Arias Saavedra M,et al.Glucocorticoids in systemic lupus erythematosus. Ten questions and some issues[J].J Clin Med,2020,9: 2709.
[20]Imbasciati E,Tincani A,Gregorini G,et al. Pregnancy in women with pre-existing lupus nephritis: predictors of fetal and maternal outcome[J]. Nephrol Dial Transplant,2009,24:519-525.
[21]Li M,Tian Z,Qian J,et al. Impact of pregnancy in patients with systemic lupus erythematosus-associated pulmonary arterial hypertension: case series and literature review[J].Lupus Sci Med,2022,9:1-9.
[22]Brito-Zerón P, Izmirly PM, Ramos-Casals M,et al. The clinical spectrum of autoimmune congenital heart block[J]. Nat Rev Rheumatol,2015,11: 301-312.
[23]Vanoni F,Lava SAG,Fossali EF,et al. Neonatal systemic lupus erythematosus syndrome: a comprehensive review[J].Clin Rev Allergy Immunol,2017,53:469-476.
[24]Johnson MJ,Petri M,Witter FR,et al. Evaluation of preterm delivery in a systemic lupus erythematosus pregnancy clinic[J].Obstet Gynecol,1995,86:396-399.
[25]Smyth A,Oliveira GH,Lahr BD,et al. A systematic review and meta-analysis of pregnancy outcomes in patients with systemic lupus erythematosus and lupus nephritis[J].Clin J Am Soc Nephrol,2010,5:2060-2068.
[26]Bundhun PK,Soogund MZ,Huang F.Impact of systemic lupus erythematosus on maternal and fetal outcomes following pregnancy: A meta-analysis of studies published between years 2001—2016[J]. J Autoimmun,2017,79:17-27.
[27]Ramenghi LA,Martinelli A,De Carli A,et al.Cerebral maturation in IUGR and appropriate for gestational agepreterm babies[J].Reprod Sci,2011,18:469-475.
[28]Askie LM, Duley L, Henderson-Smart DJ,et al. Antiplate-let agents for prevention of pre-eclampsia: a meta-analysis of individual patient data[J].Lancet,2007,369:1791-1798.
[29]Han Y,Lee JH,Chang JH,et al.Clinical features and outcomes in patients with pulmonary complications during pregnancy and peripartum[J].J Matern Fetal Neonatal Med,2020,33:1191-1196.
[30]Committee on Obstetric Practice.Committee Opinion No. 713: Antenatal Corticosteroid Therapy for Fetal Maturation[J].Obstet Gynecol,2017,130: e102-e109.
[31]Danowski TS,Bonessi JV,Sabeh G,et al. Probabilities of pituitary-adrenal responsiveness after steroid therapy[J].Ann Intern Med,1964,61:11-26.
[32]Akkara Veetil BM,Bongartz T. Perioperative care for patients with rheumatic diseases[J].Nat Rev Rheumatol,2011,8:32-41.
[33]Götestam Skorpen C, Lydersen S, Gilboe IM,et al. Disease activity during pregnancy and the first year postpartum in women with systemic lupus erythematosus[J]. Arthritis Care Res (Hoboken),2017,69: 1201-1208.
[34]上海市疾病预防控制中心,杭州市疾病预防控制中心,苏州市疾病预防控制中心,等.特殊健康状态儿童预防接种 专家共识之十五:自身免疫性疾病与预防接种[J].中国实用儿科杂志,2019,34:180-181.


