【Blood Cancer Discov】BCMA CART后MRD评估的纵向预后价值
时间:2023-08-15 17:36:19 热度:37.1℃ 作者:网络
MRD评估的价值
CAR T细胞的开发改变了三重暴露的复发/难治性MM(RRMM)患者的结局,但由于其新颖性,以及CAR T治疗(即单次输注)独特的作用方式和给药方案,对初始缓解、疾病复发和进展过程中肿瘤负荷动力学的了解仍有限。
缓解深度(包括MRD)是新诊断和RRMM的关键预后因素,但关于其在CAR T细胞治疗的患者中的临床意义数据仍很少。此外,在RRMM患者中研究BCMA CAR T细胞idecabtagene vicleucel(ide-cel)的I期CRB-401研究中发现,与MRD阴性相比血清学缓解通常有所延迟。从而提出了一个重要问题,那就是在评估CAR T治疗RRMM的疗效时,使用不同缓解标准的最佳时间点存在不确定性。
基于此,学者分析了II期KarMMa研究中,ide-cel治疗后血清学和MRD缓解深度的纵向预后价值。近日发表于《Blood Cancer Discovery》。

研究结果
二代MRD方法的一致性和预后价值
在分析ide-cel输注后血清学和MRD缓解深度的纵向预后价值之前,作者先比较了二代流式细胞术(NGF)和二代测序(NGS)的结果,因为在RRMM中CAR T治疗后使用这些方法获得的MRD数据很少。在ide-cel输注后第一年内的第1、3、6和12个月,使用NGF和NGS分别对骨髓(BM)进行了总计336和257次MRD评估。
ide-cel后第1、3、6和12个月分析的BM穿刺样本中,NGF和NGS之间的MRD状态一致的比例分别为67%、75%、81.5%和73%。大多数不一致是由于BM穿刺被NGF分类为血液稀释,而NGS分类为MRD阴性(使用流式细胞术可同时评估MRD和血液稀释,以避免可能的假阴性MRD;出处为Potential future direction of measurable residual disease evaluation in multiple myeloma.Blood . 2023 Jul);血液稀释&NGS-的情况在ide-cel输注后立即达到峰值,并持续至输注后1年(第1、3、6和12个月分别为25%、13%、9.3%和9.8%)。因此,排除血液稀释样本的亚组分析显示NGF和NGS之间的一致性较高(ide-cel后1、3、6和12个月时分别为94%、88%、90%和83%)。
基于预后,NGF和NGS在所有时间点对无进展生存期(PFS)均显示出相似的预测价值。无论采用何种方法, MRD-均与每个标志的进展和/或死亡风险显著降低相关,风险比(HR)介于0.05-0.265。根据NGF(图1A,n=17)或NGS(图1B,n=19),第12个月时持续MRD-的患者未达到中位PFS,而持续性MRD患者在里程碑时间后不久进展。里程碑定义为该时间点之前从未MRD阳性。
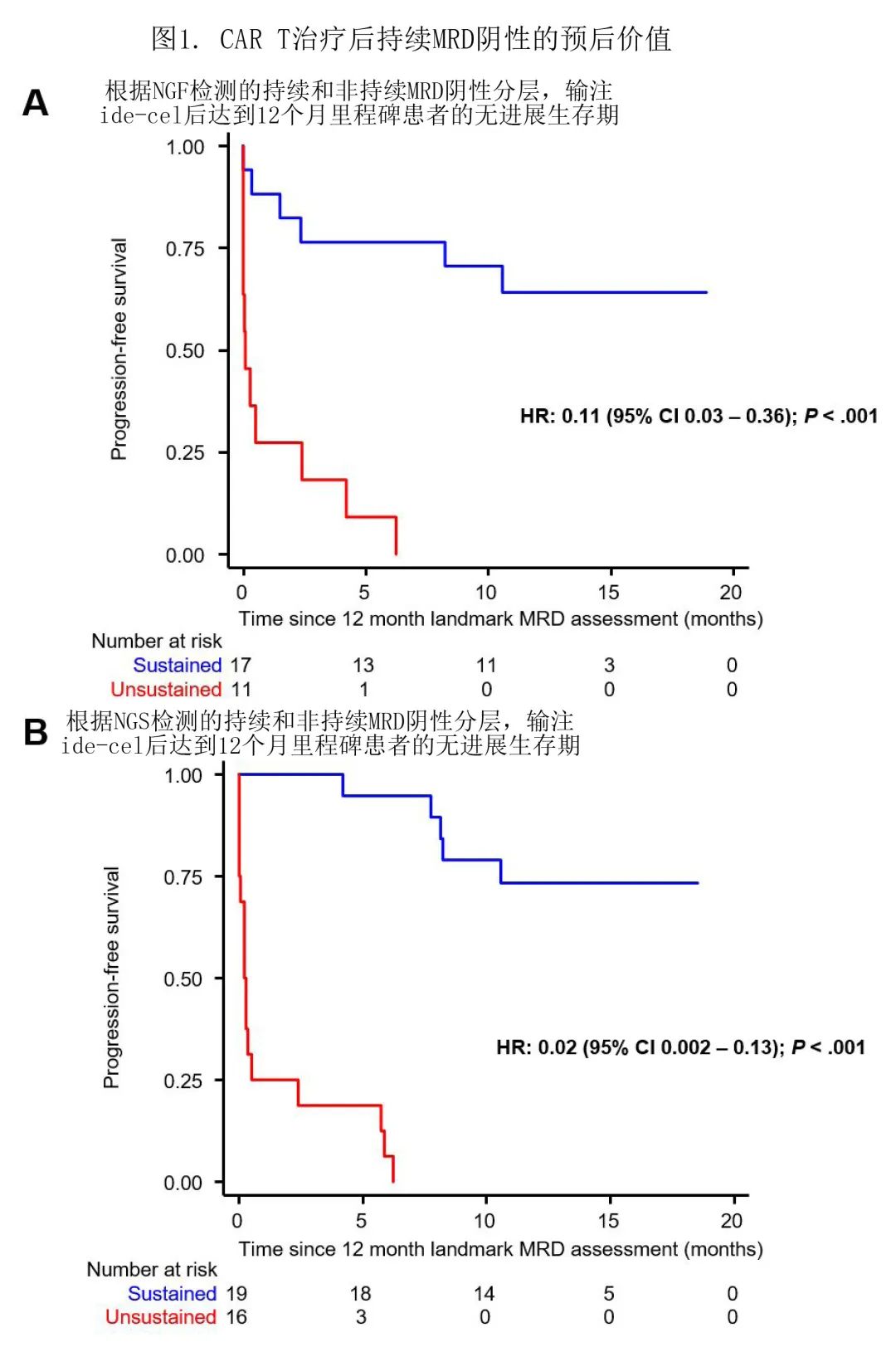
不同血清学和MRD反应动力学的临床意义
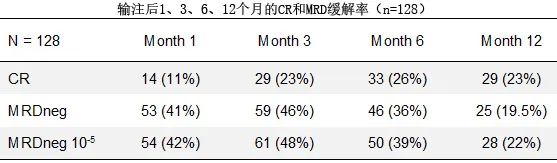
证实NGF和NGS的一致性后对NGF数据集进行了分析,以研究ide-cel输注后血清学和MRD反应深度的纵向预后价值,因为如上所述,NGF检测了更多的样本,且血液稀释监测是该方法的固有要求。ide-cel后1、3、6和12个月时,治疗患者人群(N=128)中MRD阴性率(<1x 10-6)分别为41%、46%、36%和19.5%。10-5时的相应比率(即如果可检测水平<1x10-5,则为MRD阴性)分别为42%、48%、39%和22%。值得注意的是,在10-5被视为MRD阴性的10例患者样本中检测到10-6对数范围内的持续MRD,所有患者此后均不久进展(中位3.6个月)。
值得注意的是,除第12个月外,治疗患者人群在ide-cel后第1、3、6和12个月的CR率(11%、23%、26%和23%)均低于相应时间点的MRD-率。这些结果是由于该本研究中MRD阴性的定义不受是否达到CR的影响。
因此,该结果表明,BM肿瘤细胞的清除早于M蛋白,可能是由于一些免疫球蛋白的半衰期较长。或者,某些患者在达到一过性MRD阴性状态后疾病进展,但从未达到CR;事实上,在ide-cel输注后1个月时MRD-的53例患者中,有25例观察到这种情况(图2)。

CR率和MRD率的不一致模式,进一步增加了研究ide-cel输注后不同血清学和MRD反应动力学的临床意义的兴趣。ide-cel输注后1个月的里程碑PFS,在1个月时<CR患者(n=103)与CR患者(n=14)之间无显著差异(中位8 vs 11个月,P=0.09);相比之下,与MRD-伴CR或<CR的患者相比,第1个月时MRD+预示着里程碑PFS较差(图3A)。在ide-cel后3、6和12个月,CR且MRD-患者的中位里程碑PFS显著长于<CR且MRD-患者(图3B-D);达到CR/MRD- vs <CR/MRD- vs CR/MRD+ vs <CR/MRD+ vs <CR/MRD+的患者第6个月和第12个月的中位标志性PFS逐渐降低(图3C-D)
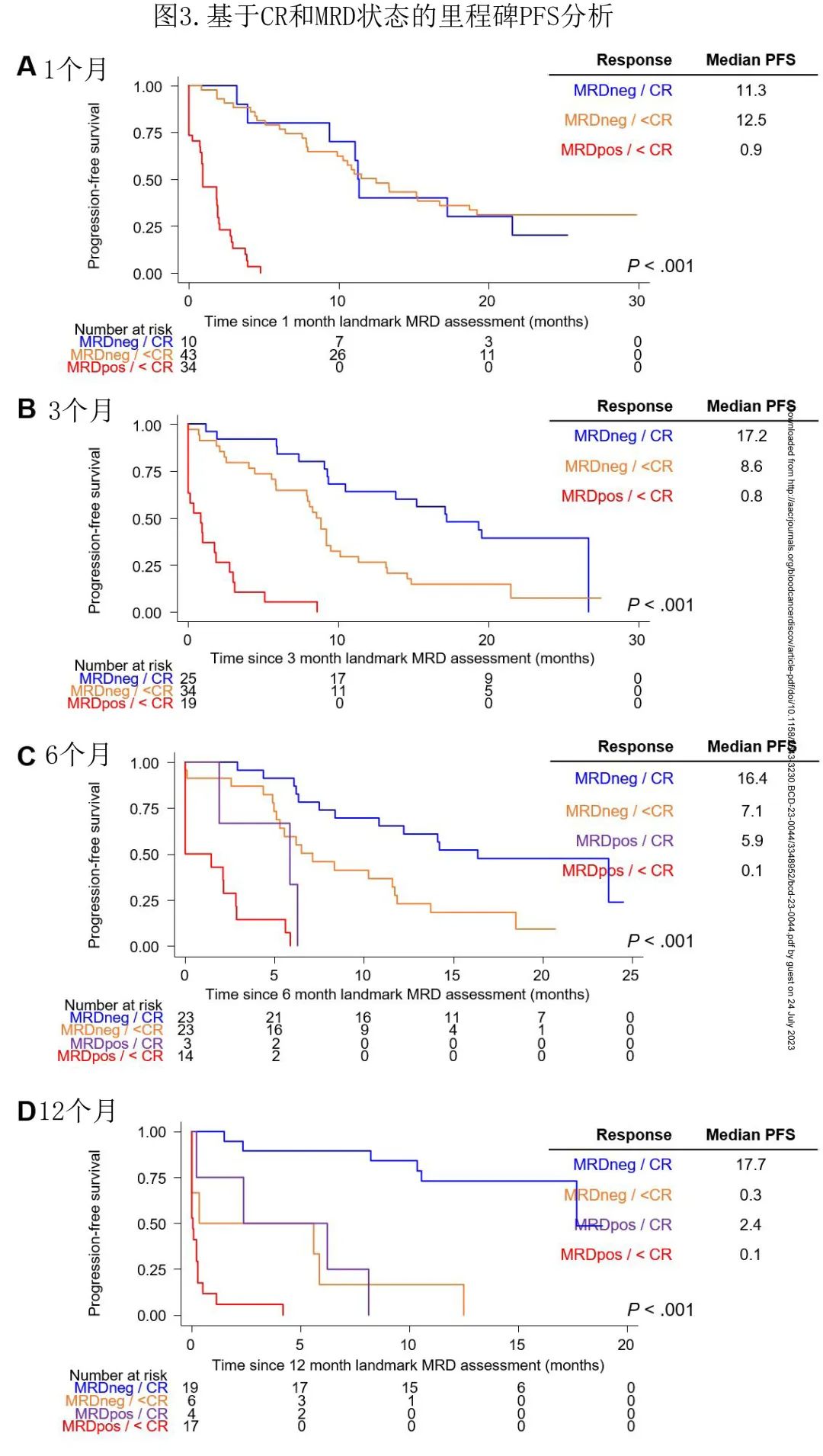
再次出现正常浆细胞(PC)预示进展风险更高
作者假设,正常浆细胞的再现可以作为CAR T细胞持久性和/或功能丧失的替代标志物,因为靶向BCMA的免疫治疗无法区分肿瘤和正常PC。在这种情况下,该信息有助于识别哪些MRD-患者由于CAR T监测丧失而进展风险较高。有趣的是,在所有时间点均观察到正常PC再次出现,且通常发生于MRD转阳和疾病进展之前(图4A)。
因此,在第1、3和12个月时再次出现正常PC与PFS较差相关。尽管患者数量减少无法得出明确结论,但在第1个月时MRD-且再次出现正常PC的患者PFS较差且与MRD阳性患者相似(图4B)。在12个月时再次出现正常PC的所有患者均可检测到ide-cel水平,通过每微克基因组DNA的载体转基因拷贝的定量PCR测定(中位数355),这表明已经功能丧失而非持续。到目前为止,3例患者显示无正常PC和第12个月时MRD-,目前均未进展(图4C)。
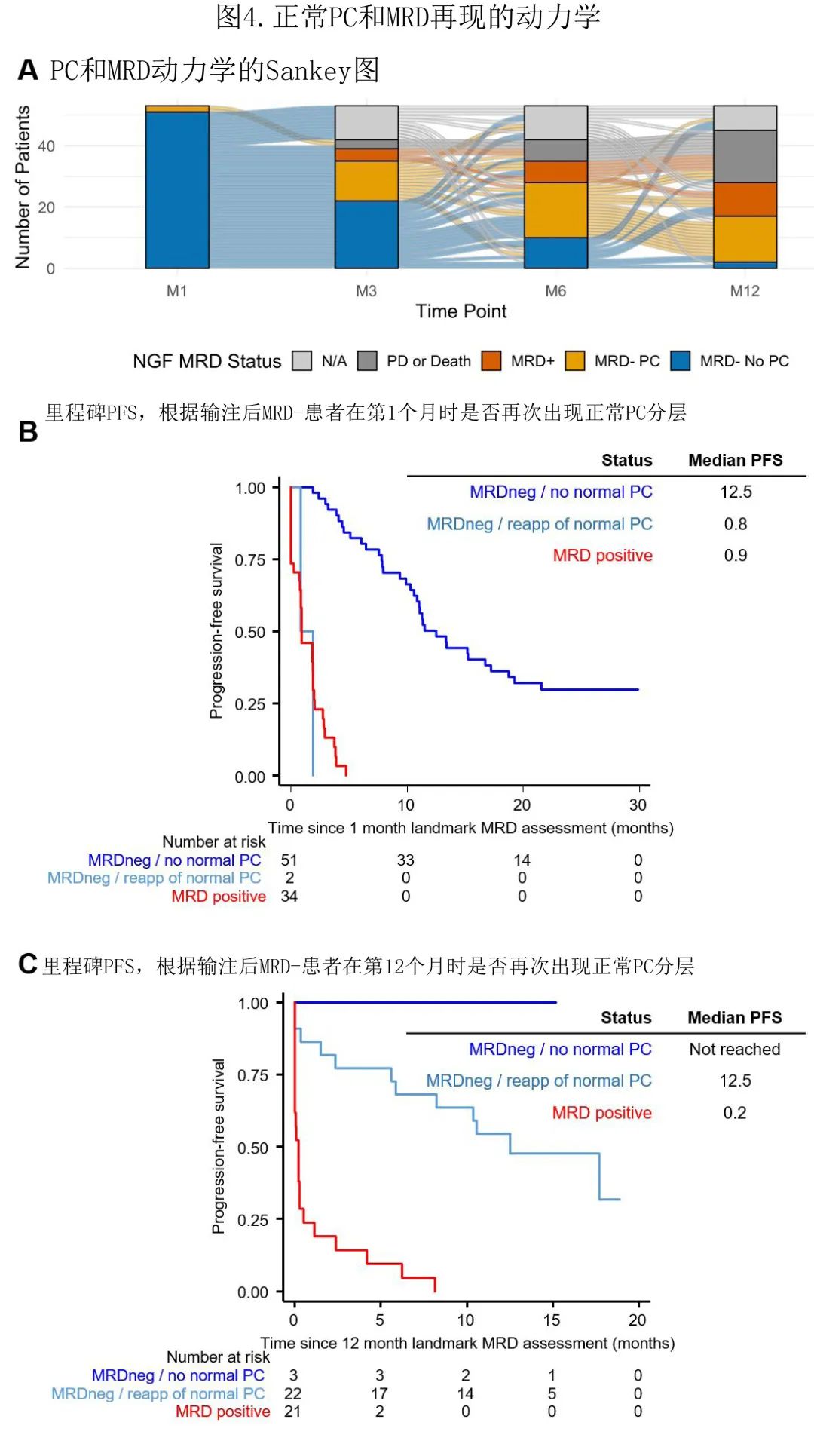
总结
MRD在CAR T细胞治疗多发性骨髓瘤患者中的作用尚不确定。作者分析了入组KarMMa研究的125例RRMM患者输注ide-cel后第一年的MRD动力学。在ide-cel后第1个月时,<CR患者与CR患者的PFS无差异,仅MRD状态可预测该里程碑时间点显著不同的PFS。在3个月及以后的MRD-患者中,达到CR的患者的PFS长于<CR的患者。在10-6对数范围内持续MRD+和MRD阴性患者再现正常浆细胞与PFS较差相关,这也是首次证实,BCMA CAR T治疗后再次出现正常PC可预测MRD-患者的PFS较差。
该研究揭示了ide-cel后血清学和MRD反应动力学的不同预后意义,并提示研究正常浆细胞的再次出现作为CAR T细胞功能丧失的替代指标的潜在价值。
参考文献
Paiva B,et al. Time-dependent prognostic value of serological and measurable residual disease assessments after idecabtagene vicleucel.Blood Cancer Discov . 2023 Jul 24;BCD-23-0044. doi: 10.1158/2643-3230.BCD-23-0044.


