AJH:奥布替尼治疗复发/难治性边缘区淋巴瘤的2期研究结果
时间:2023-09-03 17:10:23 热度:37.1℃ 作者:网络
奥布替尼
2023年4月21日,新型BTK抑制剂奥布替尼获得中国国家药品监督管理局批准,用于治疗复发/难治性边缘区淋巴瘤(MZL)患者,奥布替尼由此成为中国首个获批针对复发/难治性边缘区淋巴瘤适应症的BTK抑制剂,也是其在中国获批的第三个适应症。
新适应症本次获批是基于一项评价奥布替尼治疗复发/难治性边缘区淋巴瘤安全性和有效性的多中心、开放标签II期ICP-CL-00104研究数据。《American Journal of Hematology》近日发表了该研究的结果。

研究方法&结果
该多中心、开放标签、II期研究有中国32家研究中心参与,纳入R/R经中心组织病理学审查证实诊断为 MZL 且有治疗开始指征的≥18岁且≤75岁患者,既往接受过≥1线且≤4线治疗,包括至少1种抗 CD20 单克隆抗体 (mAb) 治疗,且复发或未能达到缓解。奥布替尼口服给药,每日一次 (QD),剂量为150mg,28天为一个周期,直至疾病进展、出现不可耐受的毒性、死亡或撤回知情同意。
研究的主要终点为独立审查委员会 (IRC)评估的客观缓解率(ORR,根据2014 Lugano标准),次要终点包括研究者评估的ORR、无进展生存期(PFS)、缓解维持时间(DOR)、至缓解时间(TTR)、至进展时间(TTP)和总生存期(OS)。
患者和治疗
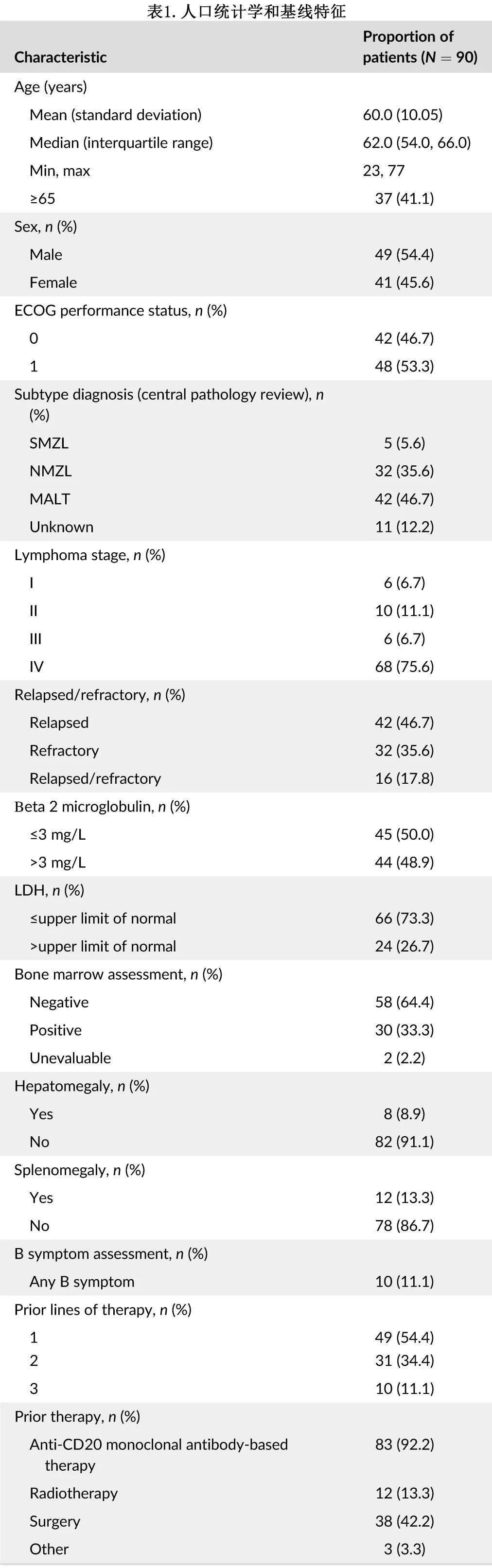
共入组111例患者(意向治疗集),其中90例患者纳入修正的全分析集(mFAS,定义为接受至少一剂奥布替尼且经中心病理学审查证实为 MZL 的所有入组患者),21例患者经中心病理学审查为非MZL。90例患者的中位年龄为62岁,41.1%为≥65岁。约半数患者 (54.4%) 为男性,基线 ECOG 状态均为0-1。MZL亚型包括脾脏MZL(SMZL,5例患者,5.6%)、淋巴结(NMZL,32例患者,35.6%)、粘膜相关淋巴组织(MALT,42例患者,46.7%)和未知(11例患者,12.2%)。基线时90例患者中的74例 (82.2%) 为III 期或 IV 期晚期疾病。30例患者 (33.3%) 存在骨髓受累。既往治疗的中位次数为1。90例患者中83例既往接受过基于抗 CD20 单抗的治疗方案(表1)。
疗效
90例患者可接受疗效评估,IRC 评估的 ORR 为58.9%,10例患者 (11.1%) 达到CR,43例患者 (47.8%) 达到PR;研究者评估的 ORR 为53.3%,包括8.9%的CR和44.4%的PR。IRC 评估的中位 TTR 为5.8个月。92.2%(83/90) 的患者肿瘤缩小。
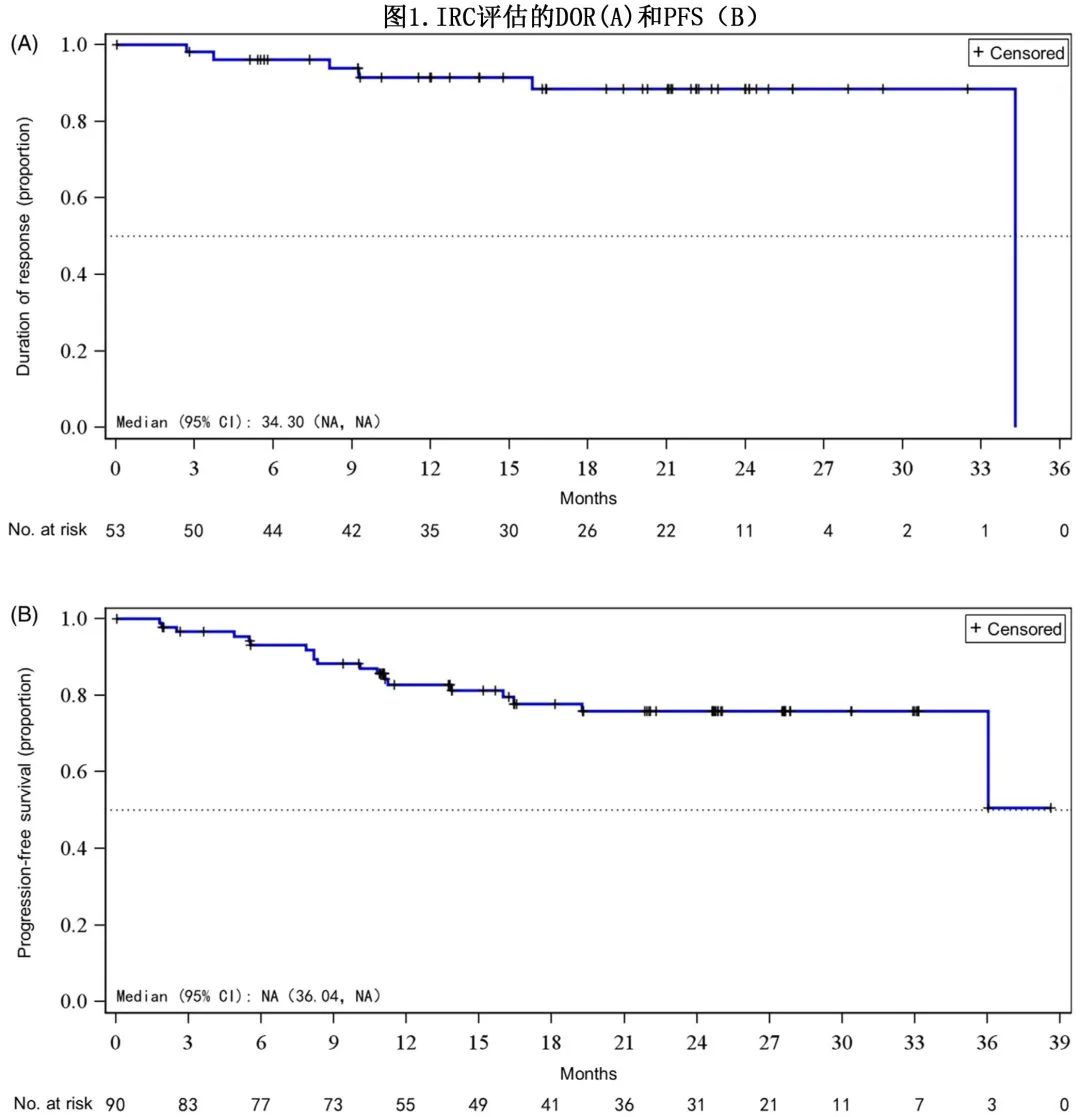
中位随访24.3个月,IRC评估的中位 DOR 为34.3个月, IRC 评估的中位PFS未达到(图1);12个月持续缓解率为91.5%,24个月时为88.5%,12个月PFS 率为82.8%,24个月时为75.8%。IRC 评估的中位TTP未达到,12个月疾病进展率为13.7%,24个月时为21.1%。中位OS未达到,12个月 OS 率为91.0%,24个月 OS 率为86.8%。
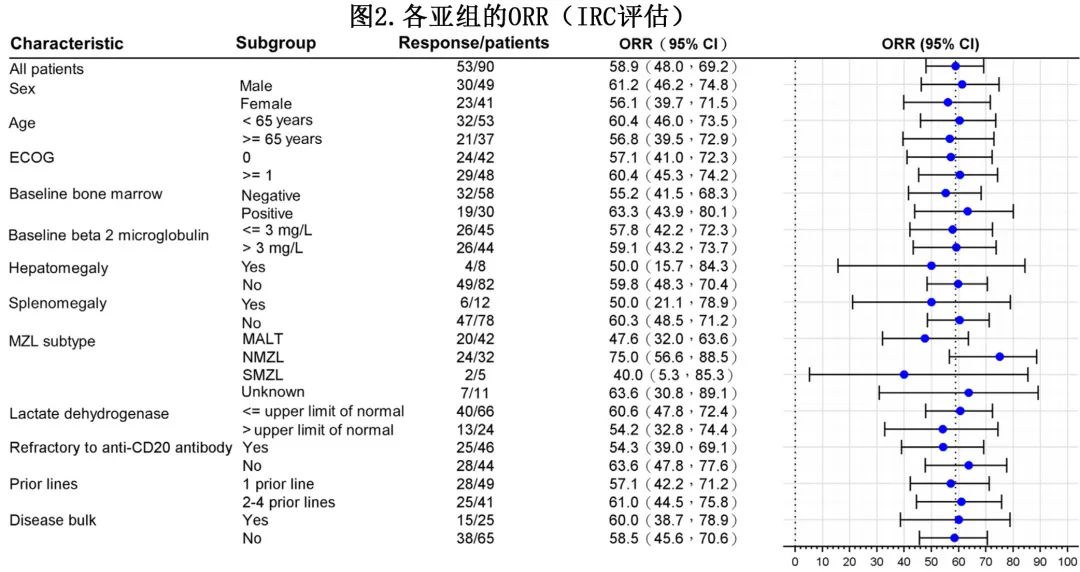
各基线特征亚组的缓解率一致。根据MZL亚型,IRC评估的NMZL、MALT和SMZL的ORR分别为75.0%、47.6%和40.0%。IRC评估的NMZL的中位DOR为34.3个月,其他疾病亚型未达到。NMZL、SMZL和MALT的中位PFS(IRC评估)分别为36.0个月、16.4个月和未达到。所有亚型均未达到中位OS。NMZL、MALT和SMZL的12个月持续缓解率分别为86.8%、93.8%和100%,12个月 PFS 率分别为87.1%、78.6%和75.0%,12个月OS率分别为90.0%、94.6%和75.0%。在按性别、年龄组、ECOG体能状态、抗CD20单抗难治性、既往治疗线数和肿瘤负荷指标(包括β2微球蛋白和IDH、大包块疾病、骨髓受累、基线时存在肝肿大或脾肿大)分层的其他亚组中ORR没有显著差异(图2)。
安全性
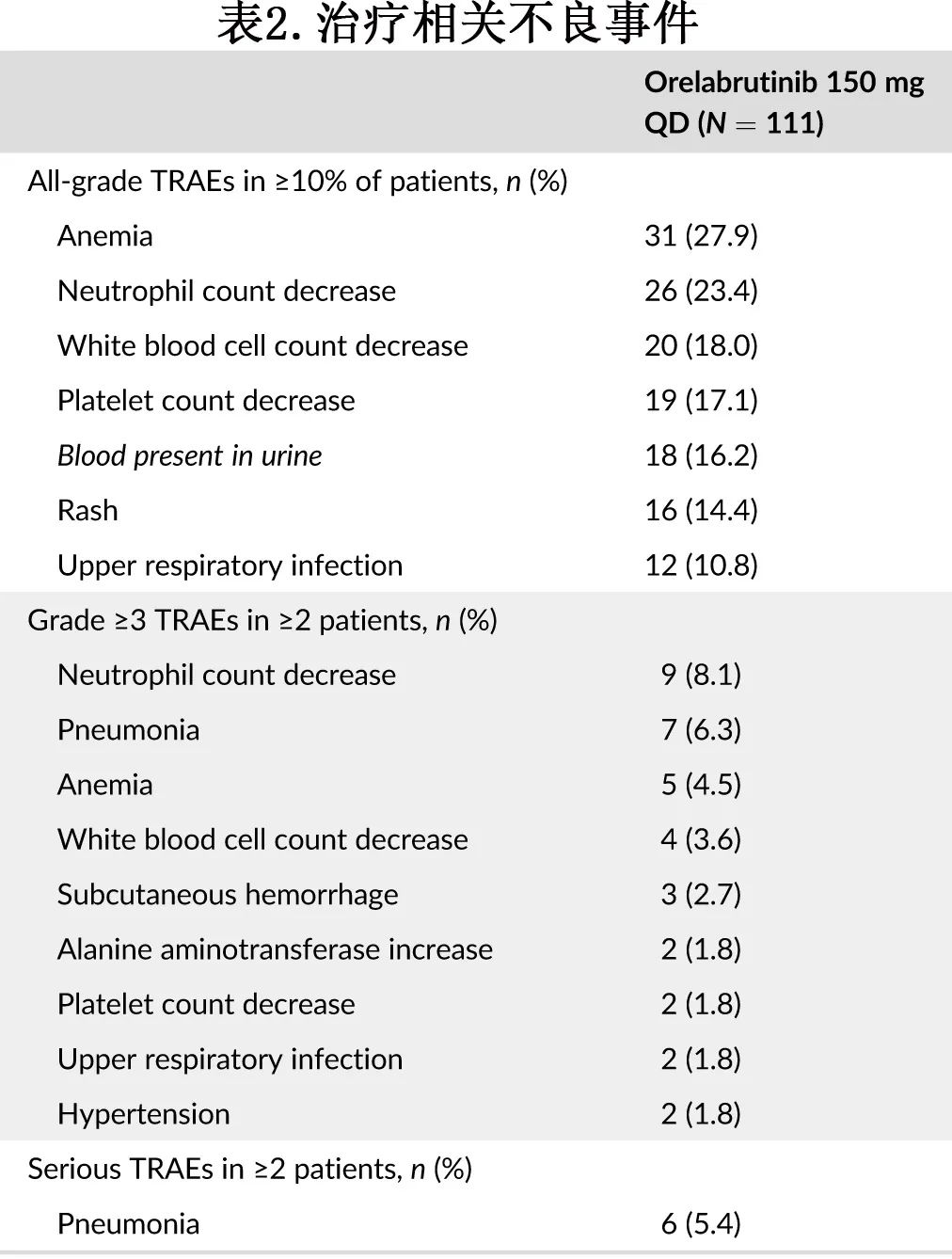
评价了所有111例患者中奥布替尼的安全性特征。109例患者 (98.2%) 发生AE,90.1%患者发生至少1起治疗相关AE(TRAE)。最常见的任何级别 TRAE 包括贫血 (27.9%)、中性粒细胞计数降低 (23.4%)、白细胞计数降低 (18.0%)、血小板计数降低 (17.1%)、尿血 (16.2%)、皮疹 (14.4%) 和上呼吸道感染 (10.8%)。34例 (30.6%) 患者报告≥3级TRAE,其中中性粒细胞计数降低 (8.1%)、感染性肺炎 (6.3%)、贫血 (4.5%) 和白细胞计数降低 (3.6%)最常见(≥2例患者中)。18例患者 (16.2%) 发生了奥布替尼相关SAE,至少2例患者报告的严重 TRAE 为肺炎(5.4%)(表2)。
7例(6.3%)患者因 TRAE 停用奥布替尼,感染 (n=4) 是最常见原因。10例患者因 TRAE 需要降低剂量,最常见原因为皮下出血 (n=4) 和感染性肺炎 (n=2)。
研究期间报告了14例死亡:5例死于证实的疾病进展,5例死于AE,4例不明。
32例患者 (28.8%) 发生治疗相关感染,13例患者 (11.7%) 为≥3级治疗相关感染,11起治疗相关感染事件符合严重标准。1例第二原发恶性肿瘤(胃腺癌)与治疗相关。3例高血压事件与治疗相关,其中2例事件≥3级。23.4%的患者发生治疗相关中性粒细胞减少,8.1%发生≥3级中性粒细胞减少。发生1起2级治疗相关房颤、1起1级房扑事件,与奥布替尼相关。
总结
在这项 II 期、多中心、开放标签研究中,奥布替尼在R/R MZL 患者中产生了稳健的缓解,耐受性良好,且在基线时具有不同 MZL 亚型和负面预后因素的患者中均获得一致高缓解率。本研究结果支持奥布替尼作为R/R MZL 患者有效且可耐受的口服治疗选择。
参考文献
Deng L, et al.Orelabrutinib for the treatment of relapsed or refractory marginal zone lymphoma: A phase 2, multicenter, open-label study.Am J Hematol . 2023 Aug 30. doi: 10.1002/ajh.27064.


