Lancet Neurol:评估婴儿癫痫快速基因组测序的可行性、诊断产量和临床效用
时间:2023-11-26 11:32:14 热度:37.1℃ 作者:网络
婴儿发作的癫痫的严重程度从自限性癫痫到更大的发育性和癫痫性脑病。婴儿发病的发病率为1200分之一。发育和癫痫性脑病患者具有耐药性癫痫发作、严重的发育障碍和高死亡风险,对家庭具有重要的心理社会影响,并对卫生系统造成重大经济成本。
婴儿发作的癫痫通常具有遗传病因(涉及>800个基因)。包括系统回顾在内的许多研究4显示,在早期发病癫癫中基因面板和外组测序具有很高的诊断产量和成本效益,基因测试现在被认为是一线调查。基因组测序进一步提高了诊断产量,但尚未在未选定的婴儿癫痫队列中进行研究。在罕见疾病中,基因组测序,特别是三重基因组测序,已经证明了可观的诊断产量。
对于患有癫痫的婴儿,确定准确的诊断可以指导临床管理,并为有关癫痫控制、发育结果和潜在合并症的预后提供信息。越来越多的遗传癫痫具有精确治疗意义,包括四个常见的婴儿癫痫基因(KCNQ2、PRRT2、SCN1A、SLC2A1)。
尽管目前大多数癫癫痫患者无法获得遗传疗法,但定制抗癫药物通常是可能的。此外,遗传诊断可以告知临床试验或非抗癫药物治疗(如癫痫手术)的资格,并实现精确的遗传咨询。在关于非基因组测序基因测试对癫痫的影响的几项研究中,遗传诊断影响了36-72%的病例的管理。

虽然快速基因测试和及时实施个性化治疗(如果有的话)可能会改善结果,但一个主要挑战是,测试通常需要数月到数年时间,婴儿因不受控制的癫痫发作或潜在疾病而患有渐进的神经鼻痫。在新生儿重症监护室(NICU)和儿科重症监护病房(PICU)进行的研究表明,在一系列条件下快速(即周)和超快(即天)基因组测序具有高诊断率,具有临床效用和医疗保健成本的降低。
迄今为止,快速基因组测序主要在ICU进行,以及及时遗传诊断对婴儿的影响癫痫尚未确定。因此,2023年10月17日发表在Lancet Neurol的研究,旨在证明快速基因组测序的可行性,并研究新发性癫痫婴儿的诊断产量和临床效用。
研究人员进行了一项国际多中心队列研究(Gene-STEPS),这是国际精准儿童健康伙伴关系(IPCHiP)的试点研究。IPCHiP是一个由四个儿科中心组成的财团,在澳大利亚、加拿大、英国和美国提供三级亚专业服务。我们从IPHiP中心招募了患有新发性癫痫或复杂发热性癫痫发作的婴儿,他们在癫痫发作时不到12个月。本文排除了有简单发热性癫痫、急性诱发性癫痫发作、已知后天性原因或已知遗传原因的婴儿。
从探亲和可用的亲生父母那里收集了血液样本。从医疗记录、治疗临床医生和父母那里收集了临床数据。当父母双方都可用时,三重基因组测序,当父母一方或父母双方都可用时,进行双重或单例基因组测序。特定地点的协议用于DNA提取和图书馆制备。在临床认可的实验室进行了快速基因组测序和分析,结果已返回给家庭。我们分析了队列人口和临床特征的汇总统计数据,以及快速基因组测序的时间、诊断产量和临床影响。
研究结果显示,2021年9月1日至2022年8月31日期间,招收了100名新发癫痫的婴儿,其中41名(41%)为女孩,59(59%)为男孩。癫痫发作的平均年龄为128天(IQR 46-192)。对于100名婴儿中的43个(43%[二项分布95%CI 33-53]),本文确定了遗传诊断,从癫痫发作到快速基因组测序结果的中位时间为37天(IQR 25-59)。
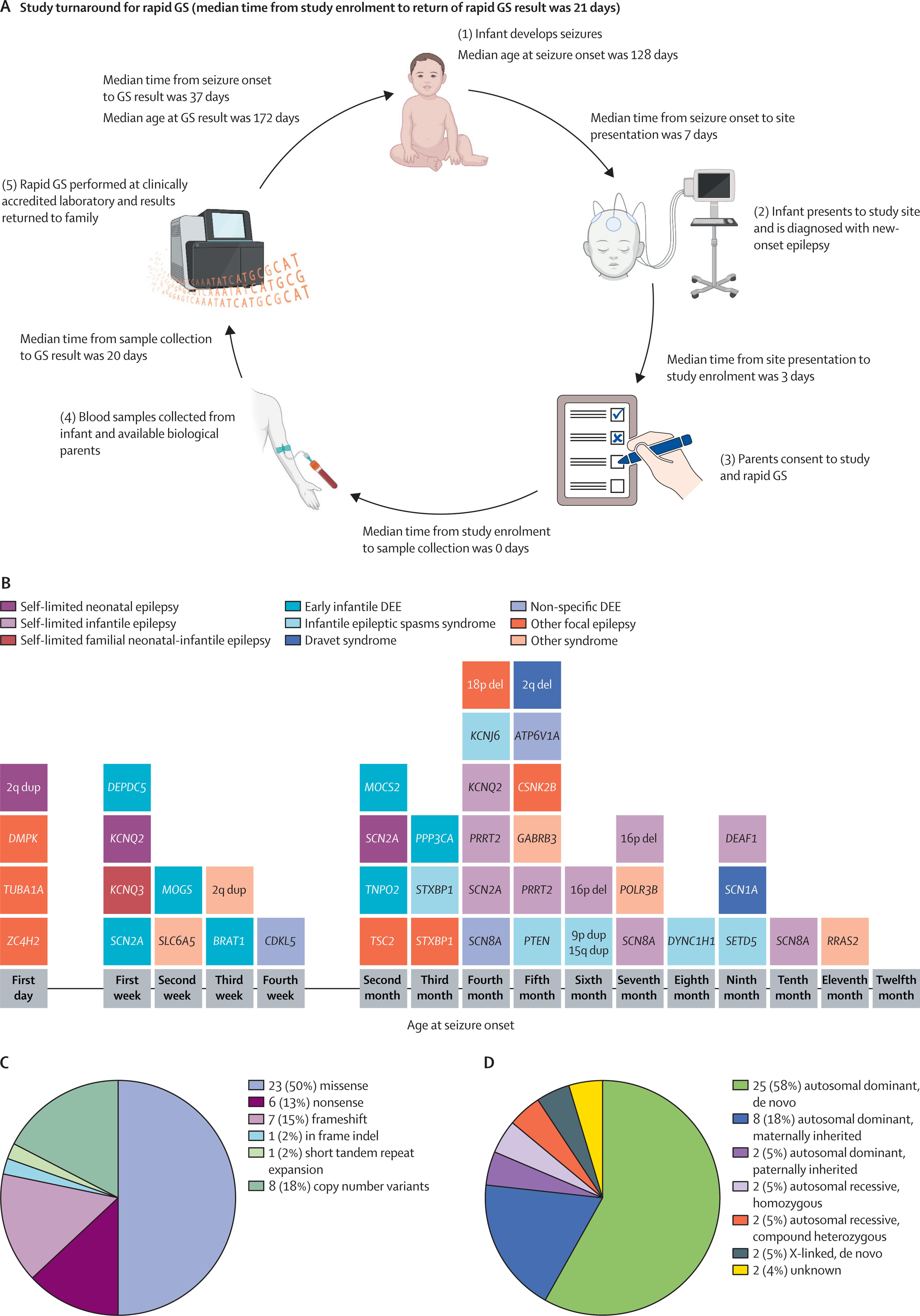
快速GS工作流程和遗传诊断摘要
遗传诊断与新生儿癫痫发作与婴儿癫痫发作(19例中的14 [74%]对81例中的29 [36%];p=0.0027),转诊设置(12 [71%],43名非重症监护住院病人中的19 [44%],40名门诊病人中的12 [30%];p=0.0178);以及癫癫综合征(15名自闭症患者(15 [87%],发育和癫癫痫病51例中的18 [35%],其他综合征的12 [35%];p=0.001)。
快速基因组测序揭示了遗传异质性,涉及34个独特的基因或基因组区域。遗传诊断具有立竿见影的临床效用,为治疗提供信息(43个中的24[56%])、额外的评估(28[65%])、预后(37[86%])和复发风险咨询(所有病例)。
综上所述,这项国际多中心基因-STEPS研究是首次主要在重症监护环境之外和疾病特异性队列中进行快速基因组测试的研究。本文证明了在多个三级儿科系统中新发性癫痫患者婴儿快速基因组测序的可行性,具有高诊断率和临床效果。本文发现为促使使用最先进的快速基因组测试提供了支持,以促进早期病因诊断,从而为这一弱势群体的紧急定向管理提供信息。
原始出处
D'Gama, A. M., Mulhern, S., Sheidley, B. R., Boodhoo, F., Buts, S., Chandler, N. J., ... & McTague, A. (2023). Evaluation of the feasibility, diagnostic yield, and clinical utility of rapid genome sequencing in infantile epilepsy (Gene-STEPS): an international, multicentre, pilot cohort study. The Lancet Neurology, 22(9), 812-825.


