ASCO 2024:卡瑞利珠单抗联合阿帕替尼(“双艾”组合)治疗不可手术切除的肝细胞癌,OS高达23.8个月
时间:2024-06-05 09:00:37 热度:37.1℃ 作者:网络
2024年5月31日-6月4日,在美国芝加哥召开的ASCO(美国临床肿瘤学会)年会上,由中国药科大学附属南京天印山医院的秦叔逵教授牵头开展的国际性III期临床研究——CARES-310研究公布了最终生存分析结果1,结果显示,相比于标准治疗,卡瑞利珠单抗+阿帕替尼组的中位总生存期(OS)显著延长,达到23.8个月,获得了迄今为止已公布数据的晚期肝癌一线治疗关键Ⅲ研究中的最长中位OS,显示出持续的具有临床意义的生存改善,且安全性可控。
CARES-310研究是首个证明在不可手术切除的肝细胞癌(HCC)一线治疗中,免疫检查点抑制剂与酪氨酸激酶抑制剂(TKI)联合应用,相较于标准治疗方案,显著改善了患者的无进展生存期(PFS,由BIRC基于RECIST v1.1标准判定)和总生存期(OS)的III期临床试验。
CARES-310研究是一项国际多中心、随机对照Ⅲ期临床研究,该研究共纳入543例既往未接受过系统治疗的不可切除或转移性肝细胞癌患者,按1:1随机接受卡瑞利珠单抗联合阿帕替尼(“双艾”组合)治疗(272例)或接受索拉非尼治疗(271例),主要研究终点是PFS和OS。旨在评价“双艾”组合对比对照组一线治疗不可切除或转移性HCC的有效性和安全性。
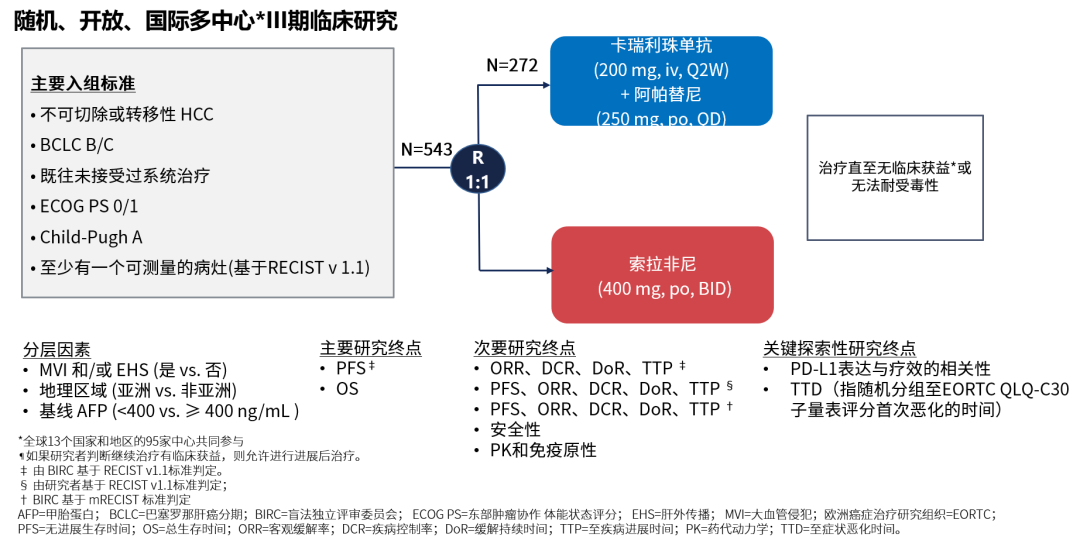
图1. CARES-310研究设计
截至2023年6月14日,共发生了351例(65%)死亡事件,并进行了方案规定的最终分析。

图2. CARES-310研究的统计分析
分别有272例患者和271例患者被分配到卡瑞利珠单抗+阿帕替尼(“双艾”)组和对照组。
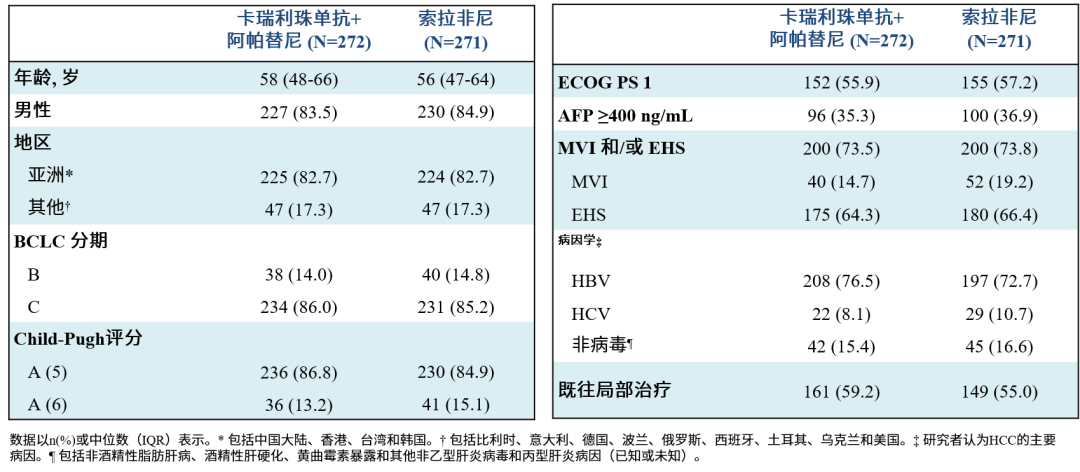
表1. 患者基线特征

临床疗效
-
截至2023年6月14日(最终分析的截止时间),“双艾”组中位随访时间22.1个月,对照组中位随访时间14.9个月。 -
研究治疗结束时,卡瑞利珠单抗+阿帕替尼组43.8%的患者和对照组56.9%的患者接受了后续的全身抗肿瘤治疗。
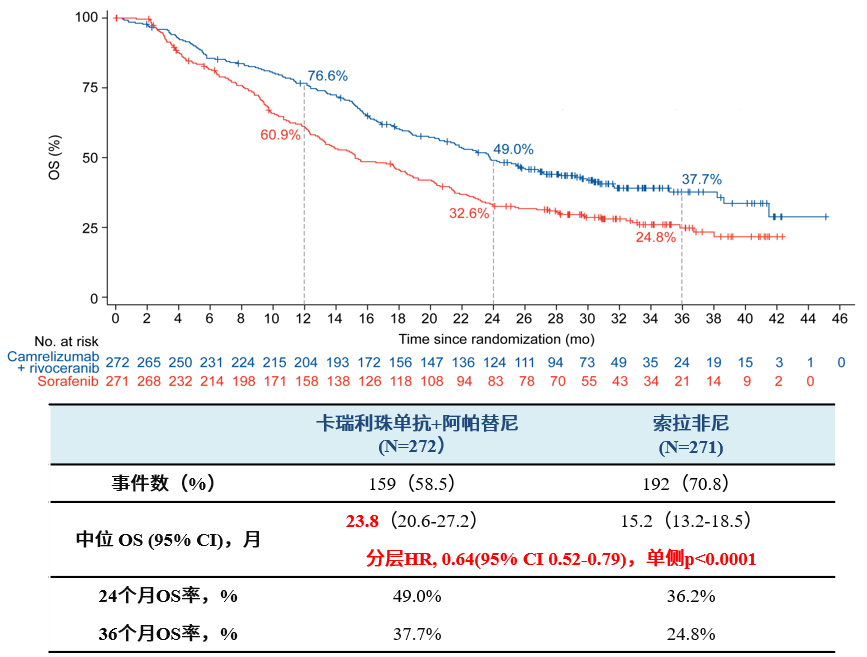
图3. 主要终点OS(FA)
-
亚组分析数据显示,在大多数亚组中,不论区域、种族和肝癌病因如何,相较于对照组,“双艾”组治疗的总生存获益保持一致。
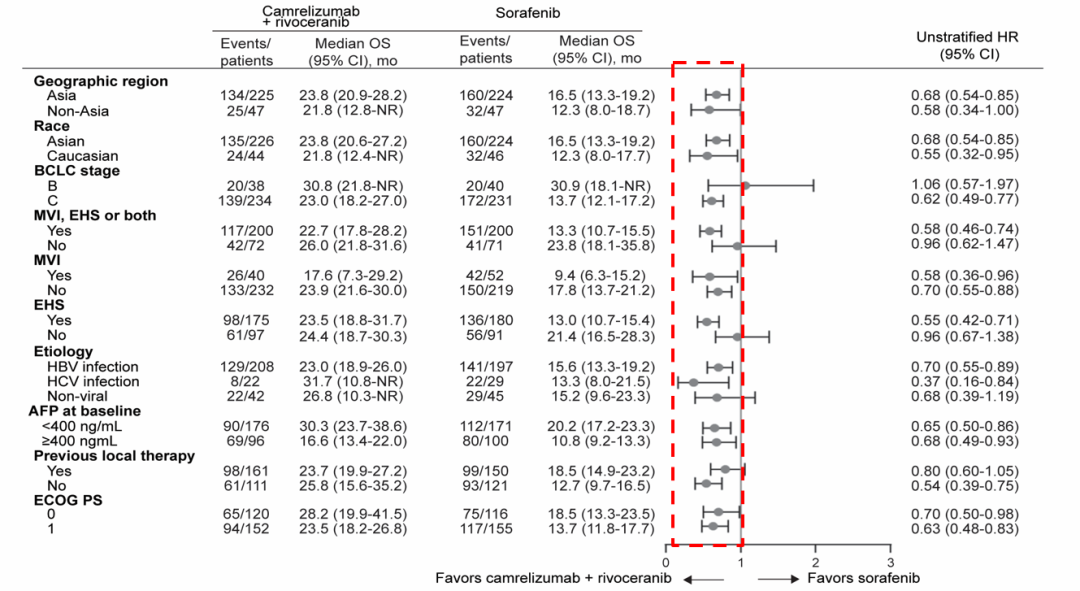
图4. OS(FA)亚组分析-所有亚组均获益
-
PFS、ORR和缓解持续时间DoR(BIRC根据RECIST v1.1 评估)也在长时间随访中保持稳定。
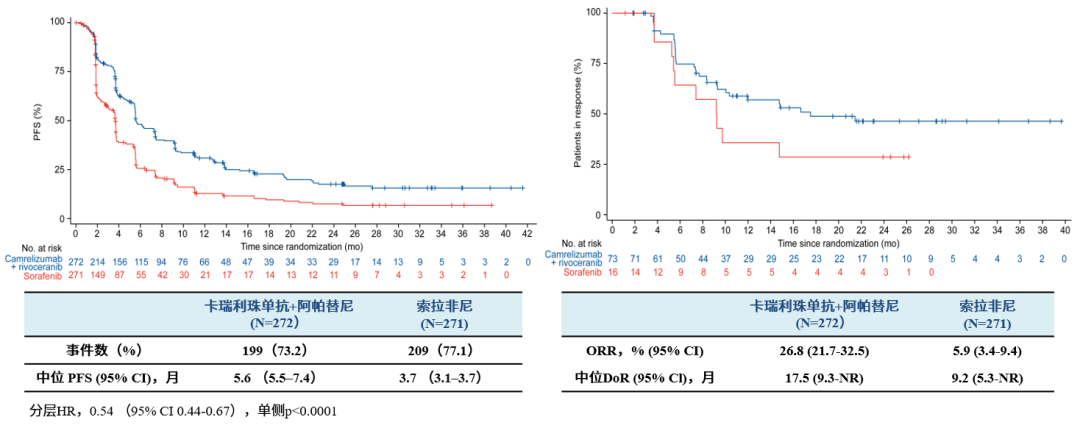
图5. PFS、ORR和DoR的更新数据
安全性
-
安全性数据与期中OS分析一致,未发现新的安全信号。治疗相关不良事件(TRAE)导致17.6%的患者停用卡瑞利珠单抗,16.9%的患者停用阿帕替尼,两种药物均停药发生率均较低,为4.4%。索拉非尼因TRAE导致停药的比例为4.8%。
CARES-310研究获最长生存期
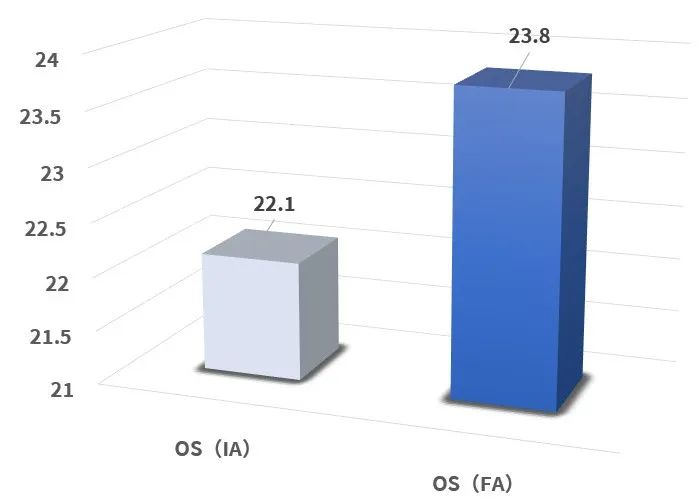
图6. CARES-310研究生存数据更新
众所周知,OS是晚期肝癌最重要的疗效评价指标和金标准,CARES-310研究即便入组人群相较于同类型的研究,疾病分期晚,病情复杂,“双艾”组合依旧获得了现已公布数据的晚期肝癌一线治疗关键性研究中最长的中位OS。
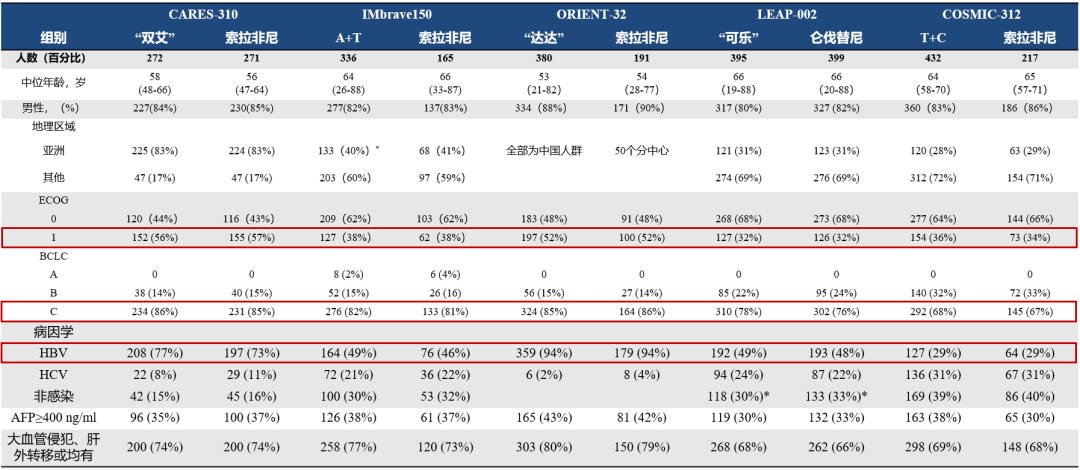
表2. 肝癌一线关键III期研究基线比较2-7
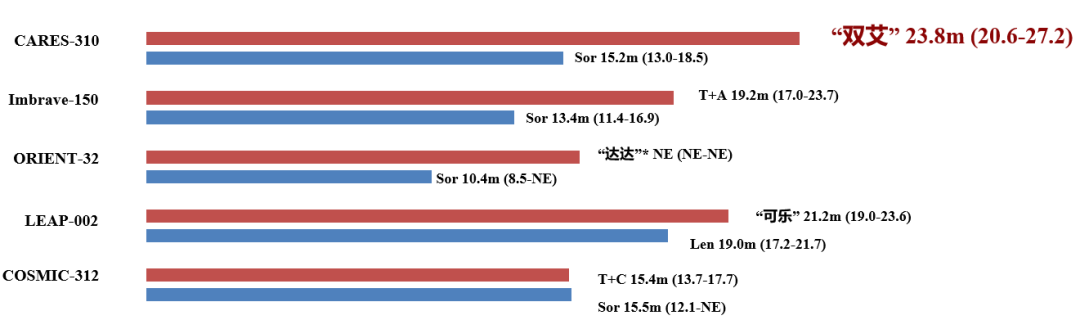
图7.肝癌一线关键III期研究OS比较1-7
总 结
在CARES-310研究方案规定的最终分析中,相比于标准治疗,“双艾”治疗组显示出持续的具有临床意义的生存改善,并且安全性可控。进一步的随访确认了卡瑞利珠单抗联合阿帕替尼方案的良好风险获益比。
CARES-310研究“双艾”治疗组中位OS长达23.8个月,获得了迄今为止已公布数据的晚期肝癌一线治疗关键Ⅲ研究中的最长中位总生存期。
CARES-310研究也是迄今首个且唯一达到PFS和OS双终点的免疫检查点抑制剂联合小分子TKI药物一线治疗晚期HCC的全球Ⅲ期研究,为晚期肝癌患者提供了新的一线治疗选择。
原始出处:
1.Arndt Voge,Shukui Qin, et al. Camrelizumab plus rivoceranib vs sorafenib as first-line therapy for unresectable hepatocellular carcinoma: final overall survival analysis of the phase 3 CARES-310 study.2024 ASCO Poster 90.


