为什么玻尿酸酶可以治疗童颜针微晶瓷导致的栓塞?
时间:2024-07-28 17:02:20 热度:37.1℃ 作者:网络
Hey guys,注射软组织填充剂期间发生的血管不良事件(VAE)对患者和从业者来说仍然是一个具有挑战性的问题。目前公认的软组织填充剂注射后VAE背后的病理机制是基于这样一种假设,即注射的材料会导致动脉内机械栓塞或压迫动脉。
透明质酸酶可以在VAE过程中溶解透明质酸(HA)基软组织填充剂,或用于任何需要去除填充剂的并发症。对于非透明质酸填充剂,缺乏“解药”会给VAE过程带来额外的挑战。
在最近的文章中,作者提出了关于VAEs病因的另一种假设。这两篇文章都描述了使用超声引导的透明质酸酶注射成功治疗HA填充剂注射后的VAEs患者。在所有情况下,临床症状的改善都与多普勒超声上恢复正常血流相吻合,证实了动脉血流与临床症状之间的联系。
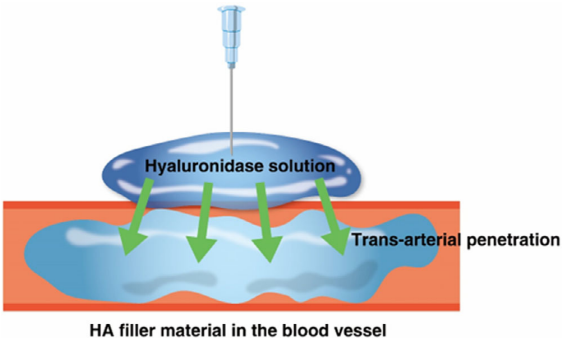
然而,尽管临床症状在皮肤表面可见,Schelke等人描述了HA物质在皮下血管阻塞前后被识别并溶解。这种“血管阻塞”靶向方法的成功结果表明,源自主要面部动脉的穿支体发挥了作用,Taylor等人也将其称为“穿支体概念”或“血管组理论”。该理论表明,穿支动脉为不同的软组织区域或穿支体提供血液供应。填充剂注射引起的痉挛或这种穿支动脉的血管收缩可能会导致其提供的穿支体缺血和坏死,从而导致网状活组织皮肤变化的临床图像。
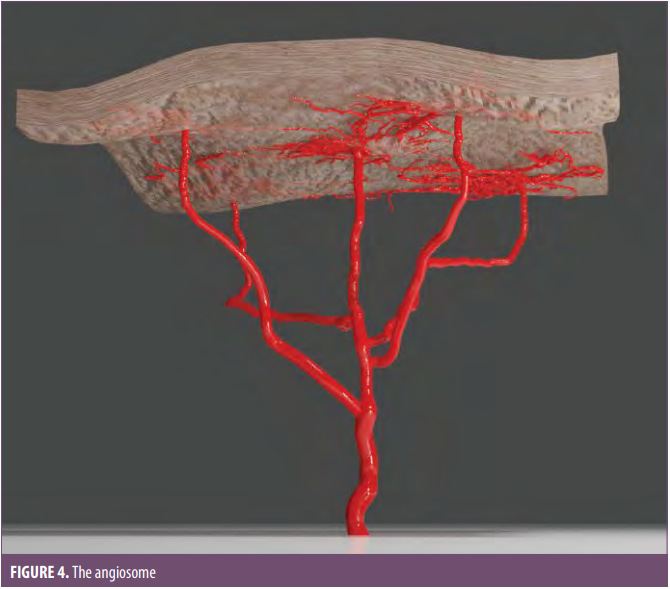
对于HA填充剂诱导的VAE,作者的超声引导下病灶内注射透明质酸酶的方案立即恢复了血流。对于由羟基磷灰石(CaHA)诱导的VAEs,作者使用硫代硫酸钠(STS)作为主要治疗方法,因为它可以溶解CaHA。此外,作者总是使用透明质酸酶,认为它可以增加组织渗透性并分散CaHA产物。使用这种联合方法,在所有患者的多普勒超声成像中观察到血流的改善。鉴于对STS在溶解CaHA方面的有效性的怀疑,以及软组织填充剂注射影响动脉血流的重新研究模型,作者决定使用透明质酸酶作为CaHA(和其他非HA)VAE病例的主要治疗方法,保留STS。在这篇文章中,作者描述了三例由非HA填充剂诱导的VAE,并使用Schelke等人描述的方案用超声引导的透明质酸酶注射成功治疗。
患者1
一名患者在3天前用针在下巴尾部注射(0.2ml)CaHA后,被转诊到作者的填充剂并发症诊所接受VAE治疗。在面诊过程中,在她的下巴左侧可以看到网状的活纹皮肤图案,从头部延伸到下唇,从尾部延伸到颈部(图1),还出现了血肿。患者在类花斑状皮肤模式的水平上疼痛,但也沿着左下颌线疼痛,可能是因为大面积肿胀。在多普勒超声成像上,可以看到左颏下动脉的一些高血管动脉血流。花斑网状皮肤图案下方的皮下组织显示没有血流流动。CaHA填充剂是一种清晰可见的高回声沉积物,具有后部声学阴影。在多普勒超声引导下,作者在SMAS水平注射了150单位透明质酸酶(Hyason,Organon,the Netherlands),流量减少。几分钟后,观察到皮下层中的穿支和小动脉的血流恢复(视频S1)。
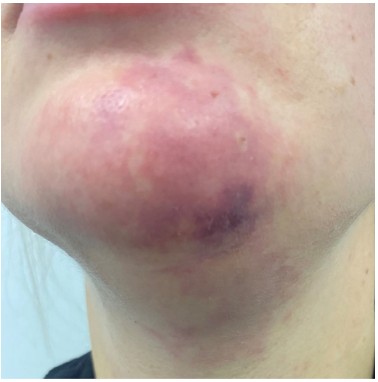
图1
多普勒超声检查发现,CaHA的所有血管不良事件都比HA表现出更多的炎症,因此每天口服泼尼松龙20mg和乙酰水杨酸500mg,持续5天。
患者2
一名53岁的女性患者接受了第二次面部高稀释CaHA治疗。用0.5 ml 2%利多卡因和2.5 ml抑菌盐水以1:2的比例重建CaHA,然后用22G 70mm钝针进行治疗。进入点用0.15ml 1%利多卡因和肾上腺素局部麻醉。在注射了大约2毫升高稀释的CaHA后,美容从业者注意到患者的右下脸开始出现一些瘀伤。患者在受影响区域施加压力,同时对侧也用2.5毫升超稀释混合物进行治疗。此后,患者在左右转动头部时开始感到头晕。患者出现轻微肿胀,毛细血管充盈良好。给患者敷冰袋,敷在面部右下方的肿胀和瘀伤处。当天进行的神经系统评估(瞳孔、眼睛等)正常。第二天对患者进行了重新评估。体检时,右侧颧骨弓下可见瘀伤/血肿、肿胀和大理石花纹皮肤。患者接受了MRI检查,无异常。在多普勒超声成像中,CaHA填充剂可见,为具有后部声学阴影的明确的高回声沉积物。靠近CaHA沉积物和花斑网状皮肤图案下方的皮下组织显示没有流动。在填充材料周围,观察到右侧面横动脉的一些高血管动脉血流和相应的微血管形成。在多普勒超声引导下,以SMAS水平注射300个单位的透明质酸酶,其中流量减少,之后毛细管再填充改善。在多普勒超声下,受影响区域的穿支和小动脉的血流也有所改善。患者开始服用高剂量的泼尼松和美利嗪。第3天,患者开始感觉好些,眩晕症状逐渐减轻,并进行了重新评估。瘀伤和肿胀也消退了。在多普勒超声成像上,到达受影响区域的血流仍然得到改善。在超声引导下再注射150单位的透明质酸酶,以减少血肿和肿胀。在接下来的几天里,患者病情稳步好转;到第11天,瘀伤/活皮肤模式和眩晕的所有症状都已完全消失。患者痊愈,无疤痕。
患者3
一名52岁的女性患者接受了使用生物刺激性填充剂(Lanluma,聚乳酸,PLLA,GCS Co.Ltd,Gyeonggi-do,Korea)的面部治疗。用20ml无菌水和2.0ml 1%利多卡因重建PLLA,然后用22G 50mm钝针进行治疗。进入点用1%利多卡因和肾上腺素局部麻醉。首先,对太阳穴进行每侧1.5毫升的治疗。在颧骨区域右侧注射后,注意到治疗区域的皮肤变白和变色。毛细管再填充延迟。对受影响区域进行了多普勒超声检查。注射的PLLA可见一个定义不清的低回声带,并有一些后部阴影。在填充剂周围,观察到右侧面横动脉的高血管动脉血流。在SMAS水平上总共注射了500个单位的透明质酸酶,观察到异常的血流和紊乱的微血管形成。几分钟内,观察到面横动脉和穿支恢复正常血流进入浅表脂肪层。
患者开始服用乙酰水杨酸300mg每日联合泮托拉唑40mg每日,为期一周。患者痊愈后没有留下疤痕。
讨论
到目前为止,人们普遍认为由相关填充剂组成的栓子是缺氧的最可能原因,这导致人们关注溶解填充剂的治疗策略。事实上,当使用透明质酸酶注射治疗HA诱导的VAE时,这种方法效果很好,似乎支持了作者正在溶解HA填充剂栓子的观点。然而,当作者分析目前关于这一主题的可用文献时,还没有研究能够在体内证明或证明填充剂注射诱导的组织坏死是填充剂材料血管内注射导致填充剂栓剂机械阻碍血流并导致局部缺血的结果。此外,没有研究证明在VAE病例中,透明质酸酶被精确地注射到受影响的血管中,或通过被动扩散最终进入血流,并真正溶解填充剂栓子。将透明质酸酶准确地输送到HA栓子的位置对成功至关重要。最近,Taylor等人引入了穿支体概念。这一概念表明,一条动脉,即穿支,为不同的软组织区域(穿支体)提供血液供应。这种穿支体取决于特定血管的血液供应以维持生存,
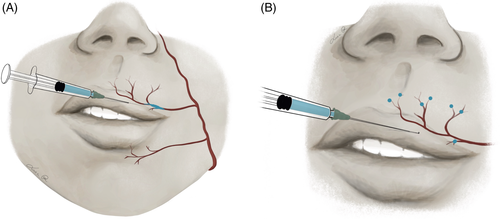
尽管相邻的穿支体通过吻合连接。如果填充剂引起的穿支动脉和连接吻合的痉挛是填充剂注射后VAE的主要原因的假设是正确的,则VAE治疗必须旨在缓解这种痉挛。有趣的是,透明质酸酶已被证明具有恢复小鼠血管痉挛的特性。由于有报道对STS在溶解CaHA方面的作用表示怀疑,并且作者注意到STS/透明质酸酶联合治疗的初步成功,作者在这两例CaHA诱导的VAE中使用透明质酸酶类作为单一治疗方法。这种方法在CaHA诱导的VAE以及PLLA诱导的VAE中的疗效,为填充剂注射后VAE的病理生理学和治疗提供了新的线索。有人可能会说,在HA诱导的VAE病例中,透明质酸酶的有效治疗并不是因为HA填充剂栓子溶解了,而是因为该酶的直接作用释放了血管痉挛。考虑到这些出版物和对血管痉挛假说的日益增长的支持,作者正在真正溶解动脉内填充剂栓子焦点的想法至少应该受到质疑和严格调查。
此外,一些出版物已经描述了与VAE相关的皮肤的基于穿支体的临床活组织模式。如果动脉内滞留的填充剂栓子是VAE的主要原因,那么人们可能会看到更多不规则的皮肤模式和坏死,而不是目前描述的基于穿支体的复发性分布。透明质酸酶可以缓解穿支体血管痉挛的假说也可以解释过去这种治疗方法的成功。需要更多的研究来阐明导致填充剂注射诱导的缺血和坏死的确切病理生理机制。
参考文献
1. Kadouch J, Schelke L, Groh O, Sokol V, Velthuis P. Intralesional hyaluronidase injection to relieve non-hyaluronic acid filler-induced vascular adverse events. Int J Dermatol. 2024 Jul 2. doi: 10.1111/ijd.17355. Epub ahead of print. PMID: 38955457.


