杨卓教授:宫颈癌微创手术新思考
时间:2024-09-13 14:00:32 热度:37.1℃ 作者:网络
编者按:宫颈癌是全球女性面临的严峻健康挑战,微创手术技术的发展为宫颈癌治疗带来了新的希望。在2024年长三角妇科肿瘤青年医师学术研讨会上,辽宁省肿瘤医院杨卓教授发表了《宫颈癌微创手术的新思考》,从不同角度解析宫颈癌的治疗。【医悦汇】特此整理,以飨读者。
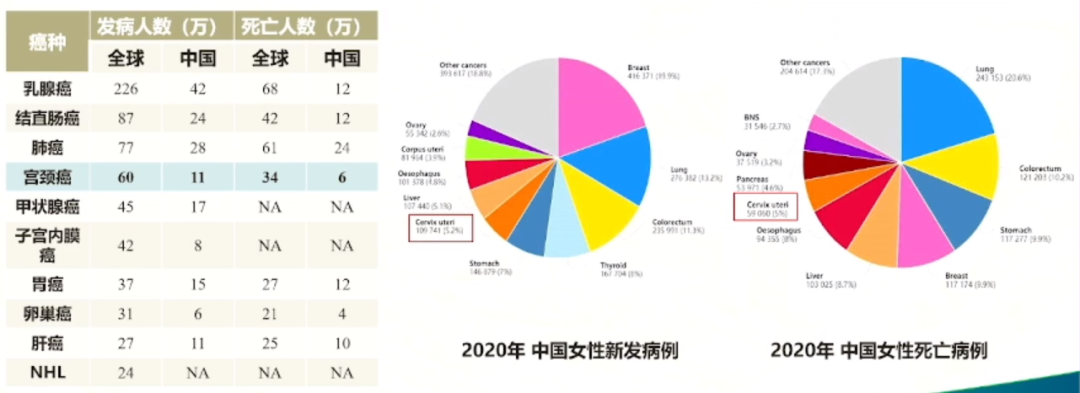
在中国,宫颈癌仍然是一个重大的挑战。2020年中国宫颈癌新发病例近11万,死亡病例近6万,分别约占全球发病和死亡总数的18.3%和17.6%,我国宫颈癌患者约占全球的1/5,防控压力不可谓不大。然而值得庆幸的是,宫颈癌是一种可以通过预防和治疗得到有效控制的疾病,人乳头瘤病毒(HPV)感染是宫颈癌的主要致病因素,并且我国也已建立了有效的一级、二级预防措施来对抗这一疾病。
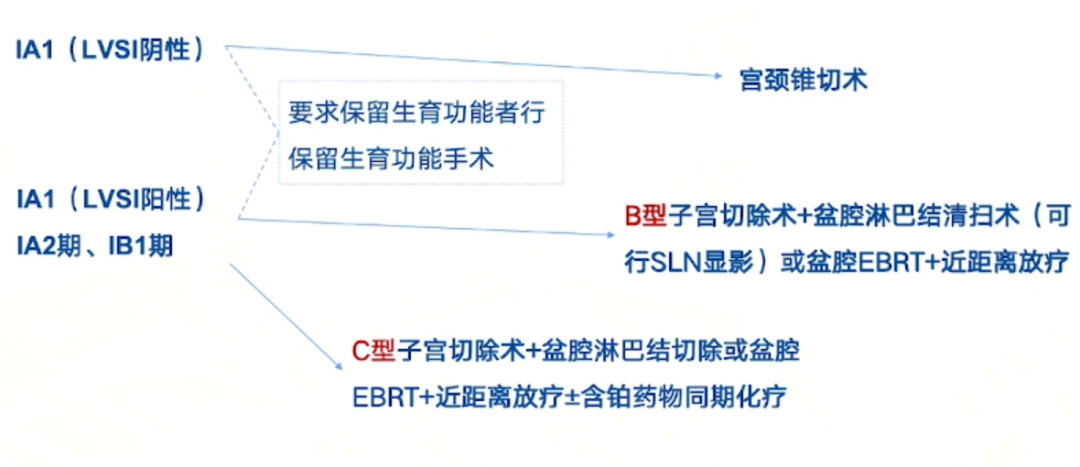
早期宫颈癌治疗原则及手术选择
宫颈癌的治疗强调根据患者具体情况制定个性化治疗方案,包括考虑患者的整体健康状况、生育愿望、年龄、病理组织学类型等因素。同时,治疗决策应遵循最新的临床指南,如美国国家综合癌症网络(NCCN)指南、国际妇产科联盟(FIGO)宫颈癌指南以及中国抗癌协会(CACA)指南等。
目前,我们已经能够对宫颈癌进行精准分期,在宫颈癌的早期阶段,分期管理对于指导后续的临床治疗至关重要。对于希望保留生育能力的患者,应采取保留生育功能的手术方式,而对于不需要保留生育能力的患者,则可根据具体情况,选择适当的子宫根治性切除手术。
初始治疗原则
对于早期宫颈癌手术方法的选择,国际上从2021年FIGO指南及2023年NCCN最新指南,都进行了手术入路推荐,而国内,2023年中国抗癌协会(CACA)的指南指出,对于1A1期宫颈癌,可以选择经腹、经阴道或微创手术。然而,对于伴有淋巴脉管间隙浸润(LVSI)的1A1期患者,以及1B1期或1B2期患者,现有证据仍然支持经腹手术作为标准手术方式。
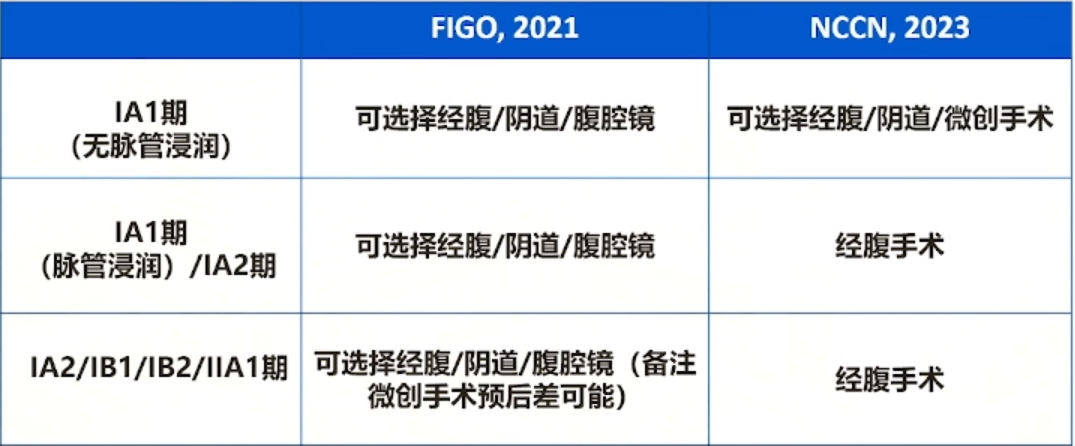
目前国际指南推荐手术入路
宫颈癌微创手术优缺点及发展
微创手术技术之所以受到广泛学习和推广,主要是因为它具有显著的优势。多孔腹腔镜手术因其长臂操作和视觉放大效果,使得盆腔内的手术操作更为便利,这些技术也便于反复学习和全面推广。
而单孔腹腔镜手术,尽管其学习曲线相对较长,并存在筒状视野限制和操作空间拥挤等缺点,但因其能够更好地隐藏腹壁瘢痕,提供更好的美容效果,并且能够快速取出手术标本,而备受女性青睐。
在中国,宫颈癌的微创手术技术自2009年起得到了广泛应用。据相关数据显示,2004年仅有大约0.35%的患者选择了微创手术,而到了2009年,这一比例上升至10%。到了2015年,选择微创手术的宫颈癌患者比例已经达到了50%。
达芬奇机器人手术系统自2008年引入中国后,便在大型医疗中心中被广泛应用。这一技术之所以受到青睐,主要得益于其在精准度、操作稳定性方面的优势,以及相对较短的学习曲线。这些特点不仅提高了手术的成功率,还减少了因手术团队配合不佳而导致的不良影响。
早期宫颈癌术式引发争议
2018年的LACC研究引发了广泛关注,该研究比较了微创根治性子宫切除术与开放式手术在治疗早期宫颈癌中的疗效。结果显示,微创手术组的无病生存率(DFS)和总生存率(OS)均低于开腹手术组,局部区域复发率较高。因此,2019年的NCCN指南更新了建议,对于标准的宫颈癌根治性子宫切除术,推荐选择开腹路径手术。

研究发现的问题
然而,中国的专家们并没有因此全面否定微创手术,而是开始反思和探索,并积极寻找原因和改进措施。专家在研究中发现,对于>2cm的肿瘤,微创根治术的结果更差,而对于<2cm的肿瘤结果是未可知的,从无病生存期(DFS)的事件分析来看,微创手术组的比例高于开腹手术组。特别是在复发病例中,微创手术组的播散性转移比例显著增加。根据当时公布的数据,微创手术组的复发转移播散比例约为24%,相比之下,开腹手术组的这一比例为0%(图1)。对于未经锥切术的患者的愈后会更差,对于经过锥切手术的患者,微创患者的肿瘤愈后则并无差异(图2)。

图1
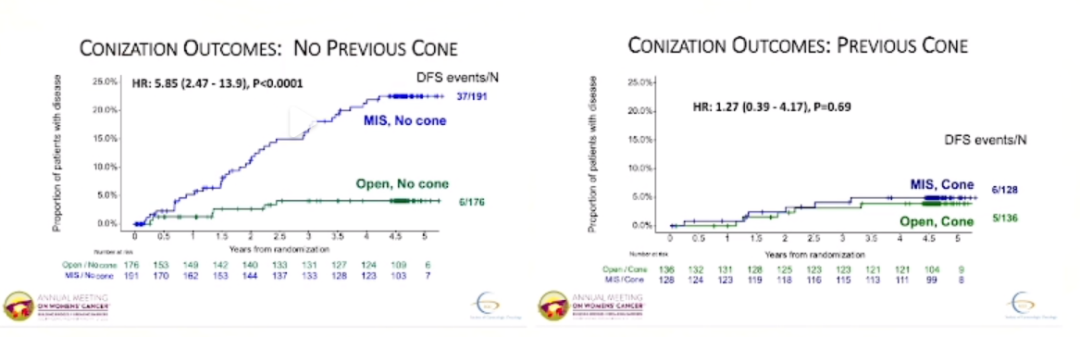
图2
这些问题也促使我们反思并分析总结可能导致不良预后的相关因素。
1.在选择无瘤原则时,我们未能充分考虑宫颈癌这一局部肿瘤疾病的特点,包括使用举宫杯、手术中直接切开阴道以及淋巴结后将其放置在髂窝等位置的操作等,这些可能对患者的术后恢复和长期预后产生负面影响。
2.宫颈癌术后预后不良可能还与患者病情相关,例如肿瘤的大小,肿瘤直径≥2cm,腹腔镜手术会有更高的复发风险,5年的DFS也会明显下降。此外,一些特殊的病理类型,比如说腺癌或者是腺鳞癌,也会致使腹腔镜组的DFS明显降低。
3.术者及医疗中心原因:在每个医疗中心,手术量的多少实际上是宫颈癌根治术后无病生存的一个独立预后因素。医院的手术量与患者的无病生存之间存在着显著的相关性:手术量越大,患者的复发率往往越低。
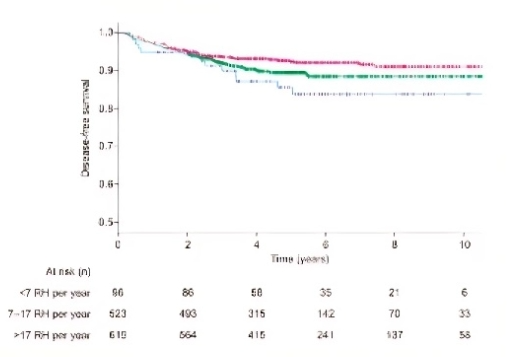
手术量越多,患者复发率越低
解决方法
针对当前的问题,我们正在探索多种解决方案来优化宫颈癌的治疗。目前,我们已经开始全面采用无举宫杯的微创手术技术,这包括选择性地进行宫体缝扎悬吊、凝闭输卵管,以及实施无气腹或封闭阴道后的子宫切除手术等。此外,我们还采用了大量蒸馏水冲洗和从上到下、从外到内、由浅入深的整块淋巴结切除方法,以提高手术的精确性和安全性。
对于宫颈癌微创手术的适应症,我们也正在实施更为严格的评估标准,此外,也在考虑是否应该仅在肿瘤直径<2cm或经过锥切手术后确定的患者中应用,以及考虑是否应该限制在肿瘤负荷较低的情况下。
经阴道根治性子宫切除术
经阴道根治性子宫切除术(RVH)自1994年首次报道以来,已成为妇科手术的经典方法。然而,由于手术视野受限、操作空间狭小,且采用逆行解剖,该手术路径对医生的手感和经验要求较高,导致学习曲线较长。
随着技术进步,机器人辅助腹腔镜手术和腹腔镜联合阴式手术提供了更清晰的手术视野和更高的精确度,提高了手术安全性和有效性。特别是机器人辅助的腹腔镜联合阴式根治性子宫切除术,结合了微创手术的优势,降低了手术难度,并在保持无肿瘤原则的同时,其肿瘤预后与开放手术相媲美。
机器人辅助腹腔镜联合阴式
根治性子宫切除术
在达芬奇机器人辅助的腹腔镜手术中,淋巴结清扫技术与常规腹腔镜手术相似,从外部入路开始,确保淋巴结及其周围组织的完整性,力求整块切除。
我们也在不断探索和完善腹部淋巴结清扫技术,已能在适宜条件下进行全面清扫。机器人手术的淋巴结显影效果优良,有助于前哨淋巴结识别和术中淋巴图谱创建,指导精确清扫。
在盆腔手术中,采用机器人辅助技术,从上方游离输尿管隧道,与传统的下方建立方法相比,提供了更充分的游离空间。手术过程中,我们保持阴道无举宫状态,避免不必要的触碰,确保手术安全和患者舒适度。
在阴道手术中,我们采用全层阴道黏膜切开术,并通过间断缝合技术将阴道壁闭合成套袖状,包绕肿瘤病灶完全封闭。在腹部侧,进行锐性与钝性剥离,切除残余的骶棘韧带和颈腰韧带,随后实施彻底的根治性子宫切除。阴道缝合采用全程环状缝线缝合阴道和腹膜,在12和6个时钟点合并缝合线。肿瘤在直视下操作,避免接触和挤压,确保阴道切除范围充足。我们会根据肿瘤情况、患者年龄和阴道壁厚度进行个体化切除。
数据分析显示,采用腹腔镜或机器人辅助腹腔镜进行阴式根治性子宫切除术,无论是OS还是DFS,其整体预后优于单纯腹腔镜手术,且与开放手术的肿瘤预后相当。
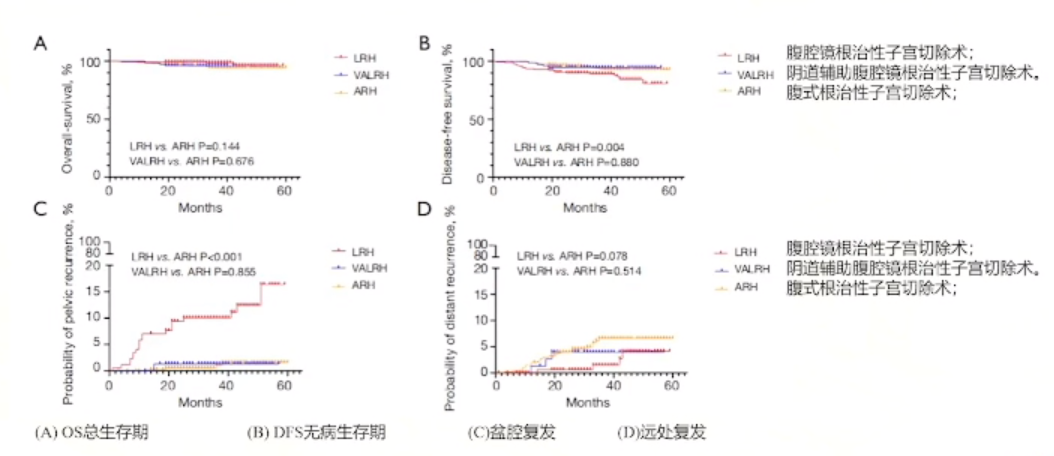
总结
在考虑我国宫颈癌的实际情况时,我们不能一概而论地否定微创手术的价值。我们应该深入分析导致局部复发率高、无病生存率(DFS)低、总生存率(OS)低的潜在原因,并积极改进腹腔镜微创技术。首先,对于不同情况的患者,应根据其具体情况选择最合适的手术方式和路径,制定个性化的治疗方案。对于早期宫颈癌患者,我们应严格控制微创手术的适应症,优先考虑低风险患者,并提高手术操作的精准度,严格遵守肿瘤无接触原则,以确保患者能够从微创手术中获得真正的益处。其次,我们需要收集和分析更多的数据,以评估经过改进的腹腔镜手术与开腹手术在应用价值和预后方面的差异,从而为临床决策提供更有力的支持。


