结肠癌肝转移,既往丙肝病史,66岁男性治疗效果如何?| MDT病例分享
时间:2024-10-14 06:01:09 热度:37.1℃ 作者:网络
01 病例介绍
病例摘要
患者:男,66岁,身高177cm,体重60kg,体表面积1.77m2 ,ECOG评分1分。
主诉:确诊结肠癌近4年
吸烟史、饮酒史:少量
既往史:既往有“丙肝”病史,曾口服“来迪派韦索磷布韦片”治疗三月。否认结核等传染病史,否认高血压、糖尿病、癫痫等慢性病史,否认其他手术、外伤、输血史,否认食物、药物过敏史,预防接种史不详。
2020年5月无明显诱因出现下腹部疼痛,多为晨起或进食后,为间断性隐痛,排便后可缓解。
2020-05-30至江苏大学附属医院消化内科门诊,查结肠镜示:横结肠处不规则菜花样新生物,占肠腔4/5圈(距离肛门60cm),新生物病理示:横结肠腺癌。
上腹部CT平扫+增强(2020-06-05,本院):肝内多发结节,考虑转移瘤。右肾囊肿。
基因检测:未检测到KRAS/NRAS/BRAF V600E激活突变,APC第16外显子移码突变,SMAD4第7外显子截短突变,TP53第4外显子错义突变。
诊断:横结肠腺癌IV期(肝转移,KRAS/NRAS/BRAF野生型)
治疗经过
mFOLFOX6+西妥昔单抗治疗6周期后,复查MRI,提示肝脏转移瘤变少、变小。
2020-10-12于江苏省人民医院行横结肠癌根治术,肝脏肿瘤未探及。
术后病理:中分化、腺癌。肿瘤穿透固有肌层达浆膜层,或侵犯无腹膜覆盖的结直肠旁组织(T3)。肠周淋巴结未见癌转移(0/15),肠周脂肪结缔组织内另见癌结节2枚,大小直径0.3-0.4cm,肠上下切缘未见肿瘤累及。
术后MRI:肝脏多发异常强化灶,考虑异常灌注可能性大。
术前影像学检查:
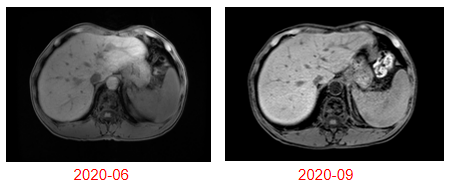
术后影像学检查:
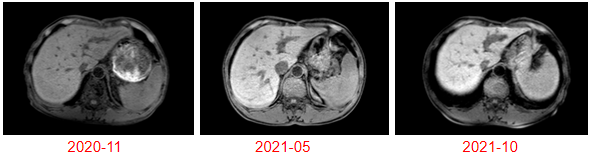
2020-11至2021-05行西妥昔单抗+mFOLFOX6 4周期后西妥昔单抗+卡培他滨维持治疗,PFS 6个月;
2020-11至2022-03行西妥昔单抗+FOLFIR治疗,PFS 16个月;
2022-04至2023-01行西妥昔单抗+雷替曲塞治疗,PFS 9个月;
2023-02至2023-04行西妥昔单抗+曲氟尿苷嘧啶治疗,PFS 2个月;
2023-04至2024-01行贝伐珠单抗+曲氟尿苷嘧啶治疗,PFS 9个月;
2024-02至病例讨论时行贝伐珠单抗+信迪利单抗200mg+拓泊替康治疗。
影像学检查:
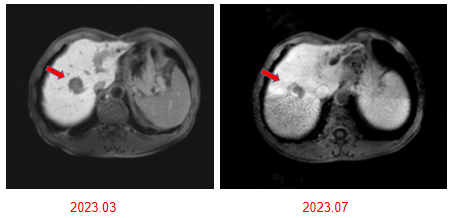
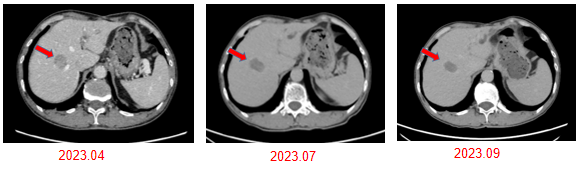
02 病例讨论
问题 1:对于RAS/BRAF野生型mCRC(特别是对于右半结肠癌患者),一线靶向选择应严格按照指南选择还是考虑其他因素?转化治疗后肝转移病灶很难根治,肝脏潜在病灶的后续管理有什么合适的方法?
江苏省中西医结合医院-肿瘤科-胡灿红:患者接受了靶向治疗和化疗,至今已有四年生存时间。目前,患者的肝脏病灶得到了良好的控制,尽管病灶多发,但体积较小,因此患者的生活质量仍然保持在较高水平。预计患者的生存期还有望进一步延长。
从这个病例中,我们观察到西妥昔单抗在右半结肠肿瘤治疗中的有效性。尽管先前的研究表明西妥昔单抗在左半结肠肿瘤中的疗效更佳,但本次病例显示在右半结肠中也取得了显著的治疗效果。因此,最新的NCCN指南更新了相关建议,取消了西妥昔单抗在左半结肠肿瘤治疗中的限制。
然而,目前临床证据表明,西妥昔单抗的跨线治疗尚缺乏足够的有效性证据。相比之下,贝伐珠单抗的跨线治疗则得到了一些临床证据的支持。在一线治疗进展后,可以在二线治疗中更换化疗方案,并与贝伐珠单抗联合使用,这已被证明是有益的。
今天的病例也让我们认识到,在结直肠癌的晚期治疗中,经典的治疗方案,如靶向治疗联合抗血管生成治疗和免疫治疗,是可行的选择。例如,贝伐珠单抗联合替雷利珠单抗的治疗方案,也显示出了良好的疗效。
综上所述,在多种综合治疗手段的支持下,晚期结直肠癌患者的总生存期可以得到显著延长,生存四年以上已不再是罕见情况。因此,结直肠癌的治疗前景是可观的,这反映了靶向治疗和免疫治疗在结直肠癌治疗中的重要价值。
南京医科大学第二附属医院-肿瘤科-陆彬彬:患者接受了基因检测,结果显示为KRAS、BRAF野生型,但在诊断时未考虑MSI(微卫星不稳定性)和MMR(错配修复)的表达水平。建议在诊断时进行免疫组化检测,以评估患者的MMR或MSI状态,因为免疫治疗可能对这类患者有效。
患者接受了FOLFIRI(5-FU/亚叶酸、伊立替康)和FOLFOX(5-FU/亚叶酸、奥沙利铂)联合西妥昔单抗的转化治疗。在治疗初期,患者的肿瘤退缩明显,肝脏转移灶不可见。遗憾的是,在手术探查时未能发现肝脏病灶,仅进行了结肠切除。有时,切除原发病灶可能会刺激转移病变的增长,这可能是患者在切除原发病灶后肝脏病灶逐渐增大的原因。
在患者肝脏病灶增大时,应重新评估手术机会,如果可能,进行二次手术切除肝脏病灶,可能会改善预后。在右半结肠癌的治疗中,虽然并非所有患者都能从西妥昔单抗中获益,但与左半结肠癌相比,右半结肠癌患者从西妥昔单抗治疗中获益的程度可能较低。
在转化治疗中,可以考虑使用西妥昔单抗联合mFOLFOX6(改良的叶酸、5-FU、奥沙利铂)的方案,因为研究表明这种联合方案的转化成功率高于单独使用贝伐珠单抗。对于跨线治疗,目前贝伐珠单抗的证据较多,而其他药物的跨线治疗证据较少。
在二线治疗中,如果西妥昔单抗维持治疗效果不佳,可以考虑更换为贝伐珠单抗联合化疗或其他治疗。此外,对于肝脏上的两个主要病灶,可以考虑局部治疗,如消融治疗或冷冻治疗,以减少对胆管的损伤。局部放疗或粒子植入治疗也是可行的方案。
目前,患者使用贝伐珠单抗联合方案的维持治疗效果很好,耐受性良好,可以继续使用。如果病灶无法控制,可以考虑进行局部处理,再联合其他治疗方案,以延长患者的生存时间。
南京医科大学第二附属医院-肿瘤科-王娟:这位结直肠癌患者经历了一系列个性化的治疗步骤。最初,患者接受了标准的西妥昔单抗联合FOLFOX方案化疗,并在病情稳定后,继续使用西妥昔单抗加卡培他滨进行维持治疗。随着病情的进展,治疗方案调整为继续使用西妥昔单抗,并更换化疗药物为FOLFIRI,这种策略在标准临床实践中并不常见。
对于肝脏转移灶的局部处理,包括了立体定向放疗(SBRT)、消融或介入治疗等方法。鉴于患者目前正在接受免疫治疗、贝伐珠单抗和TAS-102的联合治疗,如果肝脏病灶能够持续退缩或稳定,那么进行局部治疗是有必要的。对于肝转移灶,在新辅助治疗后虽然影像学上消失了,但仍有可能存在微小病灶,因此可以考虑使用普美显增强核磁共振成像来进一步明确。
此外,建议进行多学科团队(MDT)评估,包括外科、肝胆外科和普外科医生,以全面评估患者的状况,尤其是对于手术时发现的多发肝转移病灶。有时,尽管影像学上显示病灶消失,但手术中可能无法精确定位所有病灶。因此,外科医生的经验和技能在这种情况下至关重要。如果评估显示可以切除,那么应该考虑在第一次手术时尽可能地切除所有影像学可见的病灶,以减少复发风险。
患者已经经历了四年多的治疗,目前的总生存期是相当可观的。随着免疫治疗和靶向治疗药物的不断涌现,对于晚期结直肠癌患者,即使在三线或四线治疗之后,仍然有可能通过药物的重新组合来获得更好的治疗效果。这对于临床医生来说,是一个值得探索的问题。
03 MDT小结
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。通过西妥昔单抗联合双药化疗的转化治疗,患者达到了显著的疗效。值得称赞的是,该病例在关键治疗节点均有MDT团队的参与。
该病例为66岁男性患者,诊断为横结肠腺癌IV期(肝转移,KRAS/NRAS/BRAF野生型 )。这位患者经过mFOLFOX6联合西妥昔单抗、西妥昔单抗联合FOLFIRI等一系列治疗,目前生存时间达四年多,还在接受治疗中,算是一个比较成功的病例。
述评
南京明基医院-肿瘤科-王志宁:在结直肠癌的治疗中,药物选择相对有限,因此局部治疗的重要性日益凸显。这不仅考验着医生的专业知识,也要求医生与患者进行有效沟通,尤其是在涉及到胆管等复杂部位的治疗时。我们医院虽然已经开展了一些局部治疗,但像冷冻消融这样的技术还未实施。
此外,局部放疗,包括放射粒子植入,也是我们尚未开展的治疗方式。我认为放疗在某些情况下类似于外科手术,对医生的个体技术要求极高。这不仅关系到治疗的成功率,还涉及到并发症的控制,这些都与医生对治疗部位的精准把握密切相关。
总的来说,局部治疗在结直肠癌治疗中扮演着越来越重要的角色,但同时也带来了新的挑战,需要我们不断学习、探索和提高。


