【专家述评】| 甲状腺癌的流行病学现状及其影响因素研究进展
时间:2025-02-28 12:15:30 热度:37.1℃ 作者:网络
[摘要] 甲状腺癌是内分泌系统和头颈部最常见的恶性肿瘤,包括甲状腺乳头状癌(papillary thyroid cancer,PTC)、甲状腺滤泡癌(follicular thyroid cancer,FTC)、甲状腺髓样癌(medullary thyroid cancer,MTC)和甲状腺未分化癌(anaplastic thyroid cancer,ATC)等类型。近几十年,甲状腺癌的发病率迅速增长。从地区分布看,甲状腺癌的发病率在经济发达地区较高;发病率上升较快的主要是一些高收入国家,但在一些中等收入国家也出现了快速增长;从人群看,女性甲状腺癌的发病率显著高于男性。中国甲状腺癌的发病率近年来也呈明显上升趋势,但死亡率则稳定在较低水平;城市甲状腺癌的发病率高于农村地区,东部沿海地区发病率高于中、西部地区。甲状腺癌的病因复杂多样,主要危险因素包括遗传易感性、辐射暴露、碘摄入水平、内分泌紊乱、环境污染和生活方式等。其中,辐射暴露(尤其是儿童时期暴露于电离辐射)是甲状腺癌公认的重要诱因。此外,碘摄入不足或过量均可影响甲状腺功能,增加癌变风险。在遗传学方面,甲状腺癌的家族聚集性和基因(如BRAF、RET/PTC等)突变在疾病发生中的作用已被广泛研究,而环境污染和现代生活方式的改变也可能在某种程度上促进了疾病的发生、发展。因此,对有甲状腺癌家族史的人群开展早期筛查,减少不必要的医疗辐射暴露,及时干预肥胖等与生活方式密切相关的危险因素,可能对甲状腺癌的预防有积极意义。甲状腺癌患者大多数预后良好,预后影响因素主要有病理学分型(PTC预后较好,而MTC和ATC预后较差)、临床分期(TNM分期Ⅰ、Ⅱ期预后较好,Ⅲ、Ⅳ期较差)、生理因素(女性总体预后优于男性)、遗传学因素和环境因素等。了解甲状腺癌的流行病学现状,探索其发病和预后的影响因素,对于甲状腺癌的预防、治疗和健康管理有重要意义。未来可基于甲状腺癌危险因素进行高危人群的识别和干预研究,从而预防肿瘤,减少疾病负担,提高患者的生存质量。
[关键词] 甲状腺癌;流行现状;危险因素;早期预防
[Abstract] Thyroid cancer is the most common malignant tumor of the endocrine system and head and neck region, mainly including papillary thyroid cancer (PTC), follicular thyroid cancer (FTC), medullary thyroid cancer (MTC) and anaplastic thyroid cancer (ATC). Over the past few decades, the global incidence of thyroid cancer has risen rapidly, nearly doubling in some developed countries. Geographically, thyroid cancer incidence is higher in economically developed regions. Although the fastest increase in incidence has been observed in high-income countries, certain middle-income countries have also reported significant growth. Demographically, the incidence rate is notably higher in women than in men. In China, the incidence of thyroid cancer has increased significantly in recent years, while the mortality rate has remained stable at a low level. Urban areas report higher incidence rates than rural areas, and eastern coastal regions have higher rates compared to central and western regions. The etiology of thyroid cancer is multifaceted, with major risk factors including genetic predisposition, radiation exposure, iodine intake levels, endocrine disruptions, environmental and lifestyle factors. Among these, radiation exposure (particularly ionizing radiation during childhood) is a recognized critical risk factor. In addition, both insufficient and excessive iodine intake can disrupt thyroid function, thereby increasing disease risk. Genetic factors, such as familial clustering and gene (BRAF, RET/PTC, etc.) mutations, have been widely studied, while environmental pollution and modern lifestyles may also contribute to disease onset. Therefore, it is beneficial to conduct early screening for people with a family history of thyroid cancer, reduce unnecessary medical radiation exposure and conduct intervention on lifestyle-related risk factors such as obesity to prevent and control thyroid cancer. Most patients with thyroid cancer have a favorable prognosis. The main factors influencing the prognosis include pathological typing (PTC has a relatively better prognosis, while MTC and ATC have poorer prognoses), clinical staging (patients at TNM stages Ⅰ and Ⅱ have better prognoses, while those at stages Ⅲ and Ⅳ have worse ones), physiological factors (the overall prognosis of females is superior to that of males), genetic factors and environmental factors. Understanding the epidemiological trends and identifying factors influencing the onset and prognosis of thyroid cancer are essential for its prevention, treatment and health management. Future research should focus on identifying high-risk populations and developing targeted interventions to prevent and control thyroid cancer, reduce its disease burden, improve quality of life for patients, and lower healthcare costs.
[Key words] Thyroid cancer; Epidemiology; Risk factors; Early prevention
1 引言
甲状腺癌是内分泌系统和头颈部最常见的恶性肿瘤,也是危害女性健康的常见恶性肿瘤[1]。最近几十年,全球甲状腺癌的发病率迅速增长,在一些发达国家中几乎增长了2倍[1]。中国甲状腺癌的发病率同样呈上升趋势,《2021中国肿瘤登记年报》[2]公布的最新数据显示,中国甲状腺癌排在女性恶性肿瘤发病顺位的 第4位。了解甲状腺癌的流行病学现状,探索其发病和预后的影响因素,对于甲状腺癌的预防、治疗和健康管理有重要意义。
根据世界卫生组织(World Health Organization,WHO)第5版分类[3],甲状腺滤泡起源的肿瘤为甲状腺内最常见的肿瘤,其中恶性肿瘤包括分化型甲状腺癌(differentiated thyroid carcinoma,DTC)、高级别分化型甲状腺癌(differentiated high grade thyroid carcinoma,DHGTC)、低分化甲状腺癌(poorly differentiated thyroid carcinoma,PDTC)和甲状腺未分化癌(anaplastic thyroid carcinoma,ATC)。由于PTC、FTC和嗜酸细胞癌都来源于甲状腺滤泡细胞,分化较好,因此统称为DTC[4-5]。甲状腺髓样癌(medullary thyroid cancer,MTC)来源于甲状腺滤泡旁降钙素分泌细胞(C细胞),属于甲状腺神经内分泌肿瘤,有散发型和家族遗传型两类[5]。ATC可以由滤泡细胞发展而来,也可以由分化的甲状腺癌去分化形成,虽然其较为少见,但恶性程度高,预后差[6]。近年来,全球甲状腺癌的发病率快速上升,然而死亡率则稳定保持在较低水平。本述评重点介绍上述相关病理学类型甲状腺癌的流行病学现状。
2 甲状腺癌的流行病学现状
2.1 甲状腺癌的全球流行现状
最近几十年甲状腺癌的发病率在全球范围和中国都呈上升趋势,其中主要表现为甲状腺乳头状癌(papillary thyroid cancer,PTC)发病率的增长(图1、2)[7]。2022年全球甲状腺癌预计新发病例为821 173例,其中女性614 686例,占74.9%;死亡47 485例,其中女性30 241例,占63.7%[8]。美国国立癌症研究所(National Cancer Institute,NCI)公布的数据[9]显示, 2024年美国甲状腺癌预计新发病例数为44 020例,其中71.6%为女性。与甲状腺癌快速上升的发病率形成对比,甲状腺癌的死亡率一直维持在较低水平。例如,2024年美国因甲状腺癌死亡人数预计为2 170例,男女构成相似,分别为990例和1 180例[9]。
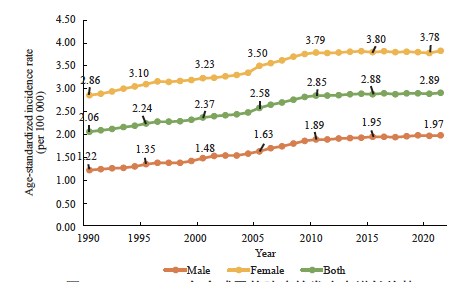
图1 1990—2021年全球甲状腺癌的发病率增长趋势
Fig.1 The trend of global incidence rate of thyroid cancer from 1990 to 2021
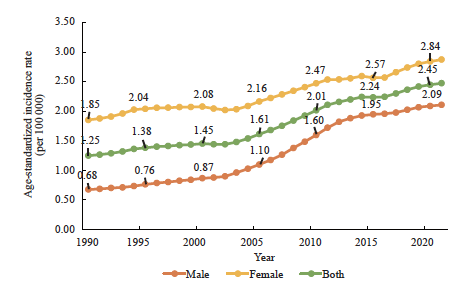
图2 1990—2021年中国甲状腺癌的发病率增长趋势
Fig. 2 The trend of incidence rate of thyroid cancer in China from 1990 to 2021
2.1.1 地区分布
国际癌症研究中心(International Agency for Research on Cancer,IARC)的全球癌症报告数据[1]显示,甲状腺癌的发病率在经济发达地区较高,如2022年北美洲和西欧地区的发病率达11.9/10万和7.4/10万;但在经济相对欠发达地区,如西非和南亚地区等地区较低,发病率分别为0.9/10万和1.6/10万[8]。然而,近年来随着甲状腺癌筛查技术的快速发展和卫生服务可及性的提高,一些发展中国家的甲状腺癌发病率也随之升高[10]。2022年塞浦路斯共和国女性甲状腺癌的发病率居全球首位,高达51.6/10万人,是2002年的5倍,已成为该国女性排在第2位的恶性肿瘤[11]。中国2022年甲状腺癌的发病率高达24.6/10万人,成为亚洲甲状腺癌发病率第1位的国家,但死亡率保持相对稳定[11]。
2.1.2 时间分布
过去30年里,甲状腺癌的发病率在全球范围内均快速上升。发病率上升较快的主要是一些高收入国家,但在一些中等收入国家,如中国、巴西和土耳其,甲状腺癌的发病率也出现了快速增长[1]。全球癌症统计数据[12]显示,1998—2002年全球甲状腺癌的年龄标化发病率比1993—1998年增加了约58%,其中女性增长(66.7%)更为明显。美国健康监测、流行病学及结局数据库(Surveillance, Epidemiology, and End Results Program,SEER)数据[13]显示,甲状腺癌的发病率从1974—1977年的4.56/10万人上升至2010—2013年的14.42/10万人,年增长率为3%;而死亡率变化不大,1994—1997年为0.40/10万人,2010—2013年为0.46/10万人。
2.1.3 人群分布
甲状腺癌的发病率呈现出明显的性别差异,女性的发病率显著高于男性。IARC 2020年的癌症报告数据[11]显示,在全球范围内,女性甲状腺癌的发病风险约为男性的3倍。美国2022年肿瘤监测数据[9]显示,女性甲状腺癌的新发病例数是男性的2.85倍(38 620∶13 549),甲状腺癌新发病例数在女性所有恶性肿瘤中排在第6位;2014—2016年,全年龄段女性罹患甲状腺癌的风险是男性的2.71倍(1.9%∶0.7%)。在日本,女性和男性的发病率比约为3∶1[14]。甲状腺癌的发病率也存在种族差异,白人和黑人发病率的年增长速度较亚洲人快;NCI收集的1992—2004年的数据[15]显示,非拉美裔白人甲状腺癌发病率的年均增长率最高,黑人次之,亚裔和美洲印第安人/阿拉斯加原住民最低。
2.2 中国甲状腺癌的流行病学现状
IARC 2022年的全球癌症报告[8]数据显示,中国的甲状腺癌新发病例数已超过46万,占全球新发病例数一半以上,死亡数占24.3%。近年来中国甲状腺癌的发病率明显上升,但死亡率则稳定在较低水平[16];东部沿海地区的发病率高于中、西部地区,女性发病率明显高于男性[17]。
《2021中国肿瘤登记年报》[2]显示,2018年甲状腺癌发病位居癌症发病谱第8位。全部甲状腺癌病例中有明确组织学类型的病例占87.60%,其中绝大多数为PTC,占93.43%;其次为FTC,占1.27%;MTC占0.18%[2]。新发病例数为84 593例,占全部癌症发病的5.41%;其中男性21 198例,女性34 263例;发病率为16.17/10万,以中国人口构成计算的标准化发病率(中标率)为13.99/10万,以世界人口构成计算的标准化发病率(世标率)为12.01/10万;女性中标率是男性的2.93倍;0~74岁的累积发病率为1.14%[2]。甲状腺死亡位居癌症死亡谱第22位,因甲状腺癌死亡病例3 232例,占全部癌症死亡的0.35%[2]。甲状腺癌的死亡率为0.62/10万,中标死亡率为0.38/10万,世标死亡率为0.37/10万[2]。
2.2.1 地区分布
2018年全国肿瘤登记数据[2]显示,中国东、中、西部地区的甲状腺癌发病率存在差异:东部最高(中标率为21.95/10万),中部次之(中标率为10.78/10万),西部最低(中标率为6.41/10万)。甲状腺癌的发病率在城乡之间也存在差异,城市甲状腺癌的发病率(中标率为18.26/10万)高于农村地区(中标率为10.31/10万)[2]。甲状腺癌的死亡率中部地区(中标死亡率为0.41/10万)高于东部(中标死亡率为0.38/10万)和西部地区(中标死亡率为0.35/10万);城市的中标死亡率(0.41/10万)高于农村(0.35/10万)[2]。
2.2.2 时间分布
中国肿瘤登记数据[14]显示,2008—2017年,中国女性人群甲状腺癌的发病率以年度变化百分比(annual percent change,APC)17.1%的速度增长,已成为中国发展最快的恶性肿瘤。2002—2016年甲状腺癌的发病率逐年上升,而死亡率则稳定保持在较低水平[14]。中国沿海地区近年来发病率上升尤为明显。例如,江苏省甲状腺癌的中标发病率呈逐年上升趋势,由2009年的2.02/10万上升至2019年的13.63/10万,APC为22.05%,中标死亡率为0.23/10万[18]。青岛市甲状腺癌的发病率由2010年的1.0/10万上升到2017年的11.68/10万,但死亡率总体保持平稳,约为0.20/10万[19]。深圳市甲状腺癌的发病率由2001年的3.55/10万上升至2015年的17.97/10万,APC约11%[20]。
2.2.3 人群分布
《2021中国肿瘤登记年报》[2]显示,2018年中国女性甲状腺癌的发病率在各年龄段均高于男性,女性中标发病率是男性的2.93倍。女性甲状腺癌发病自15~19岁组开始快速上升,至50~54岁组达高峰,而男性则从20~24岁组开始呈缓慢上升趋势[2]。儿童青少年人群甲状腺癌的发病率较低,约1.45/10万。14岁后甲状腺癌的发病率显著增加,占青少年人群发病率的74%[21]。
3 甲状腺癌的危险因素
3.1 影响甲状腺癌发病的危险因素
对于全球甲状腺癌发病率近年来快速上升的原因,意见尚不统一。有学者认为主要与过度诊断相关,筛查技术的进步和医疗资源的普及导致发现更多小且低风险病灶[22-23],依据是甲状腺癌发病率的增长主要归因于微小癌(肿瘤直 径<1 cm)的增加,而死亡率却长期稳定在较低水平[10,24];但也有学者认为,甲状腺癌发病相关环境危险因素的变化,如碘摄入量、肥胖等也有可能导致甲状腺癌发病率上升[25],其依据是肿瘤直径>4 cm的甲状腺癌发病率也在增加,而死亡率的相对稳定主要是由于甲状腺癌的死亡风险较低,而观察时间相对不够所致[26]。影响甲状腺癌发病的主要危险因素详见表1。探讨甲状腺癌的危险因素及其分布,对于降低发病风险、减少发病有重要意义。

3.1.1 生理因素
甲状腺癌的发病风险与性别及年龄相关。如前所述,世界范围内女性甲状腺癌的发病率均显著高于男性,中国女性甲状腺癌的发病率是男性的3倍左右[4]。这些现象提示女性生育相关因素可能是甲状腺癌的危险因素。既往多项研究表明甲状腺癌组织中有雌激素受体(estrogen receptor,ER)的表达,雌激素本身可能是促癌物,其代谢中2-羟基化反应增强可能与甲状腺癌的发生有关[27]。美国1973—2013年白人不同性别各年龄段甲状腺癌的发病率数据[28]显示,育龄期女性的发病率高,60岁以前女性甲状腺癌的发病率随年龄增加而上升,60岁以后逐渐下降。与女性不同,男性甲状腺癌的发病率基本呈现随年龄上升的趋势,仅在80岁以后发病率下降。
3.1.2 生活和环境因素
3.1.2.1 电离辐射
暴露于电离辐射是甲状腺癌比较明确的危险因素,核电站或核武器产生的放射性物质,以及一些医疗设备检查是电离辐射的主要来源[1]。如切尔诺贝利核电厂事故产生的核污染物、暴露于头颈部和胸背部上端的放射性检查等[29-30]。儿童时期的电离辐射暴露史与PTC密切相关,可能与儿童对放射线较成人更加敏感有关[4]。
3.1.2.2 肥胖
近年来全球肥胖和甲状腺癌的发病率都在增长,并且两者的变化几乎同步[31]。流行病学研究[32]指出,无论儿童或成人,超重或肥胖均可能增加甲状腺癌的发病风险。超重和肥胖对甲状腺癌的影响与其病理学分型有关,可能增加PTC和ATC的风险,而降低MTC的发病风险[33-34]。肥胖影响甲状腺癌的机制尚不明确,可能通过胰岛素抵抗、影响甲状腺激素和雌激素通路等影响发病风险[35,36]。
3.1.2.3 碘摄入量
碘是合成甲状腺激素的原料,人体每天通过饮食摄入一定量的碘。WHO推荐的碘摄入量为:0~59个月学龄前儿童为90 μg/d,6~12岁儿童为120 μg/d,12岁以上儿童和成人为150 μg/d,妊娠期和哺乳期女性为250 μg/d。碘摄入量和甲状腺疾病的发病风险呈“U”型曲线,摄入缺乏或过量均可影响甲状腺疾病的发生、发展[37]。碘的长期过高或过低摄入可能导致脑垂体过度分泌促甲状腺激素,促使甲状腺滤泡上皮细胞增生从而可能诱发甲状腺癌[38]。此外,碘摄入量还与甲状腺癌的病理学分型有关,碘摄入过量则PTC的发病率升高,而碘摄入不足可能导致FTC的发病率升高[4,25,39]。缺碘的甲状腺对放射性物质更加敏感,暴露于电离辐射环境更容易诱发甲状腺癌。
随着食盐碘化的普及,高碘与甲状腺癌发病率的关系受到关注,但目前国内外研究尚无定论。中国学者研究发现,高碘地区甲状腺癌的发病率高,且多为PTC[39]。在韩国人群中开展的研究[38,40]显示,碘缺乏或过量摄入可能会引起BRAF基因的突变,而该基因突变被认为是诱发甲状腺癌的重要危险因素,且与肿瘤向甲状腺外侵犯、淋巴结转移及癌症进展密切相关。
3.1.2.4 其他
精神因素如不良情绪、压力、焦虑等可能增加甲状腺癌的发病风险[41]。关于饮食因素与甲状腺癌关联性的研究[42]提示,烟熏、高脂、高淀粉食品的过多摄入可能增加甲状腺癌的发病风险,但仍需进一步研究验证。
3.1.3 遗传学因素
甲状腺癌发病率的种族差异提示其可能与遗传因素有关[43]。家族史是甲状腺癌可能的危险因素[41],约5%的患者有相同类型的甲状腺癌家族史,且部分研究[6]显示,家族性甲状腺癌比散在发病的甲状腺癌预后差。原癌基因突变、错配修复基因突变和抑癌基因失活等均可能导致甲状腺癌变[4]。目前被普遍认可的与甲状腺癌发生、发展或预后有关的基因有RET、BRAF、 RAS和p53等。原癌基因BRAF突变是甲状腺癌常见的基因突变,有研究[44]显示,甲状腺癌患者中BRAF基因突变频率为29%~83%。抑癌基因如控制细胞周期的p53基因可阻止受损的DNA重新复制,其基因突变可能促使DTC向PDTC和ATC转化,且与甲状腺癌发展、转移、侵袭和预后有关[44]。
3.2 影响甲状腺癌发展和预后的相关因素
甲状腺癌患者大多数预后良好,生存期达10~30年。甲状腺癌的发展和预后受多种因素的综合影响,了解这些相关因素,对于指导治疗、判断预后和健康管理有重要意义。
3.2.1 病理学分型
甲状腺癌的病理学分型是影响患者预后的重要因素。PTC多见于30~45岁女性,较早出现颈部淋巴结转移,分化较好,恶性程度相对较低,预后良好;FTC常见于50岁左右中年人群,中度恶性、可侵犯血管,经血运转移至肺、肝、骨及中枢神经系统[45],预后较PTC差[46]。例如,NCI数据[47]显示,1969—2013年,在美国阿拉斯加原住民中PTC的5年生存率为100%,而FTC的5年生存率为86.3%(95% CI:54.7%~96.5%)。但目前的研究结论尚不一致,也有学者认为两者的预后并不存在显著差异[48]。PTC和FTC有时亦可共存,例如,PTC又可进一步划分为经典PTC(classical PTC,CPTC)和滤泡型PTC(follicular variant of PTC,FVPTC)等,其预后亦有不同。MTC较为少见,恶性程度高,可有颈部淋巴结侵犯和血行转移[45]。ATC最为少见,但侵袭性强,发病迅速、恶性程度高,预后差,1年生存率仅5%~15%[49]。
3.2.2 临床分期
美国癌症联合会(American Joint Committee on Cancer,AJCC)发布的甲状腺癌TNM分期系统是目前公认的评估患者生存预后的参考标准,AJCC于2017年更新发布了第8版TNM分期系统[50]。根据该分期方法,临床上把肿瘤大小、被膜侵犯、淋巴结转移作为评定甲状腺癌分期及预后的重要指标。在DTC中,肿瘤直径>4 cm、癌组织突破腺体、颈部淋巴结转移及远处转移者预后较差;TNM分期Ⅰ、Ⅱ期预后较好,Ⅲ、Ⅳ 期较差;多灶性甲状腺癌也被列为不良预后的危险因素[45]。
3.2.3 生理因素
虽然女性甲状腺癌的发病率高于男性,但女性的总体预后优于男性。甲状腺癌确诊时的年龄也是影响甲状腺癌预后的重要因素:AJCC将年龄>45岁作为甲状腺癌患者淋巴结转移及术后复发的危险因素,而第8版甲状腺癌TNM分期系统[51-52]将高危年龄由45岁提升至55岁。一项针对PTC患者的研究[53]显示,尽管年轻患者局部复发频繁,但预后良好,而老年患者则相对预后较差;而另一项针对PTC和甲状腺微小乳头状癌(papillary thyroid microcarcinoma,PTMC)患者的研究[54]发现,患者年龄作为肿瘤生长预测指标的效应在PTC和PTMC之间存在显著差异,年龄≥60岁是PTC患者死亡的强预测因素,年龄<40岁是PTMC生长的独立预测因素。
3.2.4 遗传学因素
不同种族甲状腺癌生存率存在差异,提示遗传因素可能影响甲状腺癌的发病和患者预后[47]。在基因层面,前述影响甲状腺癌发生的原癌基因和抑癌基因突变,也可能对甲状腺癌的发展和预后产生影响。既往多项研究[55-57]显示,BRAF基因突变与甲状腺癌的复发及不良预后相关,p53基因突变可能促进DTC向PDTC和ATC转化,并且与甲状腺癌的发展、转移、侵袭和预后相关。IG20基因在甲状腺癌中有促细胞增殖的作用[44]。然而根据单个基因作为临床预后的判断尚存在争议,可联合其他多个基因进行检测和风险评估[44]。
3.2.5 环境因素
社会经济学状况可能影响甲状腺癌患者的生存。例如,一项针对美国甲状腺癌患者的回顾性队列研究[58]发现,社会经济地位的脆弱性使甲状腺癌患者的生存率下降,且总体脆弱性的增加与PTC晚期分期的可能性增加及进行指定治疗的可能性降低有关。
综上所述,虽然甲状腺癌的病因研究结果仍存在不确定性,但对已知明确的致病因素如电离辐射暴露可进行有效预防。服用碘化钾是在核事故中保护公众的医学应急措施之一,能够有效地阻止甲状腺对放射性碘的吸收[4]。对于医疗检查中的电离辐射,美国食品药品管理局于2010年倡导减少不必要的医疗辐射暴露,以影像学检查的合理性与暴露剂量的最优化为原则保护患者安全[59]。及时干预肥胖等与生活方式密切相关的危险因素,对于甲状腺癌的预防可能有积极意义。同时,对于MTC,特别是遗传性MTC,根据易感基因的检测结果有针对性地进行预防性治疗也可能起到预防作用[60]。
4 结语
甲状腺癌作为内分泌系统和头颈部最常见的恶性肿瘤,发病率在全球迅速增长,同时在高收入国家和地区、女性人群中发病率较高,其危险因素包括遗传易感性、辐射暴露、碘摄入水平、内分泌紊乱、环境污染和生活方式等。了解甲状腺癌的流行病学现状,探索其发病和预后的影响因素,对于甲状腺癌的预防、治疗和健康管理有重要意义。目前关于甲状腺癌流行病学现状的人群研究数量较少,未来可基于甲状腺癌危险因素进行高危人群的识别与干预研究,从而预防肿瘤,减少疾病负担,提高患者的生存质量并降低医疗成本。
第一作者:
张芷悦,学士。通信作者:
何慧婧,博士,副研究员;林岩松,博士,主任医师。
作者贡献声明:
张芷悦:文献检索,论文撰写;何慧婧:提出研究思路,论文撰写指导;单广良,林岩松:论文撰写指导。
[参考文献]
[1] International Agency for Research on Cancer. World Cancer Report[R]. Lyon, 2014.
[2] 赫捷, 魏文强. 2021中国肿瘤登记年报[M]. 北京: 人民卫生出版社, 2023.
HE J, WEI W Q. Annual report of cancer registries in China 2021[M]. Beijing: People’s Medical Publishing House, 2023.
[3] 刘志艳, 刘书佚, 王馨培, 等. 第5版WHO甲状腺滤泡源性肿瘤分类解读[J]. 中华病理学杂志, 2023, 52(1): 7-12.
LIU Z Y, LIU S Y, WANG X P, et al. Interpretation of the 5th edition WHO classification of follicular cell derived thyroid tumors[J]. Chin J Pathol, 2023, 52(1): 7-12.
[4] 董 芬, 张 彪, 单广良. 中国甲状腺癌的流行现状和影响因素[J]. 中国癌症杂志, 2016, 26(1): 47-52.
DONG F, ZHANG B, SHAN G L. Distribution and risk factors of thyroid cancer in China[J]. China Oncol, 2016, 26(1): 47-52.
[5] 梁 岭. 甲状腺癌临床特征分布与发病相关因素研究[D]. 合肥: 安徽医科大学, 2019.
LIANG L. Research on the distribution of clinical characteristics and related risk factors of thyroid cancer[D]. Hefei: Anhui Medical University, 2019.
[6] 杨 雷, 王 宁. 甲状腺癌流行病学研究进展[J]. 中华预防医学杂志, 2014, 48(8): 744-748.
YANG L, WANG N. Research progress in the epidemiology of thyroid cancer[J]. Chin J Prev Med, 2014, 48(8): 744-748.
[7] KITAHARA C M, SOSA J A. Understanding the ever-changing incidence of thyroid cancer[J]. Nat Rev Endocrinol, 2020, 16(11): 617-618.
[8] PIZZATO M, LI M M, VIGNAT J, et al. The epidemiological landscape of thyroid cancer worldwide: GLOBOCAN estimates for incidence and mortality rates in 2020[J]. Lancet Diabetes Endocrinol, 2022, 10(4): 264-272.
[9] AHMEDIN JEMAL DVM P. Cancer statistics, 202 [J]. CA A Cancer J Clin, 2024, 74(1): 12-49.
[10] AHN H S, KIM H J, WELCH H G. Korea’s thyroid-cancer “epidemic”: screening and overdiagnosis[J]. N Engl J Med, 2014, 371(19): 1765-1767.
[11] WILD C P, WEIDERPASS E, STEWART B W. World cancer report: cancer research for cancer prevention[J]. 2020
[12] KILFOY B A, ZHENG T Z, HOLFORD T R, et al. International patterns and trends in thyroid cancer incidence, 1973-2002
[J]. Cancer Causes Control, 2009, 20(5): 525-531.
[13] LIM H, DEVESA S S, SOSA J A, et al. Trends in thyroid cancer incidence and mortality in the United States, 1974-2013[J]. JAMA, 2017, 317(13): 1338-1348.
[14] Globocan: global cancer statistics[EB/OL]. [2024-12-20]. https://gco.iarc.fr.
[15] YU G P, LI J C, BRANOVAN D, et al. Thyroid cancer incidence and survival in the national cancer institute surveillance, epidemiology, and end results race/ethnicity groups[J]. Thyroid, 2010, 20(5): 465-473.
[16] WANQING CHEN PHD M, MPH R Z, et al. Cancer statistics in China, 2015[J]. CA A Cancer J Clin, 2016, 66(2): 115-132.
[17] 张思维, 郑荣寿, 孙可欣, 等. 2016年中国恶性肿瘤分地区发病和死亡估计: 基于人群的肿瘤登记数据分析[J]. 中国肿瘤, 2023, 32(5): 321-332.
ZHANG S W, ZHENG R S, SUN K X, et al. Estimation of cancer incidence and mortality in different geographic areas of China in 2016: analysis based on population-based cancer registry data[J]. China Cancer, 2023, 32(5): 321-332.
[18] 杨志杰, 王 璐, 钱 云, 等. 2009—2019年江苏省肿瘤登记地区甲状腺癌发病趋势和年龄变化特征分析[J]. 中国肿瘤, 2024, 33(12): 991-998.
YANG Z J, WANG L, QIAN Y, et al. Trends of incidence and diagnostic age of thyroid cancer in cancer registration areas of Jiangsu province from 2009 to 2019[J]. China Cancer, 2024, 33(12): 991-998.
[19] 罗亭亭, 孟 迪, 张 华, 等. 2010—2017年青岛市居民甲状腺癌发病与死亡分析[J]. 中华肿瘤防治杂志, 2019, 26(17): 1231-1236.
LUO T T, MENG D, ZHANG H, et al. Analysis of thyroid cancer incidence and death among Qingdao residents from 2010 to 2017[J]. Chin J Cancer Prev Treat, 2019, 26(17): 1231-1236.
[20] 雷 林, 尚庆刚, 刘维耿, 等. 深圳市2001—2015年甲状腺癌发病现状和趋势分析[J]. 中国肿瘤, 2019, 28(7): 504-508.
LEI L, SHANG Q G, LIU W G, et al. Incidences and epidemiologic trends of thyroid cancer in Shenzhen, 2001-2015[J]. China Cancer, 2019, 28(7): 504-508.
[21] 杜 瑞, 梁 楠, 孙 辉. 儿童及青少年甲状腺癌诊疗进展[J]. 中国普通外科杂志, 2019, 28(11): 1431-1436.
DU R, LIANG N, SUN H. Progress of diagnosis and treatment of thyroid carcinoma in children and adolescents[J]. Chin J Gen Surg, 2019, 28(11): 1431-1436.
[22] LI M M, DAL MASO L, PIZZATO M, et al. Evolving epidemiological patterns of thyroid cancer and estimates of overdiagnosis in 2013-17 in 63 countries worldwide: a population-based study[J]. Lancet Diabetes Endocrinol, 2024, 12(11): 824-836.
[23] KITAHARA C M. The growing global burden of thyroid cancer overdiagnosis[J]. Lancet Diabetes Endocrinol, 2024, 12(11): 780-782.
[24] VACCARELLA S, FRANCESCHI S, BRAY F, et al. Worldwide thyroid-cancer epidemic? The increasing impact of overdiagnosis[J]. N Engl J Med, 2016, 375(7): 614-617.
[25] BARREA L, GALLO M, RUGGERI R M, et al. Nutritional status and follicular-derived thyroid cancer: an update[J]. Crit Rev Food Sci Nutr, 2021, 61(1): 25-59.
[26] LI N, DU X L, REITZEL L R, et al. Impact of enhanced detection on the increase in thyroid cancer incidence in the United States: review of incidence trends by socioeconomic status within the surveillance, epidemiology, and end results registry, 1980-2008[J]. Thyroid, 2013, 23(1): 103-110.
[27] LIU J, XU T M, MA L, et al. Signal pathway of estrogen and estrogen receptor in the development of thyroid cancer[J]. Front Oncol, 2021, 11: 593479.
[28] NASH S H, LANIER A P, SOUTHWORTH M B. Occurrence of endocrine and thyroid cancers among Alaska native people,
1969-2013[J]. Thyroid, 2018, 28(4): 481-487.
[29] MEMON A, ROGERS I, PAUDYAL P, et al. Dental X-rays and the risk of thyroid cancer and meningioma: a systematic review and meta-analysis of current epidemiological evidence[J]. Thyroid, 2019, 29(11): 1572-1593.
[30] BAKER S R, BHATTI W A. The thyroid cancer epidemic: is it the dark side of the CT revolution? [J]. Eur J Radiol, 2006, 60(1): 67-69.
[31] FRANCHINI F, PALATUCCI G, COLAO A, et al. Obesity and thyroid cancer risk: an update[J]. Int J Environ Res Public Health, 2022, 19(3): 1116.
[32] KITAHARA C M, MCCULLOUGH M L, FRANCESCHI S, et al. Anthropometric factors and thyroid cancer risk by histological subtype: pooled analysis of 22 prospective studies[J]. Thyroid, 2016, 26(2): 306-318.
[33] BURRAGE L C, MCLEOD D S A, JORDAN S J. Obesity and thyroid cancer risk[J]. Curr Opin Endocrinol Diabetes Obes, 2023, 30(5): 244-251.
[34] SCHMID D, RICCI C, BEHRENS G, et al. Adiposity and risk of thyroid cancer: a systematic review and meta-analysis[J]. Obes Rev, 2015, 16(12): 1042-1054.
[35] AVGERINOS K I, SPYROU N, MANTZOROS C S, et al. Obesity and cancer risk: emerging biological mechanisms and perspectives[J]. Metabolism, 2019, 92: 121-135.
[36] ALMQUIST M, JOHANSEN D, BJÖRGE T, et al. Metabolic factors and risk of thyroid cancer in the metabolic syndrome and cancer project (Me-Can)[J]. Cancer Causes Control, 2011, 22(5): 743-751.
[37] LAURBERG P, PEDERSEN I B, KNUDSEN N, et al. Environmental iodine intake affects the type of nonmalignant thyroid disease[J]. Thyroid, 2001, 11(5): 457-469.
[38] 吴 恋, 于健春, 康维明, 等. 碘营养状况与甲状腺疾病[J]. 中国医学科学院学报, 2013, 35(4): 363-368.
WU L, YU J C, KANG W M, et al. Iodine nutrition and thyroid diseases[J]. Acta Acad Med Sin, 2013, 35(4): 363-368.
[39] 崔玉山, 刘洪亮. 甲状腺癌流行病学特征和碘营养关系研究进展[J]. 环境卫生学杂志, 2020, 10(2): 212-217.
CUI Y S, LIU H L. Epidemiological characteristics of thyroid cancer and its association with iodine nutrition[J]. J Environ Hyg, 2020, 10(2): 212-217.
[40] KIM H J, PARK H K, BYUN D W, et al. Iodine intake as a risk factor for BRAF mutations in papillary thyroid cancer patients from an iodine-replete area[J]. Eur J Nutr, 2018, 57(2): 809-815.
[41] 陈 芳, 吴 凯, 徐明星, 等. 基于病例对照研究的甲状腺癌危险因素的meta分析[J]. 中华地方病学杂志, 2017, 36(4): 250-256.
CHEN F, WU K, XU M X, et al. Meta-analysis of risk factors of thyroid cancer: base on case-control study[J]. Chin J Endem, 2017, 36(4): 250-256.
[42] JUNG S K, KIM K, TAE K, et al. The effect of raw vegetable and fruit intake on thyroid cancer risk among women: a case-control study in South Korea[J]. Br J Nutr, 2013, 109(1): 118-128.
[43] ROCHE A M, FEDEWA S A, SHI L L, et al. Treatment and survival vary by race/ethnicity in patients with anaplastic thyroid cancer[J]. Cancer, 2018, 124(8): 1780-1790.
[44] 郑维晖, 龚巍巍, 陆 凤, 等. 甲状腺癌相关基因突变和表观遗传学研究进展[J]. 中华流行病学杂志, 2017, 38(11): 1579-1583.
ZHENG W H, GONG W W, LU F, et al. Progress in research of thyroid carcinoma related gene mutation and epigenetics[J]. Chin J Epidemiol, 2017, 38(11): 1579-1583.
[45] 宋创业, 严 丽, 孟艳林, 等. 甲状腺癌发生发展及预后的相关影响因素[J]. 中华普通外科学文献(电子版), 2020, 14(1): 72-75.
SONG C Y, YAN L, MENG Y L, et al. Related factors of occurrence, development and prognosis of thyroid cancer[J]. Chin Arch Gen Surg Electron Ed, 2020, 14(1): 72-75.
[46] KIM H, KIM H I, KIM S W, et al. Prognosis of differentiated thyroid carcinoma with initial distant metastasis: a multicenter study in Korea[J]. Endocrinol Metab (Seoul), 2018, 33(2): 287-295.
[47] TANG J N, KONG D G, CUI Q X, et al. Racial disparities of differentiated thyroid carcinoma: clinical behavior, treatments, and long-term outcomes[J]. World J Surg Oncol, 2018, 16(1): 45.
[48] ELISEI R, MOLINARO E, AGATE L, et al. Are the clinical and pathological features of differentiated thyroid carcinoma really changed over the last 35 years? Study on 4 187 patients from a single Italian institution to answer this question[J]. J Clin Endocrinol Metab, 2010, 95(4): 1516-1527.
[49] KIM J Y, MYUNG J K, KIM S, et al. Prognosis of poorly differentiated thyroid carcinoma: a systematic review and metaanalysis[J]. Endocrinol Metab (Seoul), 2024, 39(4): 590-602.
[50] 张 磊, 董云伟, 胡神保, 等. 美国癌症联合委员会甲状腺癌分期系统(第8版)修订对甲状腺乳头状癌分期的影响[J].中国癌症杂志, 2018, 28(7): 491-496.
ZHANG L, DONG Y W, HU S B, et al. The impact of American Cancer Joint Committee revised thyroid cancer staging system (8th edition) on staging of papillary thyroid carcinoma[J]. China Oncol, 2018, 28(7): 491-496.
[51] SHTEINSHNAIDER M, MUALLEM KALMOVICH L, KOREN S, et al. Reassessment of differentiated thyroid cancer patients using the eighth TNM/AJCC classification system: a comparative study[J]. Thyroid, 2018, 28(2): 201-209.
[52] KAZAURE H S, ROMAN S A, SOSA J A. The impact of age on thyroid cancer staging[J]. Curr Opin Endocrinol Diabetes Obes, 2018, 25(5): 330-334.
[53] CHO J S, YOON J H, PARK M H, et al. Age and prognosis of papillary thyroid carcinoma: retrospective stratification into three groups[J]. J Korean Surg Soc, 2012, 83(5): 259-266.
[54] ITO Y, MIYAUCHI A, KOBAYASHI K, et al. Prognosis and growth activity depend on patient age in clinical and subclinical papillary thyroid carcinoma[J]. Endocr J, 2014, 61(3): 205-213.
[55] 黄美玲, 李永平, 凌 瑞. BRAF V600E基因突变与乳头状甲状腺癌淋巴结转移相关性的meta分析[J]. 中国肿瘤, 2017, 26(2): 145-151.
HUANG M L, LI Y P, LING R. A meta-analysis on the
correlation between BRAF V600E gene mutation and lymph nodes metastasis in papillary thyroid carcinoma[J]. China Cancer, 2017, 26(2): 145-151.
[56] FILETTI S, DURANTE C, HARTL D, et al. Thyroid cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2019, 30(12): 1856-1883.
[57] XING M Z, ALZAHRANI A S, CARSON K A, et al. Association between BRAF V600E mutation and recurrence of papillary thyroid cancer[J]. J Clin Oncol, 2015, 33(1): 42-50.
[58] FEI-ZHANG D J, VERMA R, ARIMOTO R, et al. Social vulnerability association with thyroid cancer disparities in the United States[J]. Thyroid, 2024, 34(2): 225-233.
[59] MILLER D L, KAKAR S, JIANG L, et al. The U.S. Food and Drug Administration’s role in improving radiation dose management for medical X-ray imaging devices[J]. Br J Radiol, 2021, 94(1126): 20210373.
[60] DABELIĆ N, JUKIĆ T, FRÖBE A. Medullary thyroid cancerfeature review and update on systemic treatment[J]. Acta Clin Croat, 2020, 59(Suppl 1): 50-59.


