晚期非鳞NSCLC一线免疫治疗,STK11突变“腰斩”患者生存期,无论共突变如何
时间:2025-03-03 12:16:52 热度:37.1℃ 作者:网络
非癌基因成瘾非小细胞肺癌(NSCLC)的一线治疗方案主要为单独使用免疫治疗(ICI)或联合化疗(CT-ICI)。KRAS、TP53、KEAP1、SMARCA4或STK11等基因变异,可能对生存结局产生影响。对145例在我院接受一线免疫治疗(IO)或免疫联合化疗(CT-IO)的晚期非鳞状(nsq)NSCLC患者进行观察性研究,这些患者使用实验室开发的NGS panel进行了检测。本研究的主要目的是评估STK11突变患者的临床结局。随后,我们利用公开的OAK/POPLAR数据集进行外部验证,该数据集包括接受单药ICI或CT的nsq NSCLC患者。男性(59.7%)、既往吸烟者(61.1%)、ECOG PS为0-1的患者(84%)、接受一线CT-IO治疗的患者(58.6%)占比较高。44.8%的患者存在KRAS突变,21.4%存在KEAP1突变,50.3%存在TP53突变,13.1%存在SMARCA4突变,14.4%存在STK11突变。STK11突变患者的中位总生存期(mOS)为8个月(95% CI:5-16.7),而STK11野生型患者的mOS为17.3个月(95% CI:8.9-24.4)(p=0.038)。TP53(8.3个月 vs 17.3个月)、KRAS(9.2个月 vs 15.9个月)和KEAP1(8.9个月 vs 15.9个月)突变患者的mOS有较短的趋势,但差异无统计学意义。SMARCA4状态对mOS无影响。在单变量(风险比(HR)1.74,p=0.041)和校正性别、年龄、ECOG PS评分、治疗方式(ICI vs CT-ICI)、KRAS、KEAP1、TP53和SMARCA4状态后的多变量模型(HR 1.97,p=0.025)中,STK11突变与较差的OS相关。在我们的队列中,基因变异对无进展生存期(PFS)无影响。在OAK/POPLAR数据集中,单变量(HR 2.01,p<0.001)和校正年龄、性别、治疗方式(ICI vs CT)、KRAS、KEAP1、TP53和SMARCA4状态后的多变量模型(HR 1.66,p=0.001)显示,STK11突变(60/818例患者)与死亡风险增加显著相关。本研究表明,在接受一线ICI或CT-ICI治疗的nsq NSCLC患者中,STK11突变与较短的mOS相关。这种不良预后影响似乎与ICI治疗类型无关。
研究背景
晚期非小细胞肺癌(NSCLC)的治疗策略是根据预测性生物标志物,将非癌基因成瘾和癌基因成瘾疾病区分开来。免疫检查点抑制剂(ICI)是非癌基因成瘾NSCLC治疗的基石。
KRAS基因激活突变在肺腺癌中约占25%-30%。由于最新试验证实新研发的药物有效,KRAS突变不再是无靶向治疗方案的靶点。多项研究评估了KRAS突变在免疫治疗中的预测和预后作用,但结果存在差异,因为STK11、KEAP1、TP53和SMARCA4等基因共突变,也可能影响预后。
丝氨酸/苏氨酸激酶11(STK11)是一种抑癌基因,其编码的蛋白通过激活AMPK通路,参与细胞代谢、增殖和生长过程。约15%的nsq NSCLC患者存在STK11失活,且高达30%的患者同时存在KRAS突变。携带STK11突变的NSCLC患者,其肿瘤微环境(TME)具有独特特征,表现为低T CD8、高肿瘤内中性粒细胞以及低PD-L1表达。因此,KRAS/STK11共突变影响TME的组成,肿瘤相关中性粒细胞和调节性T细胞(T-reg)浸润增加,T CD8减少,同时PD-L1表达降低。Kelch样ECH相关蛋白1(KEAP1)参与细胞氧化应激调节,其功能异常可能促进肿瘤发生。无论组织学类型是鳞癌还是腺癌,携带KEAP1突变的NSCLC患者,其特征为淋巴细胞浸润低,甚至呈现“免疫荒漠”表型。SMARCA4基因转录BRG1蛋白,该蛋白参与染色质重塑复合物。约10%的NSCLC患者存在SMARCA4缺陷,其预后相关性尚不明确。TP53是一种抑癌基因,编码的蛋白参与细胞代谢、增殖、凋亡和衰老。TP53的生理影响,以及其失活对免疫系统的负面影响已得到广泛研究,在免疫治疗疗效背景下是一个有趣的因素。
在本研究中,我们报告了一项转化项目的结局,该项目旨在探索STK11基因在不同关键突变和治疗下的预后作用。
研究方法
研究人群为患有晚期、非癌基因成瘾(无EGFR、ALK、ROS1或RET变异)、非鳞状NSCLC且接受一线基于免疫的治疗(免疫单药或联合化疗)的患者。根据临床实践,所有患者均在诊断时接受NGS检测(Oncomine Focus Assay,52基因)。使用实验室开发的NGS panel,在内部队列中对存档肿瘤组织进行额外的基因突变分析,分析15个基因(BRAF、CDH1、CDK4、CTNNA1、HRAS、KEAP1、KRAS、MITF、NRAS、PTPN11、SMARCA4、SMARCB1、SMARCE1、STK11和TP53)的整个编码区(CDS)或热点区域。本研究的主要目的是根据关键的共突变(如KRAS、KEAP1、TP53和SMARCA4),确定STK11的预后作用。为了确定共突变的预后意义,我们使用从OAK/POPLAR随机试验数据集中提取的临床和基于血液的NGS数据,进行了一项外部验证研究。验证队列纳入了接受多西他赛或阿替利珠单抗治疗的晚期非鳞状NSCLC患者。
研究结果
内部队列
内部队列纳入了145例接受一线基于ICI治疗方案的患者。男性(59.7%)、既往吸烟者(90.3%)、ECOG PS为0 - 1(84%)、接受了CT - ICI治疗(58.6%)的患者占比较高(表1)。50.3%(n = 73)的患者存在TP53突变,44.8%(n = 65)存在KRAS突变,21.4%(n = 31)存在KEAP1突变,14.4%(n = 21)存在STK11突变,13.1%(n = 19)存在SMARCA4突变。
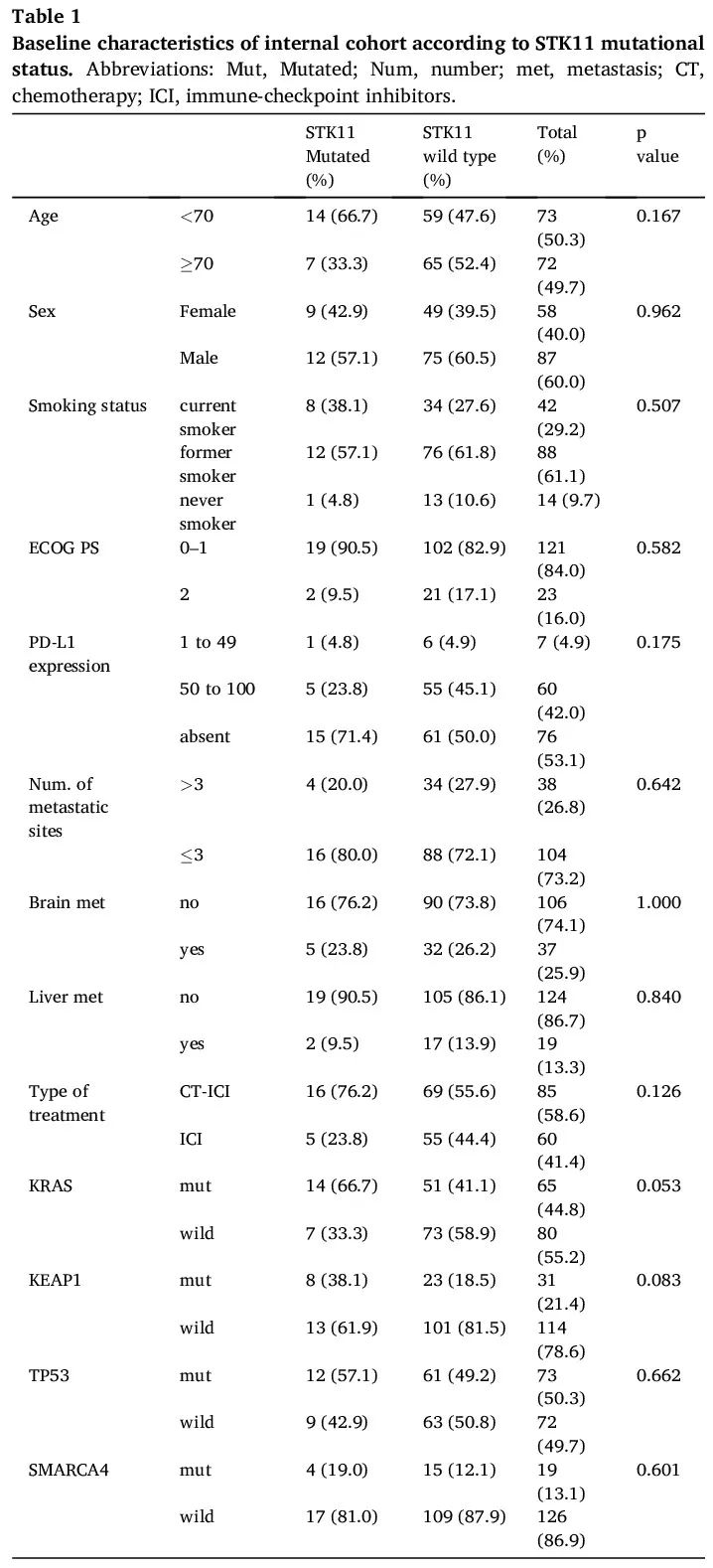
表1
除了KRAS共突变趋势(14/21,p = 0.053)外,没有其他基线特征与STK11突变相关(表1)。KRAS突变与女性性别(p = 0.004)、吸烟习惯(p = 0.03)以及TP53共突变(p = 0.038)相关。在KRAS突变患者中,p.G12C是最常见的亚型(40%,n = 26/65),其次是p.G12V(23%,n = 15/65)和p.G12A(13.8%,n = 9/65)。
在整个队列中,中位OS为13.2个月(95% CI,8.6 - 19.6),中位PFS为6.5个月(95% CI,4.8 - 8.9)。中位随访时间为27.7个月(IQR 21.1 - 36.0)。
STK11突变患者的中位OS为8个月(95% CI,5 - 16.7),而STK11野生型患者为17.3个月(95% CI,8.9 - 24.4)(p = 0.038)(图1)。STK11突变与较差的PFS无关(6.4个月 vs 6.5个月,p = 0.1)(图2)。
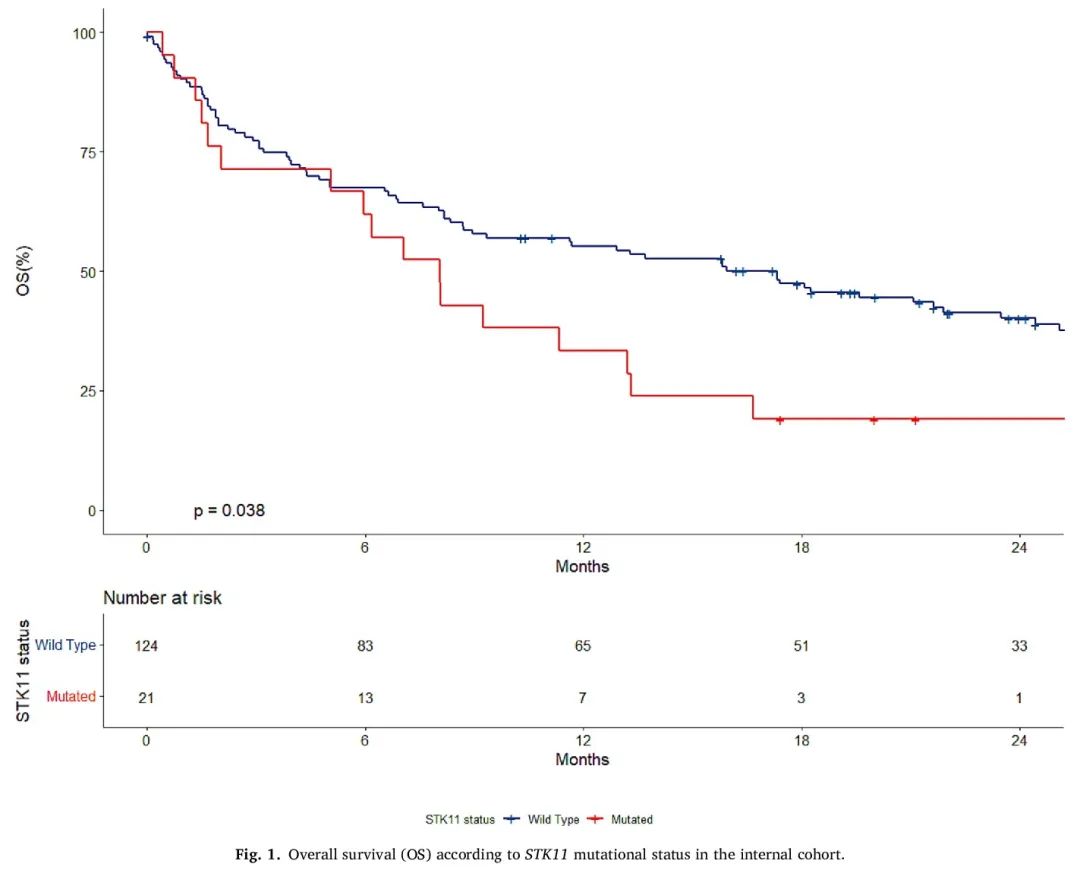
图1
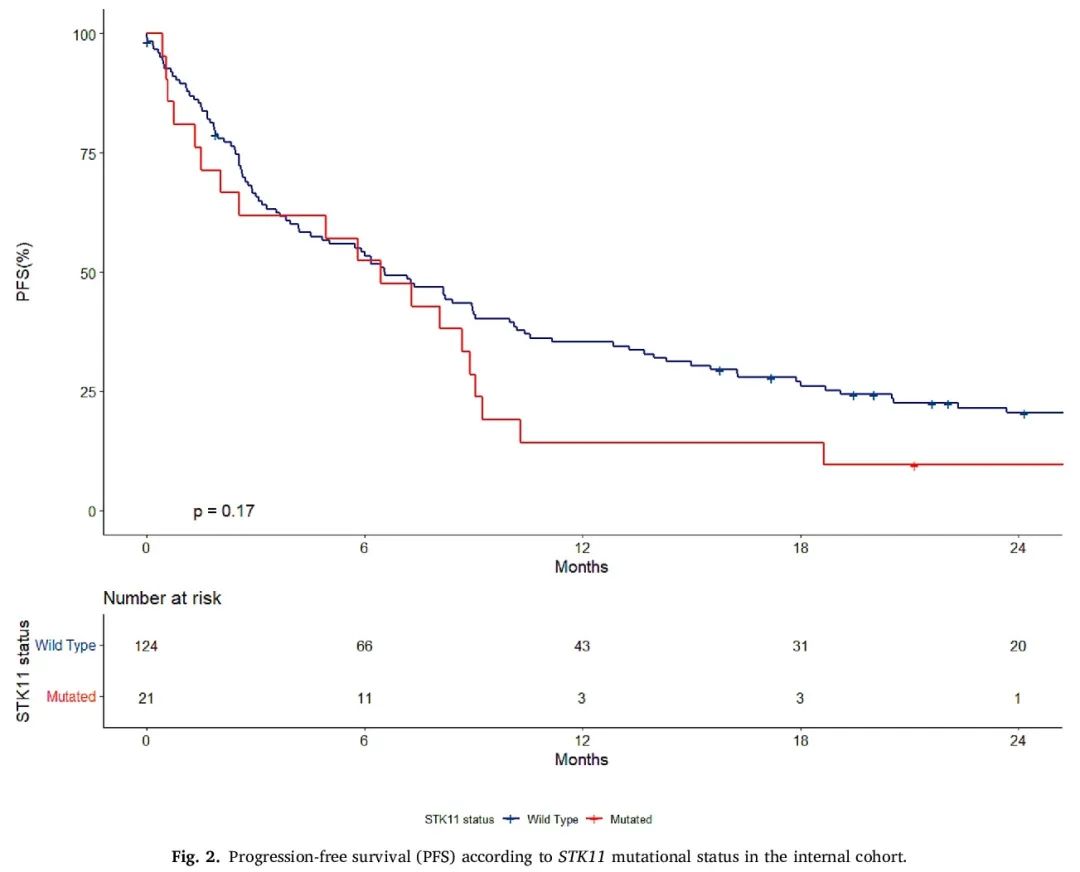
图2
携带KRAS(9.2个月 vs 15.9个月,p = 0.27)、TP53(8.3个月 vs 17.3个月,P = 0.2)和KEAP1(8.9个月 vs 15.9个月,P = 0.2)突变的患者,OS有较短的趋势,但差异无统计学意义。单变量(HR 1.74,95%CI,1.02 - 2.97,p = 0.041)和校正性别、年龄、ECOG PS评分、治疗方式(ICI vs CT - ICI)、KRAS、KEAP1、TP53和SMARCA4状态后的多变量模型(HR 1.97,P = 0.025)显示,STK11突变与较差的OS相关。在同一模型中,ECOG PS预测死亡风险增加(多变量HR 2.82,95%CI,1.67 - 4.75,p < 0.001)(表2)。

表2
关于PFS回归分析,单变量(HR 2.15,95%CI,1.34 - 3.45,p = 0.001)和多变量模型(HR 2.46,95%CI,1.50 - 4.05)显示,ECOG PS是唯一预测进展风险增加的预后因素。值得注意的是,在我们的队列中,基因变异对中位进展风险没有影响(表2)。
验证队列
验证队列包括818例患者。7.3%的患者存在STK11突变,7.9%存在KRAS突变,32.2%存在TP53突变,11%存在KEAP1突变,7.6%存在SMARCA4突变。STK11突变的存在与肿瘤突变负荷(TMB)>16 mut/mb(43% vs STK11野生型中22.7%,p = 0.001)、KEAP1共突变(41.7% vs STK11野生型中8.6%,p < 0.001)和SMARCA4共突变(18.3% vs STK11野生型中6.7%,P = 0.003)的比例较高相关。值得注意的是,KRAS(p = 0.002)、TP53(p < 0.001)、KEAP1(p < 0.001)和SMARCA4(p < 0.001)突变患者更常出现TMB >16 mut/mb。在该队列中,未包括KRAS p.G12C突变的患者。最常见的KRAS亚型是p.G12V(41.5%,n = 27/65),其次是p.G61X(16.9%,n = 11/65)。KRAS与TP53(47.7% vs KRAS野生型中30.8%,p = 0.008)和SMARCA4(15.4% vs KRAS野生型中6.9%,p = 0.025)显著共突变。
该队列的中位OS为12.7个月(95% CI,11.7 - 14.1),中位PFS为3.3个月(95% CI,2.8 - 4.0)。STK11突变患者的中位OS为6.4个月(95% CI,4.8 - 9.7),而STK11野生型患者为17.3个月(95% CI,12 - 14.5)(p < 0.0001)(图3)。STK11野生型患者的中位PFS为3.9个月(95% CI,2.9 - 4.1),而STK11突变患者为1.5个月(95% CI,1.4 - 2.8)(p = 0.0041)(图4)。
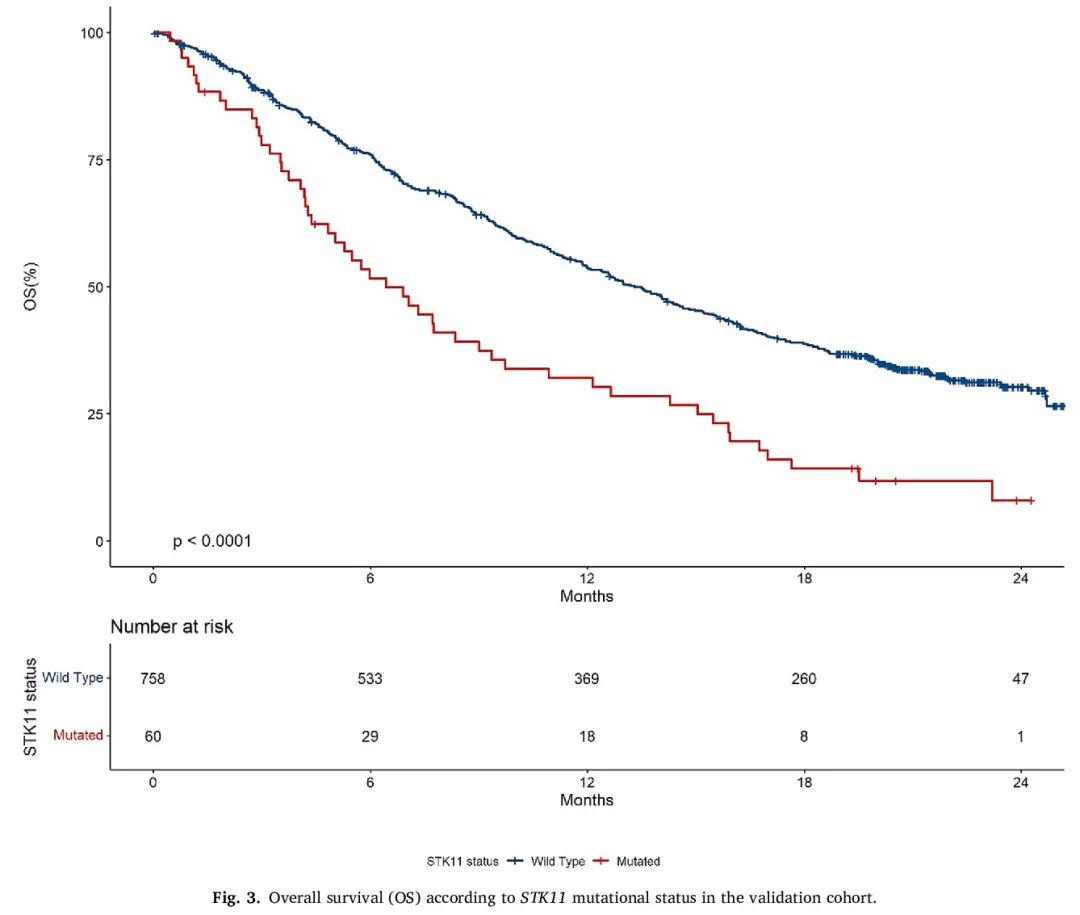
图3
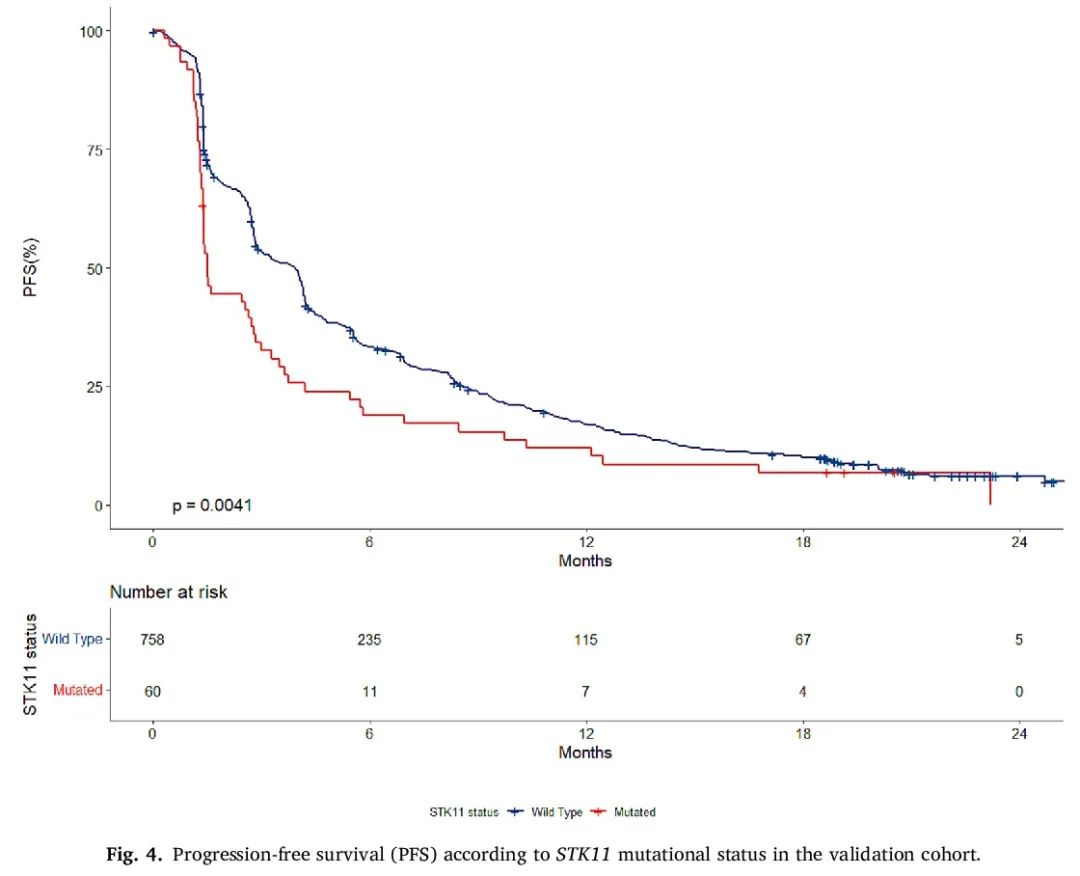
图4
校正性别、年龄、治疗类型(CT vs ICI)和共突变状态后的多变量模型显示,KRAS(HR 1.55,p = 0.004)、STK11(HR 1.65,p = 0.001)和KEAP1(HR 1.74,p < 0.001)突变独立增加死亡风险。在同一模型中,转移部位超过3个与死亡风险独立相关(多变量HR 1.79,p < 0.001)。
在单变量(HR 1.55,p < 0.001和HR 1.64,p > 0.001)和校正性别、年龄、治疗类型(IO vs CT)、KRAS、STK11、TP53和SMARCA4突变状态后的多变量模型(HR 1.50,p < 0.001)中,转移部位数量(>3个)和KEAP1突变与较差的PFS相关。在同一模型中,TP53和STK11变异在单变量模型中预测进展风险增加,但在多变量模型中不是如此。
讨 论
在这项单中心转化研究中,我们致力于分析非癌基因成瘾晚期NSCLC患者的基因组构成。通过将基线NGS分析与实验室开发的panel相结合,我们确定了STK11突变的不良预后价值,无论其他关键基因(KRAS、KEAP1、TP53、SMARCA4)突变状态、治疗类型和线数如何。这一结果在随机对照研究的验证队列中得到了证实。
随着多种预测性生物标志物的出现,对NSCLC患者进行广泛的基因检测变得很有必要,对于晚期患者,诊断时几种基因变异检测被认为是必需的。
癌症组织是进行分子检测的最佳标本,尽管在晚期NSCLC诊断的临床实践中,经常遇到小活检样本或细胞学样本。NGS是一种分子检测方法,可同时分析不同患者的多种生物标志物。市面上有多种商业化panel可供选择,包括小panel(10 - 15个基因)、中panel(多达50个基因)、肿瘤大panel(多达150个基因)以及人类癌症综合panel(多达400个基因)。然而,分子检测的应用率并不理想,近期一项国际调查显示,确诊时实际接受检测的患者不足三分之二。分子检测覆盖率不理想,可能是由于成本、检测周转时间较长、技术可及性以及专科医生认知不足等原因导致的。
在我们的回顾性内部队列中,接受一线免疫治疗或免疫联合化疗的KRAS突变患者生存结局有较差的趋势。在验证队列中,KRAS突变与较差的OS独立相关,无论治疗(ICI vs CT)、其他临床变量和基因组特征如何。
一项系统综述和荟萃分析纳入了25项随机对照试验,评估与免疫治疗或免疫联合化疗疗效相关的预后因素。值得注意的是,与化疗相比,免疫联合化疗时KRAS突变与OS改善相关,尽管通过荟萃回归间接比较免疫治疗和免疫联合化疗时未发现差异。
如前所述,关键基因与KRAS的共突变可能会影响生存结局。值得注意的是,我们的回顾性研究在内部队列和验证队列中证实了STK11突变的不良预后作用,无论治疗类型(ICI、ICI - CT、CT)和共突变(KRAS、KEAP1、SMARCA4、TP53)如何。
STK11失活导致KRAS阳性肺腺癌的一种特殊亚型,其特征为“冷”肿瘤微环境和低PD - L1表达。在KRAS突变晚期NSCLC临床环境中,STK11共突变显著影响生存结局和单药ICI治疗的抗肿瘤疗效。有趣的是,一项双中心队列研究纳入了1261例接受ICI治疗的晚期肺腺癌患者。该队列中,STK11和KEAP1突变与较差的PFS和OS相关。这一数据在KRAS突变患者中但未在KRAS野生型人群中得到证实,提示可能与KRAS突变状态有关。研究者发现,不同KRAS突变状态的STK11和KEAP1突变NSCLC表现出不同的转录组特征和肿瘤微环境浸润。相反,我们的数据表明了STK11突变的独立不良预后影响。
越来越多的证据表明,在免疫治疗中,不同类型的STK11突变可能具有不同的预后影响。具体而言,多项研究指出,在接受免疫治疗的NSCLC中,并非所有STK11突变亚型都与不良结局相关。在我们的队列中,STK11突变主要为截断、移码或错义突变,根据Varsome工具,这些突变通常被认为具有致病性。然而,由于样本量的限制,无法进一步进行亚型特异性分析,这为未来研究提供了一个有趣的方向。Boeschen等人对公开数据集进行了全面的生物信息学分析,旨在评估KRAS、STK11和KEAP1突变作为三重、双重或单基因突变的预后价值。在比例风险模型中,携带STK11 + KEAP1或KRAS + KEAP1三重突变的患者OS显著较短,该模型还包括了其他突变组合或单基因突变。值得注意的是,对生存的影响与免疫治疗无关,强调了这些基因突变的预后而非预测价值。上述证据支持我们的研究结果,即携带STK11、KEAP1、KRAS或TP53突变的肿瘤具有更高的生物学侵袭性和不良预后,无论治疗方案如何。
随着抗KRAS p.G12C靶向疗法的出现,这些数据需要重新分析。2期CodeBreak100试验探索了索托雷塞(Sotorasib)在经治KRAS G12C突变患者中的疗效。在一项仅描述性的探索性分析中,评估了STK11、KEAP1和TP53突变对抗肿瘤活性的影响。结果发现,各分子亚组均有抗肿瘤活性,尽管KEAP1改变的存在似乎会降低ORR。
类似地,KRISTAL1试验表明了KRAS G12C抑制剂阿达格拉西布(Adagrasib)的有效性。探索性生物标志物评估显示,KEAP1突变但STK11野生型的患者,其抗肿瘤反应受到负面影响。值得注意的是,上述前瞻性试验均未提供推断性分析。一项多中心观察性研究评估了105例接受索托拉西布治疗的KRAS G12C突变晚期NSCLC患者的临床结局。KEAP1共突变的存在与PFS和OS显著缩短相关。然而,在该队列中,STK11突变未对生存结局产生影响。这些发现表明,在STK11共突变疾病中,KRAS抑制剂单独使用或与其他治疗方法(如ICI或化疗)联合使用可能有效。
最后,有限的病例数据表明,免疫治疗下,SMARCA4缺陷与不良预后相关,尽管其他研究未发现显著影响。在我们的回顾性队列中,未发现SMARCA4缺陷对预后有影响,无论内部和验证队列亚接受何种治疗。
本研究存在一些值得讨论的局限性。首先,整体样本量有限(内部队列有145例患者)。使用OAK/POPLAR数据集使我们能够探索关键突变的预后价值而非预测价值,但需要强调的是,不同的治疗环境(一线vs后线治疗)和NGS方法(组织vs液体活检)可能会限制两个队列之间的可比性。需要注意的是,验证队列中液体活检的应用可能存在一定偏差,尤其是癌症预后较差可能导致ctDNA脱落增加。此外,OAK/POPLAR数据集未包括KRAS p.G12C突变患者,这降低了研究结果对KRAS阳性患者的外部有效性。
最后,数据收集不完整,且影像学评估和评价依赖医生判断,本研究的回顾性性质也构成了另一个局限性。
尽管如此,我们的项目具有优点,作为一项独立的学术转化项目,旨在改善非癌基因成瘾晚期NSCLC的基因检测,关注了STK11突变疾病。据我们所知,本研究首次探索了STK11突变对预后的影响,无论KRAS、KEAP1、TP53和SMARCA4状态如何。
总之,在日常临床实践中,采用个性化的基因检测方法,可能提高预后预测的准确性。值得注意的是,在选择包含致癌驱动突变的NGS小panel时,也应纳入KEAP1、STK11和TP53等临床相关突变。
参考文献:
Andrea De Giglio, Dario De Biase, Valentina Favorito, Thais Maloberti, Alessandro Di Federico, Federico Zacchini, Giulia Venturi, Claudia Parisi, Filippo Gustavo Dall’Olio, Ilaria Ricciotti, Ambrogio Gagliano, Barbara Melotti, Francesca Sperandi, Annalisa Altimari, Elisa Gruppioni, Giovanni Tallini, Francesco Gelsomino, Lorenzo Montanaro, Andrea Ardizzoni, STK11 mutations correlate with poor prognosis for advanced NSCLC treated with first-line immunotherapy or chemo-immunotherapy according to KRAS, TP53, KEAP1, and SMARCA4 status, Lung Cancer, Volume 199, 2025, 108058, ISSN 0169-5002, https://doi.org/10.1016/j.lungcan.2024.108058.



