华南理工大学附属第二医院杨蕊梦/袁友永团队Biomaterials:免疫/代谢双调控的胞外靶点纳米递药体系助力胶质瘤免疫治疗
时间:2025-03-05 12:09:15 热度:37.1℃ 作者:网络
肿瘤发生免疫原性细胞死亡(ICD)过程中会释放大量ATP,经胞外核苷酶代谢后生成腺苷(ADO)。ADO与免疫细胞表面广泛分布的2A型腺苷受体(A2AR)结合后,介导肿瘤免疫抑制。为了解决这一挑战,华南理工大学附属第二医院杨蕊梦教授和袁友永教授提出了一种基于免疫/代谢双调控的胞外靶点纳米递药体系,旨在通过阻断CXCL12/CXCR4和腺苷/A2AR信号轴,在提高肿瘤免疫原性的同时,缓解免疫抑制微环境,为肿瘤免疫治疗提供了一种双管齐下的策略。此外,本研究开发了一种胞外靶点药物递送策略,利用肿瘤微环境响应性生物正交原位组装的纳米载体递送免疫调节药物,解决了传统胞内递药策略制约膜上靶点药物在胞外发挥作用的难题。
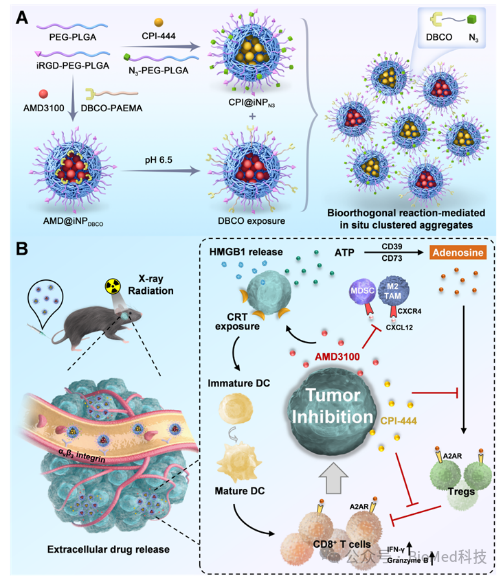
图1.(A)肿瘤酸度响应和生物正交反应介导的肿瘤原位组装纳米体系合成示意图。(B)通过靶向阻断CXCL12/CXCR4和腺苷/A2AR轴协同增强胶质瘤免疫治疗。
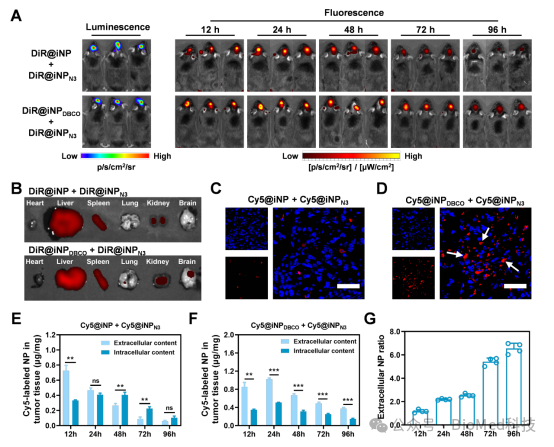
图2.原位组装纳米体系的脑肿瘤靶向与胞外释放药物
该原位组装纳米体系DiR@iNPDBCO + DiR@iNPN3在原位脑肿瘤部位的富集时间长达96小时,且肿瘤组织细胞外的纳米颗粒水平始终高于细胞内水平,表明该体系具有优异的肿瘤靶向和胞外药物释放能力。
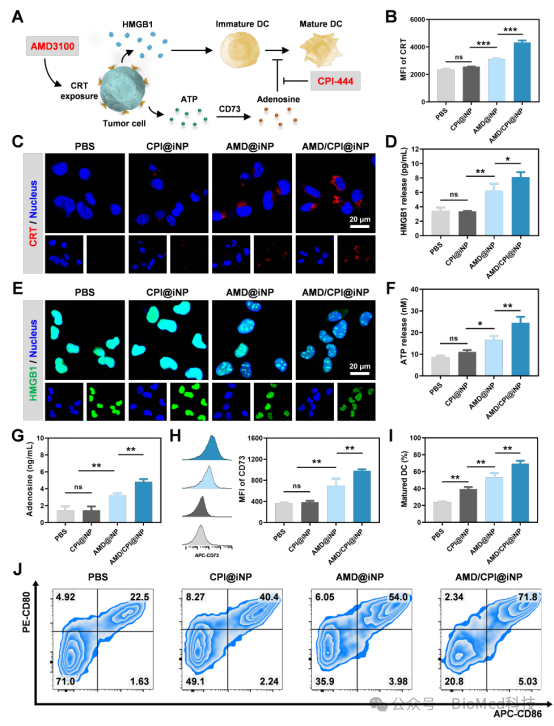
图3.原位组装纳米体系的体外ICD效应
体外细胞实验表明,CXCR4拮抗剂AMD3100与A2AR拮抗剂CPI-444联合使用可显著诱导肿瘤细胞发生ICD,表现为钙网蛋白(CRT)的外翻、高迁移率组蛋白1(HMGB1)的释放以及ATP等损伤相关分子模式(DAMPs)的分泌,进而有效促进树突状细胞(DCs)成熟,激活抗肿瘤免疫反应。
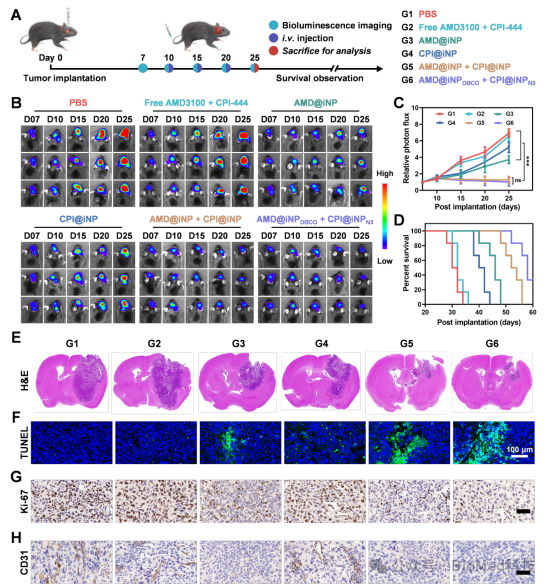
图4. 体内抗肿瘤实验
本研究评估了原位组装体系在原位胶质瘤小鼠模型中的抗肿瘤效果。结果显示,AMD@iNPDBCO + CPI@iNPN3展现出最佳的肿瘤抑制效果。H&E和TUNEL染色结果证实了其优异的肿瘤杀伤能力。此外,治疗期间小鼠体重无显著下降,主要脏器H&E染色和血生化检测未见异常,表明该纳米递药体系具有良好的体内安全性。流式分析显示,原位组装体系显著增加了肿瘤中CD8⁺T细胞的比例,减少了免疫抑制性细胞(M2型TAMs、MDSCs、Tregs)的瘤内浸润。结果表明,基于阻断CXCL12/CXCR4和腺苷/A2AR信号轴的原位组装纳米体系显著增强抗肿瘤免疫反应,为癌症免疫治疗提供了新策略。
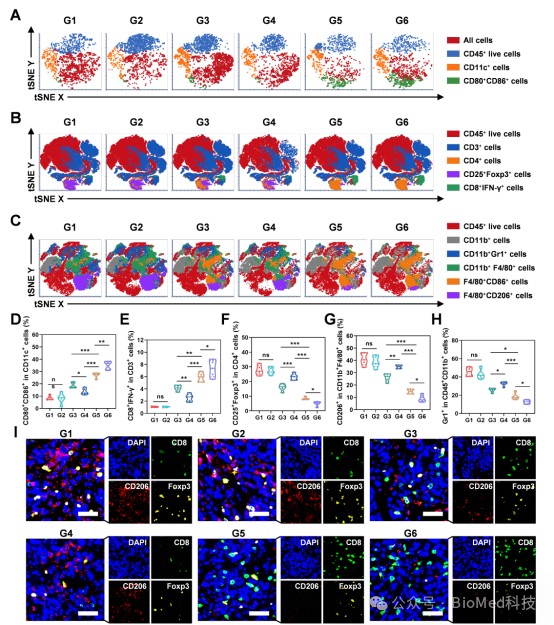
图5. 肿瘤免疫微环境的分析
研究还评估了该体系对胶质瘤放疗的增敏效果。与单独放疗组相比,放疗联合AMD@iNPDBCO+CPI@iNPN3治疗组显著抑制了肿瘤生长,促进了DCs成熟,并激活效应CD8⁺T细胞分泌细胞因子IFN-γ和颗粒酶B,从而延长了原位胶质瘤荷瘤小鼠的生存期。此外,该体系通过减少前体耗竭CD8⁺ T细胞向终末期耗竭CD8⁺T细胞的分化,显著增强了免疫检查点PD-1抗体的治疗效果,为放疗和免疫检查点阻断疗法的协同增效提供了新思路。
【全文总结】
本研究设计了一种肿瘤酸度和生物正交化学介导肿瘤原位尺寸转变的纳米递送体系,通过肿瘤原位生物正交反应,从而形成微米级大小的药物库以增强药物滞留和富集。颗粒间发生原位组装形成大尺寸聚集体更容易避免被肿瘤及相关免疫细胞摄取,有利于细胞膜上靶点免疫治疗药物发挥效能。所释放的CXCR4拮抗剂诱导肿瘤发生ICD,激活机体的肿瘤特异性细胞免疫,而腺苷受体抑制剂CPI444通过有效拮抗各种免疫细胞表面的A2AR,缓解腺苷代谢途径介导的免疫抑制,通过免疫/代谢双调节最终实现强大的抗肿瘤免疫应答。本研究尝试将该策略应用于放疗与免疫检查点阻断的联合治疗,展现出更强的抗肿瘤效果。
华南理工大学附属第二医院(广州市第一人民医院)杨蕊梦教授和华南理工大学生物医学科学与工程学院袁友永教授为该论文的共同通讯作者,华南理工大学博士研究生韦瑞丽、谢坤锋、李涛为本论文的共同第一作者。本研究受到国家自然科学基金等项目资助。
原文链接:
https://www.sciencedirect.com/science/article/pii/S0142961225001358


