变异等位基因频率与AML治疗结局的预后相关性分析
时间:2025-04-01 12:11:15 热度:37.1℃ 作者:网络
变异等位基因频率
急性髓系白血病(AML)是一种在细胞遗传学和分子生物学方面具有异质性的疾病,这些特征可用于预后分层和确定治疗靶点。有研究表明,某些基因(如EZH2、SRSF2、TP53)的诊断时高突变等位基因频率(VAF)对AML的预后有负面影响。其中研究最多的基因是TP53;诊断时不同的VAF阈值(即10%或40%)可能对患者的预后产生影响。
尽管根据VAF,突变负担与患者预后有关,但该参数尚未很好地确定用于风险分层。因此学者开展大型流行病学登记组研究,旨在分析通过NGS检测到的基因变异的突变负荷对AML患者治疗结局的影响,重点关注总生存期(OS)。研究近日发表于《Haematologica》。

研究结果
研究设计:该研究是一项非干预性、系统性、回顾性的病历审查研究,纳入2003年至2021年间诊断的3018例成人AML患者,均接受了NGS检测。
患者分组:患者根据一线治疗方案被分为接受强化疗(IC)、非强化疗(non-IC,如去甲基化药物方案)或低剂量阿糖胞苷(LDAC)治疗的组别。
基因检测:使用NGS技术检测与诊断、预后和治疗选择相关的基因突变,包括ASXL1、BCOR、CEBPA、EZH2、FLT3、IDH1、IDH2、NPM1、RUNX1、SF3B1、SRSF2、STAG2、U2AF1、ZRSR2和TP53等。
统计分析:使用SPSS和Stata软件进行统计分析,重点关注VAF作为连续变量的影响。采用Cox比例风险模型评估变量与患者无病生存期(LFS)和OS的关联。使用混合效应回归模型来考虑患者异质性。
患者特征:共纳入3018例成人AML患者,其中2464例在初诊时获得样本,554例在复发难治时获得样本。最常突变的基因是DNMT3A(24.3%),其次是NPM1(22.5%)、TET2(21.2%)和RUNX1(18.8%)。
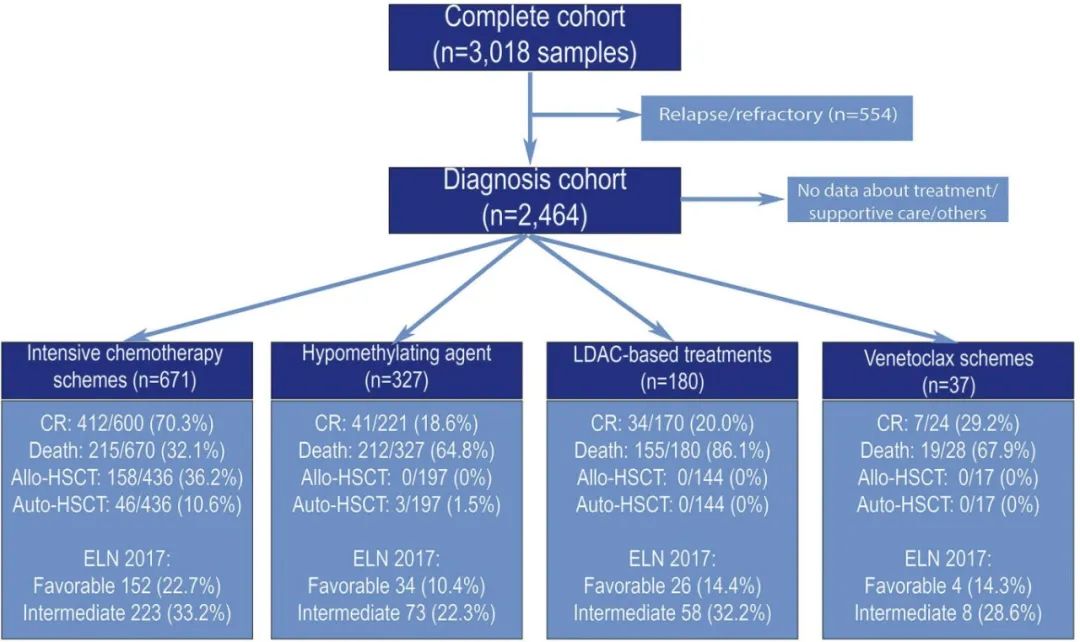
初诊组:中位年龄为67岁,55.6%接受强化疗,27.1%接受去甲基化治疗,14.9%接受LDAC治疗。强化疗组70.3%获得CR,36.2%接受了移植。中位OS为12.6个月,中位LFS为10.1个月。
对CR的影响:高龄(OR 0.935,p<0.001)和SRSF2基因突变高负荷(OR 0.978,p<0.001)与达到CR的可能性较低相关,而NPM1基因突变高负荷(OR 1.025,p<0.001)与达到CR的可能性较高相关。
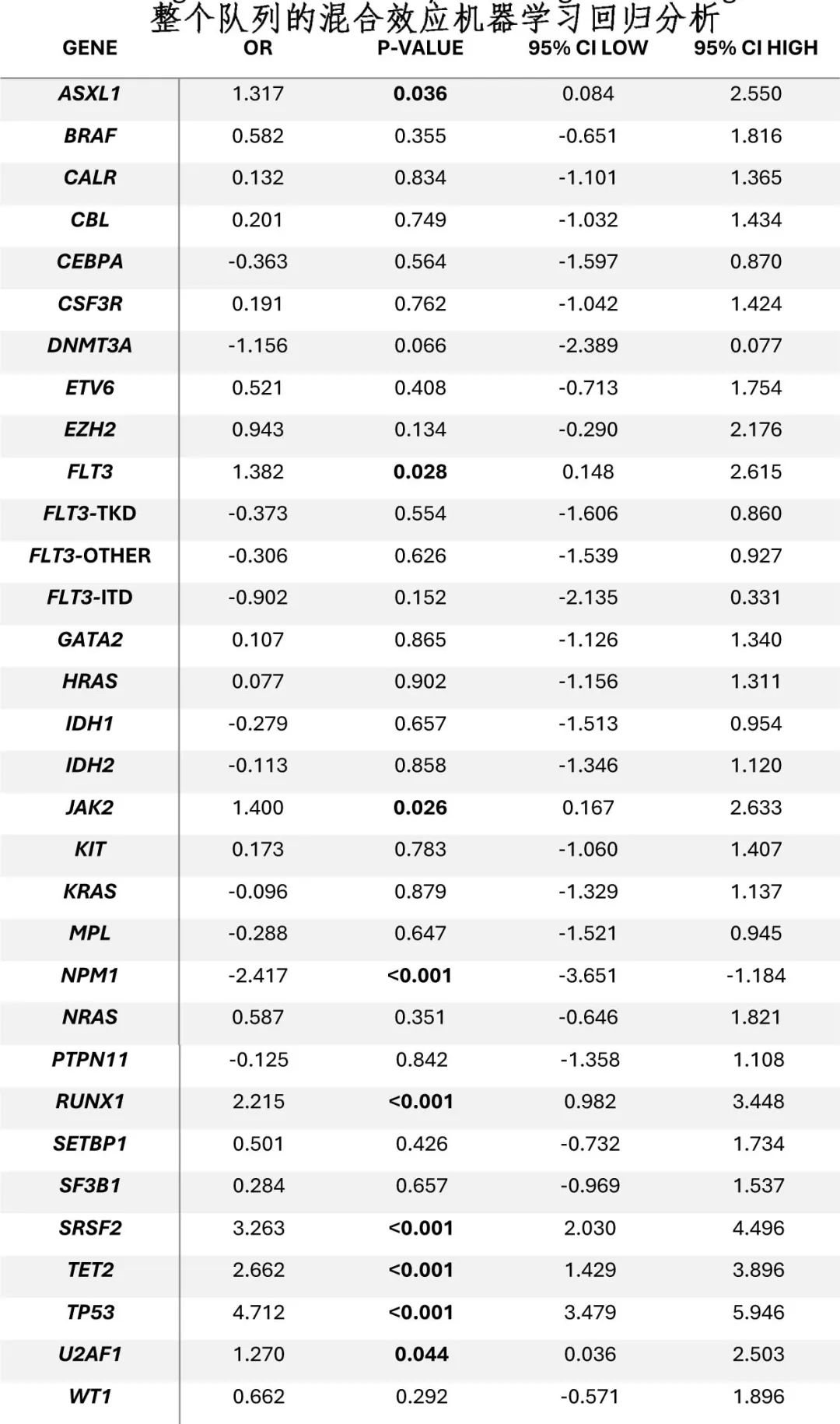
混合效应机器学习回归分析:ASXL1 (OR 1.317,p=0.036)、FLT3 (OR 1.382,p=0.028)、JAK2 (OR 1.400,p=0.026)、RUNX1 (OR 2.215,p<0.001)、SRSF2 (OR 3.263,p<0.001)、TET2 (OR 2.662,p<0.001)、TP53 (OR 4.712,p<0.012)和U2AF1 (OR 1.270,p=0.044)的高等位基因负荷与OS不良预后相关;但NPM1负荷增加带来良好预后(OR 2.417,p<0.001)。该模型对LFS的影响不显著。
VAF cutoff值对OS的影响:随后定义突变的VAF cutoff值,分别为ASXL1(0.475)、JAK2 (0.038)、RUNX1(0.043)、SRSF2(0.028)、TET2(0.030)和TP53(0.024)。所有基因的低VAF与较好的OS相关(ASXL1:低VAF vs高VAF,15.84 vs 13.51个月,p=0.025;JAK2: 15.87 vs. 10.10个月,p<0.001;SRSF2: 16.16 vs. 12.49个月,p<0.001;TET2: 17.02月vs. 10.69月,p<0.001;TP53: 17.21个月 vs 6.95个月,p<0.001),但RUNX1无统计学意义(15.41个月vs 16.03个月,p=0.789)。
不同治疗亚组的影响:
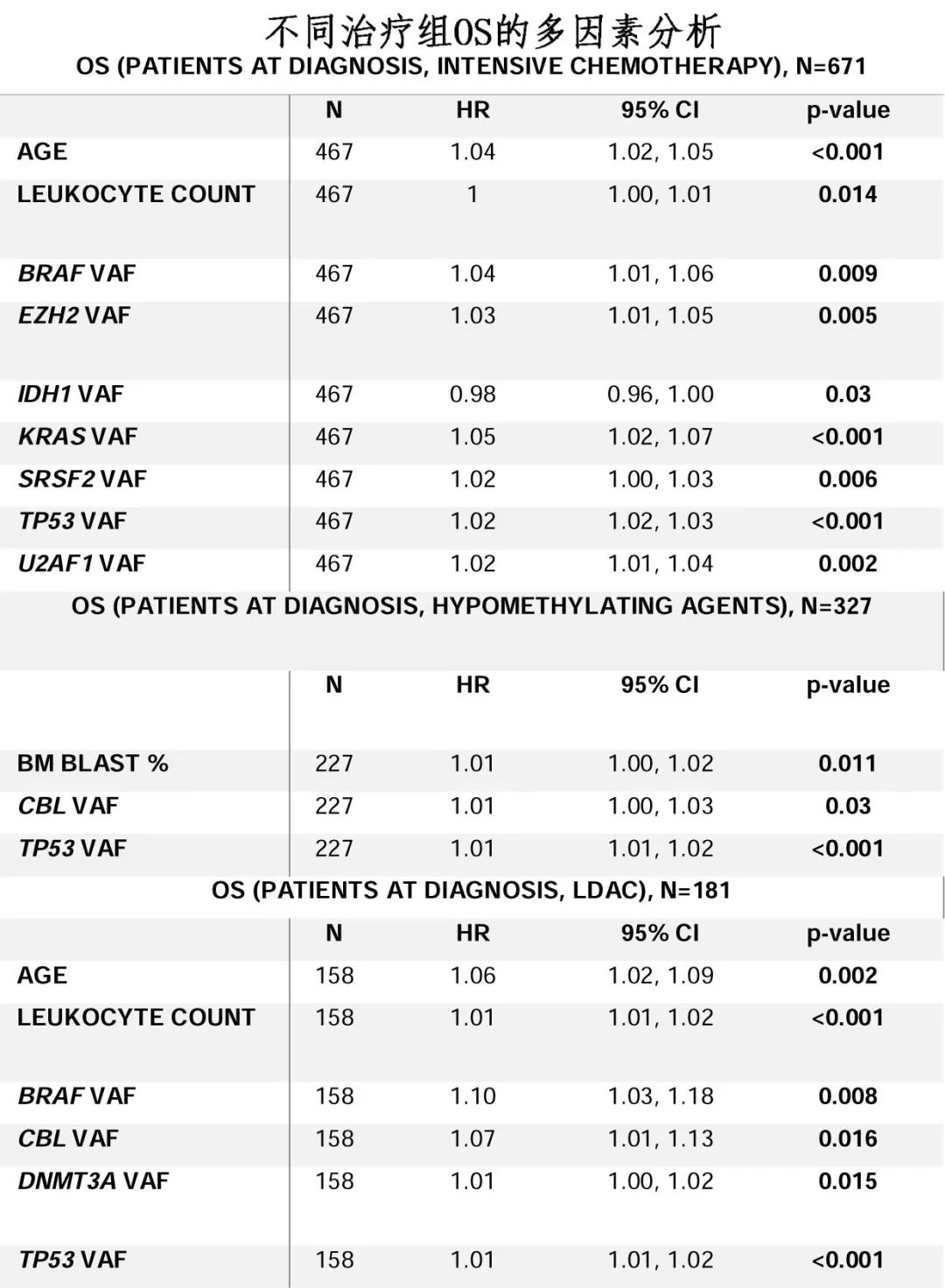
强化治疗组:突变负荷增加1%对强化方案治疗的OS和LFS的影响。BRAF (HR 1.04, p=0.009)、EZH2 (HR 1.03, p=0.005)、KRAS (HR 1.05, p<0.001)、SRSF2 (HR 1.02, p=0.006)、TP53 (HR 1.02, p<0.001)和U2AF1 (HR 1.02, p=0.009)较高的VAF与较差的OS相关,IDH1较高的VAF与较好的OS相关(HR 0.98, p=0.03)。ASXL1(HR 1.02, p=0.016)和CALR (HR 1.02, p=0.033) 高VAF的LFS较差,而IDH2高VAF的LFS较好(HR 0.98, p=0.033)。EZH2为转录调控基因,U2AF1为剪接因子基因;两者都与发育不良有关,并被列入ELN2022分类中的不良风险类别。该研究首次报道高U2AF1 VAF与较差预后之间的关系,既往也没有研究表明高CALR VAF患者有更差的OS或LFS,后者可能与慢性骨髓增殖性肿瘤继发的急性白血病有关,其预后劣于de novo AML。
LDAC组:高龄(HR 1.06, p=0.002)、高白细胞计数(HR 1.01, p<0.001)以及BRAF (HR 1.10, p=0.008)、CBL (HR 1.07, p=0.016)、DNMT3A (HR 1.01, p=0.015)和TP53 (HR 1.01, p<0.001)的高VAF与不良OS相关。未检测到剪接因子对OS有影响
去甲基化药物组:CBL(HR 1.01, p=0.03)和TP53(HR 1.01, p<0.001)的高VAF为OS的不良危险因素。未发现表观遗传因素对预后有影响。
总体而言,TP53 VAF对整体人群和三个治疗亚组的OS均有不良影响。
总结
主要发现:某些信号传导(FLT3、JAK2)、转录因子(RUNX1)、表观遗传(ASXL1、TET2)和剪接因子(SRSF2和U2AF1)基因以及TP53的突变等位基因频率增加,会恶化AML患者的OS。研究还确定了每个基因的具体预后cutoff值。
临床应用:该研究有助于在临床实践中更好地评估AML患者的预后,并可能指导治疗决策。未来也需要更多研究来确认这些结果,并进一步确定VAF在AML患者中的预后或预测价值。
参考文献
Rafael Colmenares, Noemi Alvarez, Eva Barragán, Blanca Boluda, María J. Larráyoz, María Carmen Chillón, Elena Soria-Saldise, Cristina Bilbao, Joaquín Sanchez-García, Teresa Bernal, David Martinez-Cuadron, Cristina Gil, Josefina Serrano, Carlos Rodriguez-Medina, Juan Bergua, José A. Pérez-Simón, María Calbacho, Juan M. Alonso-Domínguez, Jorge Labrador, Mar Tormo, Pilar Herrera-Puente, Cristina Martín-Arriscado, Andrés Arroyo-Barea, Inmaculada Rapado, Claudia Sargas, Iria Vazquez, María J. Calasanz, Teresa Gomez-Casares, Ramón García-Sanz, Rebeca Rodríguez-Veiga, Joaquín Martinez-Lopez, Rosa Ayala, and Pau Montesinos.Collaborative Groups: PETHEMA Group. Prognostic relevance of variant allelic frequency for treatment outcomes in patients with acute myeloid leukemia: a study by the Spanish PETHEMA registry.Haematologica. 2025 Feb 27. doi: 10.3324/haematol.2024.286311


