好文推荐 | 女性帕金森病患者异动症临床特征和危险因素分析
时间:2025-04-03 12:10:30 热度:37.1℃ 作者:网络
摘要
目的 调查女性帕金森病(PD)患者异动症的临床特征和相关危险因素。方法 采用横断面研究方法,连续收集航天中心医院PD专病门诊符合PD诊断标准的女性患者病例资料,记录一般人口学资料和临床特征数据:左旋多巴等效剂量(LEDD)、UPDRS-Ⅲ、UPDRS-Ⅳ及认知、抑郁等非运动症状评分、是否合并异动症、发生异动症单次左旋多巴剂量(LD),进行组间比较,采用二元Logistic回归分析女性PD患者异动症的影响因素。结果 共收集146例女性PD患者,出现异动症30例,发生率20.5%;异动症组与无异动症组临床特征比较,异动症组发病年龄更早[(54.3±12.5)岁 vs (62.7±10.0)岁, P<0.001]、病程更长[(9.9±3.7)年 vs (4.5±3.7)年, P<0.001]、病情更重[H-Y分期(2.65±0.58) vs (2.35±0.83), P=0.03]、LD服用时间更长[(7.5±3.2)年 vs (3.2±2.6)年, P<0.001]、LEDD更高[(703.2±203.9) mg vs (442.1±226.3) mg, P<0.001]、体重更低[(54.1±8.2) kg vs (60.0±8.7) kg, P=0.001]、BMI更低[(20.9±3.1) kg/m2 vs (23.4±3.1) kg/m2, P<0.001]。多因素Logistic回归分析,BMI高(OR=0.770, P=0.005)是女性PD患者发生异动症的保护因素,而病程长(OR=1.304, P=0.001)、LEDD高(OR=1.003, P=0.012)是女性患者出现异动症的危险因素。结论 女性PD患者有较高异动症的发生率,值得临床重视,高BMI是保护因素,病程长、LEDD高是其异动症发生的危险因素。
我国60岁以上人群中帕金森病(Parkinson disease,PD)患病率为1.37%,80岁以上人群患病率超过4%。运动并发症包括症状波动和异动症,与药物和疾病进展相关。左旋多巴(levodopa,LD)是治疗PD的主要药物之一,但长期服用会增加或诱发LD诱导的异动症(levodopa-induced dyskinesia,LID)。研究表明,异动症与性别、年龄、病程及LD应用等多种因素有关,故早期识别及了解可能危险因素对预防或延迟异动症的发生有重要的临床意义。本研究通过横断面调查本中心女性PD患者异动症的临床特征和影响因素,现报道如下。
1 资料与方法
1.1 研究对象
连续收集从2023年9月—2024年8月就诊于航天中心医院PD专病门诊的女性患者临床资料所有患者均符合PD诊断标准 (2016版)。
1.2 研究方法
采用横断面研究,记录女性PD患者一般人口学资料、临床特征,包括运动症状、非运动症状、是否合并异动症、发生异动症患者单次LD剂量等。分析女性PD患者出现异动症的临床特征和可能危险因素。一般人口学资料包括年龄、身高、体重、体重指数(body mass index,BMI)。
PD临床特征信息:(1)发病年龄、病程、计算患者每日左旋多巴等效剂量(levodopa equivalent daily doses,LEDD)、LD服用年限;(2)应用统一帕金森病评分量表第三部分(Unified Parkinson’s Disease Rating Scale-Ⅲ,UPDRS-Ⅲ)评价运动功能,Hoehn-Yahr分期(H-Y分期)评价病情严重程度;(3)应用UPDRS-Ⅳ评测患者是否存在异动症及评分,是否符合脆性左旋多巴(brittle response,BR);(4)应用非运动症状(Non-Motor Symptoms Scale, NMSS)筛查量表评价非运动症状;蒙特利尔认知评估量表(Montreal Cognitive Assessment,MoCA)量表、简易智力状态检查量表(Mini-Mental State Examination,MMSE)量表评价认知功能;汉密尔顿焦虑量表14(Hamilton Anxiety Rating Scale 14,HAMA-14)和HAMD-17评价焦虑和抑郁情绪。
1.3 统计学方法
使用SPSS 20.0软件分析,计量资料使用Kolmogorov-Smirnov检验进行正态性检验,对符合正态分布的计量资料以(x±s)表示,非正态分布的数据以中位数(百分位数间距)[M(P25,P75)]表示。计量资料的组间比较,符合正态分布的数据采用独立样本t检验,非正态分布数据使用非参数检验。计数资料和等级资料采用[n(%)]表示,组间比较采用χ2检验或Fisher精确检验。采用二元Logistic回归分析女性PD患者异动症的影响因素。采用双尾法,P<0.05为差异有统计学意义。
2 结 果
2.1 一般人口学资料
共收集女性PD患者146例,年龄(66.6±10.0)岁,发病年龄(61.1±11.1)岁,病程(5.6±4.3)年,体重(58.8±8.9) kg,BMI(22.9±3.3) kg/m2,H-Y分期(2.41±0.79),UPDRS-Ⅲ(35.2±17.1),LEDD(497.6±245.6) mg/d,LD服用时间(4.9±2.7)年(见表1)。
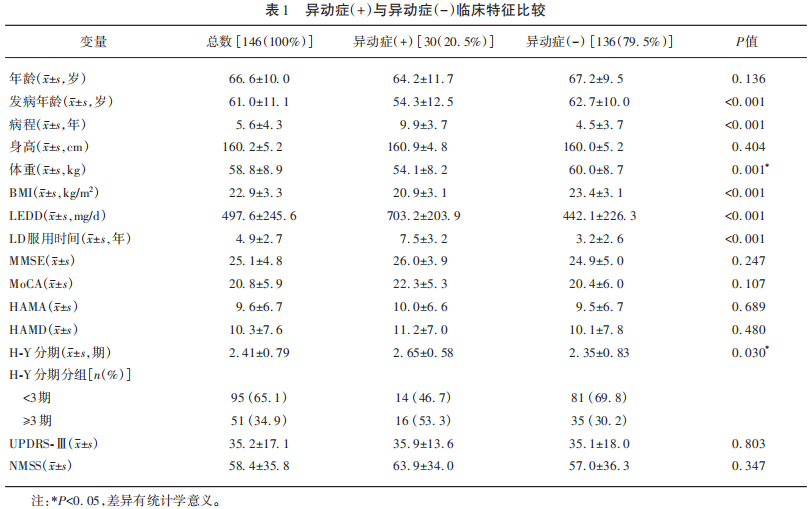
2.2 异动症组与无异动症组临床特征比较
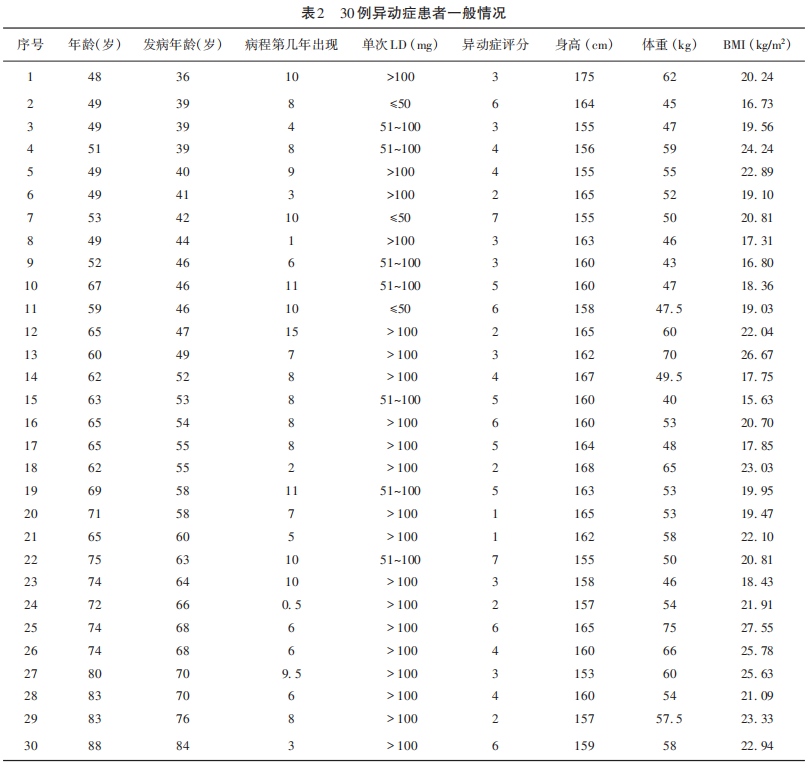
发生异动症30例,发生率20.5%,早发型13例(占早发型组52.0%)、晚发型17例(占晚发型组14.0%)。BR 10例(单次LD剂量≤100 mg出现致残性异动),占异动症33.3%,重度3例(单次LD剂量≤50 mg)、中度7例(单次LD剂量:51~100 mg)(见表2)。
异动症组年龄(64.2±11.7)岁、发病年龄(54.3±12.5)岁,最早出现在发病后0.5年,最晚发生在发病后第15年,平均病程(7.2±3.3)年,体重(54.1±8.2)kg,BMI (20.9±3.1) kg/m2,LEDD (497.6±245.6) mg/d(见表1)。
异动症(+)和异动症(-)比较,二组在发病年龄、病程、体重、BMI、LD服用时间、LEDD、H-Y分期方面差异有统计学意义(P<0.05)(见表1),提示异动症组发病年龄更早、体重和BMI更低、病程更长、LD服用时间更长、LEDD更大,但在认知障碍、NMSS、HAMA、HAMD等非运动症状及疾病严重程度方面无明显差异(P>0.05)。
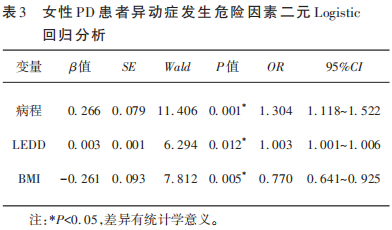
进一步以异动症为因变量,以发病年龄、病程、H-Y分期、BMI、LEDD为自变量进行多因素Logistic回归分析(见表3),结果提示BMI高(OR=0.770,P=0.005)是女性PD患者异动症的保护因素,而病程长(OR=1.304,P=0.001)、LEDD高(OR=1.003,P=0.012)是女性异动症的危险因素。
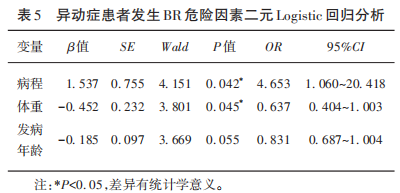
根据是否发生BR,对异动症进行亚组分析,分为BR组和no-BR组,发现BR组发病年龄更早、病程更长、体重更低(P<0.05),而二组在BMI、UPDRS-Ⅲ、H-Y分期、LEDD、NMSS、MMSE、MoCA等方面无明显差异(P>0.05)(见表4)。进一步以BR为因变量,以发病年龄、病程、体重为自变量进行多因素Logistic回归分析(见表5),结果提示体重高(OR=0.637,P=0.045)是女性患者BR的保护因素,而病程长(OR=4.653,P=0.042)是BR的危险因素。

3 讨 论
研究发现,PD患者左旋多巴诱导的异动症(levodopa-induced dyskinesia,LID)与性别有关。2018年的一项关于PD进展标志物预测因子的队列研究分析结果显示,女性是预测异动症发生的独立风险因子,其HR为1.61(95%CI 1.05~2.47),究其原因,与女性具有独特生理特点有关。因此,对女性PD患者异动症的临床特征和可能危险因素的专项研究,存在重要临床意义。
本研究发现发病年龄小、病程长、体重低、BMI值低、LD服用年限长、LEDD高、病情重是女性PD患者发生异动症的影响因素,通过多因素Logistic回归分析,病程长(OR=1.304,P=0.001)、LEDD高(OR=1.003,P=0.012)是导致女性PD患者出现异动症的危险因素。而BMI值高(OR=0.770,P=0.005)是女性PD患者发生异动症的保护因素。与先前多项临床研究相似。提示临床遇到女性PD患者,需要重点关注BMI值、LEDD剂量及病程。
有研究报道PD患者接受LD治疗5年后LID发生率约为30%~40%,治疗10年,LID发生率可达60%。König等报道,经LD治疗5年后,LID的发生率约为40%~50%,10年后甚至高达90%以上。上海一项多中心研究纳入1 558例PD患者,女性PD 703例,LID发生率11.4%。本研究纳入146例女性PD,LID发生率为20.5%。研究结果的差异考虑与纳入患者的病程、疾病严重程度、患者来源区域、人种等不同有关。整体而言,国内LID发生率要低于国外。针对不同研究结果的异同,分析可能存在以下原因:(1)国内PD患者普遍存在一定程度LD“恐惧”相关,部分与处方医生理念也相关,当前仍有相当多的人认为在不影响患者生活质量前提下,应尽可能推迟或延缓LD的使用。(2)LID的危险因素诸多,但相互影响,比如病程和疾病严重程度、LD治疗时间及剂量,药代动力学和基因学方面等因素。(3)纳入的研究人群样本和性别不同:本研究仅为女性患者,未纳入男性PD,女性PD患者LID发生率高于上海研究,考虑与发病年龄轻、病程长、体重和BMI低、LD治疗年限长及LEDD高等有关。本研究患者发病年龄(54.3±12.5)岁,病程(9.9±3.7)年,体重(54.1±8.2) kg,BMI(20.9±3.1) kg/m2,LEDD(703.2±203.9) mg/d,LD治疗时间(7.5±3.2)年,而上海研究纳入女性患者的发病年龄(63.0±9.5)岁,病程(8.2±5.5)年,体重(58.5±10.1) kg,LEDD(581.7±311.4) mg/d,LD治疗时间(5.9±4.7)年。这可能是我们女性PD患者LID高于上海研究的主要原因。
本文还针对10例存在脆性左旋多巴反应(BR)的患者进行了相关分析,占全部异动症的33.3%,BR组发病年龄(47.2±8.4)岁,病程(12.8±3.7)年,体重(49.9±6.1) kg,BMI(19.7±2.5) kg/m2,进一步比较BR组与no-BR组,发现BR组患者发病年龄更小(早发型为主)、病程更长、BMI更低。通过二元回归分析,发现病程长、体重低是异动症女性患者发生BR的危险因素,提醒我们对已发生异动症的女性患者,尤其是早发型患者,更要重点关注体重和病程,如果体重过低,需警惕BR发生可能,因为这对患者的生活影响和致残性影响更大。鉴于BR组样本量较少,希望将来可以增加更多符合条件的入组患者,这对深入了解BR的发病机制及可能的危险因素有积极的意义。关于BR概念,最早是由Mclellan在1982年提出的。当前BR定义是采用Martinez-Ramirez建议:对未行脑深部起搏器(deep brain stimulation,DBS)手术的PD患者,如果单次LD剂量在100 mg或以下,即发生中度或以上致残性LID,表明该患者存在“BR”现象,并依据单次LD剂量大小,分为中度和重度,即单次LD剂量在51~100 mg之间,为中度BR,50 mg或更小剂量,则为重度BR。本研究10例BR患者,符合重度3例(占异动症10%、BR 30%)、中度7例(占异动症23.3%、BR 70%)。BR的主要临床表现就是LD相关异动,故发病机制与异动症是相似的,分为突触前机制和突触后机制。Picconi等回顾性研究分析97例PD患者的资料,BR组11例,BMI平均19.5 kg/m2,平均体重53 kg,女性8例,占72.7%,与no-BR患者相比,BR患者体重相对更低,病程更长、BMI较低,LD较高。但在情绪、认知状态和伴有REM睡眠行为障碍方面未发现差异,与本研究结果相似,我们发现存在异动症,甚至BR的女性PD患者,与无异动症组相比,情绪及认知无显著差别。我们先前针对女性PD患者合并剂末现象(wearing-off, WO)的研究发现,WO(+)组抑郁评分显著高于WO(-)患者(P<0.05),分析原因考虑可能为关期状态的运动和或非运动症状的加重要大于异动症带来的对情绪影响。
综上所述,异动症在女性PD患者当中有较高的发生率,高危因素包括:BMI低、病程长、LEDD大,而是否发生BR与长病程和低体重关系更为密切。有报道称LD相关的异动多见于发病年龄小于45岁的早发型PD患者,譬如PARK2、PINK1、DJ-1、SNCA、LRRK2、ATP13A2、GBA、PLA2G6、VPS35等基因,因此本研究未来应增加对易感基因的检测。另外,男性PD患者异动症的临床特征及危险因素也应纳入,这更有利于全面了解PD患者异动症的临床特征及危险因素,本研究将进一步扩大样本量以进行深入和完善的研究。
参考文献
[1]Morris HR,Spillantini MG,Sue CM,et al. The pathogenesis of Parkinson’s disease[J]. Lancet,2024,403(10423):293-304.
[2]中华医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍学组. 中国帕金森病治疗指南(第四版)[J]. 中华神经科杂志,2020,53(12):973-986.
[3]Aslam S,Manfredsson F,Stokes A,et al. “Advanced” Parkinson’s disease:a review[J]. Park Relat Disord,2024,123:106065.
[4]Aradi SD,Hauser RA. Medical management and prevention of motor complications in Parkinson’s disease[J]. Neurotherapeutics,2020,17(4):1339-1365.
[5]中华医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍专业委员会. 中国帕金森病的诊断标准(2016版)[J]. 中华神经科杂志,2016,49(4):268-271.
[6]Eusebi P,Romoli M,Paoletti FP,et al. Risk factors of levodopa-induced dyskinesia in Parkinson’s disease:results from the PPMI cohort[J]. NPJ Parkinsons Dis,2018,4:33.
[7]Cerri S,Mus L,Blandini F. Parkinson’s disease in women and men:what’s the difference?[J]. J Parkinsons Dis,2019,9(3):501-515.
[8]Espay AJ,Morgante F,Merola A,et al. Levodopa-induced dyskinesia in parkinson disease:current and evolving concepts[J]. Ann Neurol,2018,84(6):797-811.
[9]Leta V,Jenner P,Ray Chaudhuri K,et al. Can therapeutic strategies prevent and manage dyskinesia in Parkinson’s disease?An update[J]. Expert Opin Drug Saf,2019,18(12):1203-1218.
[10]Xie CL,Wang WW,Zhang SF,et al. Continuous dopaminergic stimulation (CDS)-based treatment in Parkinson’s disease patients with motor complications:a systematic review and meta-analysis[J]. Sci Rep,2014,4:6027.
[11]König E,Nicoletti A,Pattaro C,et al. Exome-wide association study of levodopa-induced dyskinesia in Parkinson’s disease[J]. Sci Rep,2021,11(1):19582.
[12]Chen W,Xiao Q,Shao M,et al. Prevalence of wearing-off and dyskinesia among the patients with Parkinson’s disease on levodopa therapy:a multi-center registry survey in mainland China [J]. Transl Neurodegener,2014,3(1):26.
[13]万志荣,冯涛. 脆性左旋多巴反应的临床研究进展[J]. 临床神经病学杂志,2020,33(3):226-228.
[14]Martinez-Ramirez D,Giugni J,Vedam-Mai V,et al. The “brittle response” to Parkinson’s disease medications:characterization and response to deep brain stimulation[J]. PLoS One,2014,9(4):e94856.
[15]Yoo HS,Chung SJ,Chung SJ,et al. Presynaptic dopamine depletion determines the timing of levodopa-induced dyskinesia onset in Parkinson’s disease[J]. Eur J Nucl Med Mol Imaging,2018,45(3):423-431.
[16]Yan Y,Li Y,Liu X,et al. Analysis of factors associated with brittle response in patients with Parkinson’s disease[J]. Ann Clin Transl Neurol,2020,7(5):677-682.
[17]Picconi B,Hernández LF,Obeso JA,et al. Motor complications in Parkinson’s disease:striatal molecular and electrophysiological mechanisms of dyskinesias[J]. Mov Disord,2018,33(6):867-876.
[18]万志荣,赵静,解金金,等. 女性帕金森病患者剂末现象的临床特征和危险因素分析[J]. 神经损伤与功能重建,2023,18(8):461-464,473.
[19]Towns C,Fang ZH,Tan MMX,et al. Parkinson’s families project:a UK-wide study of early onset and familial Parkinson’s disease[J]. NPJ Parkinsons Dis,2024,10(1):188.
[20]Skou LD,Johansen SK,Okarmus J,et al. Pathogenesis of DJ-1/PARK7-mediated Parkinson’s disease[J]. Cells,2024,13(4):296.
[21]Ye H,Robak LA,Yu M,et al. Genetics and pathogenesis of Parkinson’s syndrome[J]. Annu Rev Pathol,2023,18:95-121.


