JMV: 病毒学国家重点实验室罗敏华团队在人巨细胞病毒致神经损伤机制方面取得新进展
时间:2023-03-10 20:51:30 热度:37.1℃ 作者:网络
近日,国际学术期刊Journal of Medical Virology在线发表了病毒学国家重点实验室罗敏华团队的最新研究成果,论文题为“Human cytomegalovirus infection perturbs neural progenitor cell fate via the expression of viral microRNAs”(人巨细胞病毒通过表达病毒小核糖核酸干扰神经前体细胞命运)。该工作为揭示人巨细胞病毒(Human Cytomegalovirus,HCMV)感染导致胎脑损伤机制提供了新依据。

神经前体/干细胞(neural progenitor/stem cell,NPC)是神经发育的基础,也是胎脑中对先天性HCMV感染最敏感的靶细胞。HCMV感染抑制NPCs细胞增殖,并诱导NPCs异常分化,导致NPCs细胞命运改变的机制仍未透彻解析。小核糖核酸(miRNAs)是真核生物中广泛存在的21至23个核苷酸的非编码RNAs,通过结合mRNA 的3’UTR调控靶标基因表达。HCMV可编码至少26种miRNAs,但在NPCs中的表达谱与是否参与NPC细胞命运调控未见报道。
该项研究基于HCMV感染人NPCs细胞模型,通过miRNAs微阵列分析发现大多数宿主 miRNAs水平未受影响,而6种病毒miRNAs水平显着升高。继续经深度学习的计算生物学分析策略对病毒miRNAs与相应mRNA转录组学数据进行了整合分析,预测出病毒miRNAs的调控网络,并对特定靶标进行验证。发现病毒 miRNAs的调控靶标显着富集于神经发育和细胞周期等通路;经qRT-PCR验证了病毒miRNAs和调控靶标基因的表达水平;通过构建hcmv-miR-US25-1缺陷病毒和靶标Jag1的3’UTR突变体,证实了hcmv-miR-US25-1与神经发生关键分子之一的Jag1 3’UTR靶位点的结合,并导致NPCs中Jag1 mRNA 和蛋白质水平均显着降低。该研究通过运用深度学习、多组学整合等计算生物学、生物信息学方法指导实验设计,系统性的研究了HCMV miRNAs在感染过程中的表达情况及其对神经发育相关宿主基因表达的影响,为进一步探讨先天性HCMV感染致胎脑畸形机制提供系新思路。
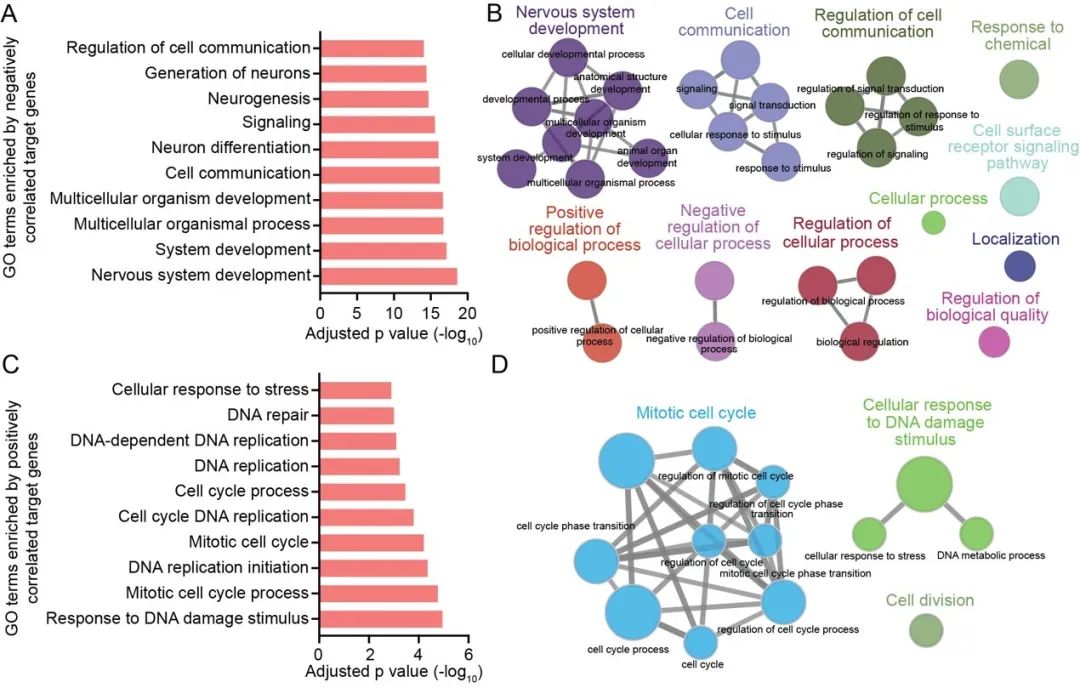
图示:HCMV感染NPCs通过表达病毒miRNAs影响神经发育及细胞周期的靶标基因
武汉病毒所-广州市妇女儿童医疗中心联合博士后姜旋、奥斯陆大学刘思情和病毒所博士研究生付亚茹为共同第一作者;武汉病毒研究所罗敏华研究员、奥斯陆大学Simon Rayner教授为共同通讯作者。该研究得到了国家自然科学基金和挪威研究委员会的资助。


