重磅更新 | 阿得贝利单抗纳入中华医学会肺癌临床诊疗指南1类推荐!
时间:2023-08-31 20:57:01 热度:37.1℃ 作者:网络
关于指南更新 2023年7月18日,《中华医学会肺癌临床诊疗指南(2023版)》于《中华医学杂志》第103卷第27期正式发布,旨在为各级临床医师提供肺癌筛查、诊断、病理、治疗和随访等方面的循证医学证据和指导性建议[1]。

国产PD-L1抑制剂阿得贝利单抗联合铂类一线治疗广泛期小细胞肺癌纳入《中华医学会肺癌临床诊疗指南(2023版)》1类推荐证据[1]
其中,今年2月28日获批上市的国产原研PD-L1抑制剂阿得贝利单抗(艾瑞利®)作为广泛期小细胞肺癌(ES-SCLC)一线治疗的1类推荐证据写入《中华医学会肺癌临床诊疗指南(2023版)》[1]。“新鲜血液”阿得贝利单抗为何能够在上市6个月内即荣获指南推荐、在白热化的PD-(L)1市场竞争中脱颖而出?论其根本,这与药物研发设计时精挑细琢的初心及临床研究中优异的疗效、安全性数据息息相关。
精挑细琢,极致纯净
随着对肿瘤免疫微环境 (TIME)了解的不断深入,人们发现PD-L1不仅表达在肿瘤细胞表面,也表达于T细胞、树突细胞及巨噬细胞等免疫细胞表面,甚至在某些免疫细胞表面的表达量远高于肿瘤细胞[2]。这就对具有Fc段效应功能(抗体依赖的细胞介导的细胞毒性(ADCC)作用、补体依赖的细胞毒性(CDC)作用、抗体依赖性细胞介导的吞噬(ADCP)作用及抗体依赖性细胞因子释放(ADCR)效应等)的抗体药物应用提出了挑战——保留的Fc段效应功能不仅可能会结合并误伤免疫细胞,甚至会引起不可控的疗效损失与不良反应。
因此,基于对可靠疗效、优异安全性的追求,阿得贝利单抗在研发立项时就非常明确要筛选得到一款抗体功能更加纯净、亲和力更高并专注于阻断PD-L1/PD-1信号通路的免疫检查点抑制剂。这份精挑细琢的初心也注定了阿得贝利单抗将极致纯净,与众不同。
首先, 抗体亚型选择不同。阿得贝利单抗采用了IgG4抗体亚型,这类抗体的分子铰链区较短,本身无CDC效应,抗体功能更加纯净,安全性更好[3];
其次,抗体Fc段进行了改造。通过进一步对阿得贝利单抗Fc段234A/235A定点突变改造,降低了与免疫效应细胞表面FcγR结合的能力,消除了ADCC、ADCP效应,同时也降低了ADCR效应[4]。ADCR效应的降低,不仅能够减少IL-8的释放,增强免疫疗效,也能够减少IL-6的释放,继而减少免疫相关不良反应的发生;
阿得贝利单抗的抗体亚型选择与结构改造 [3-5]
最后,分子结构及药理特性不同。相比于既往上市的PD-L1抑制剂,阿得贝利单抗具有独特的PD-L1结合表位——结合角度更加居中、结合区域与结合面积更接近天然配体PD-1。同时阿得贝利单抗与PD-L1结合的解离常数Kd值仅为0.27*10-10mol/L,亲和力强于已上市的PD-L1抑制剂[5]。
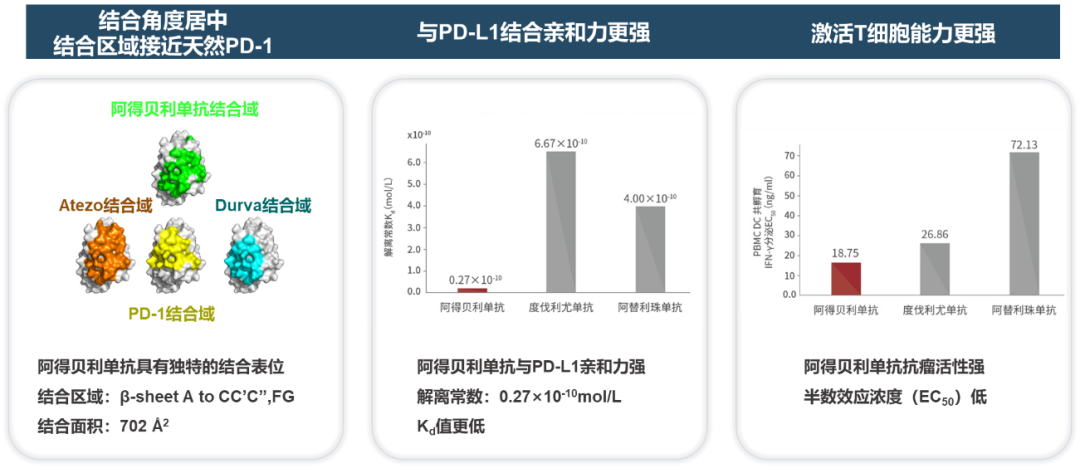
不同PD-L1抑制剂的药理特性 [5]
总而言之,阿得贝利单抗在研发过程中通过抗体类型的选择与结构的改造,减少了对免疫细胞的误伤与副作用的发生,进而使阿得贝利单抗更专注于阻断PD-1/PD-L1通路。这份精挑细琢的初心也充分体现于CAPSTONE-1临床研究可靠的疗效与优异的安全性数据中。
优选推荐,利久长安
CAPSTONE-1临床研究结果的公布,不仅推动了首个国产原研PD-L1抑制剂阿得贝利单抗联合依托泊苷和卡铂用于ES-SCLC一线治疗的适应症获批,更打破了进口药的垄断局面,为免疫治疗在中国ES-SCLC患者中的应用提供强有力的证据。阿得贝利单抗联合化疗组中位无进展生存期(mPFS)达5.8个月,相较于化疗组显著降低患者疾病进展风险33%(HR 0.67;95% CI:0.54-0.83;p<0.0001);中位总生存期(mOS)达15.3个月(HR 0.72;95% CI:0.58-0.90;p=0.0017),显著降低死亡风险28%;2年OS率达31.3%,是对照组的近2倍,使近1/3患者生存期突破两年;两组间客观缓解率(ORR)为70.4% vs. 65.9%,中位缓解持续时间(DoR)为5.6 个月vs. 4.6个月[5]。
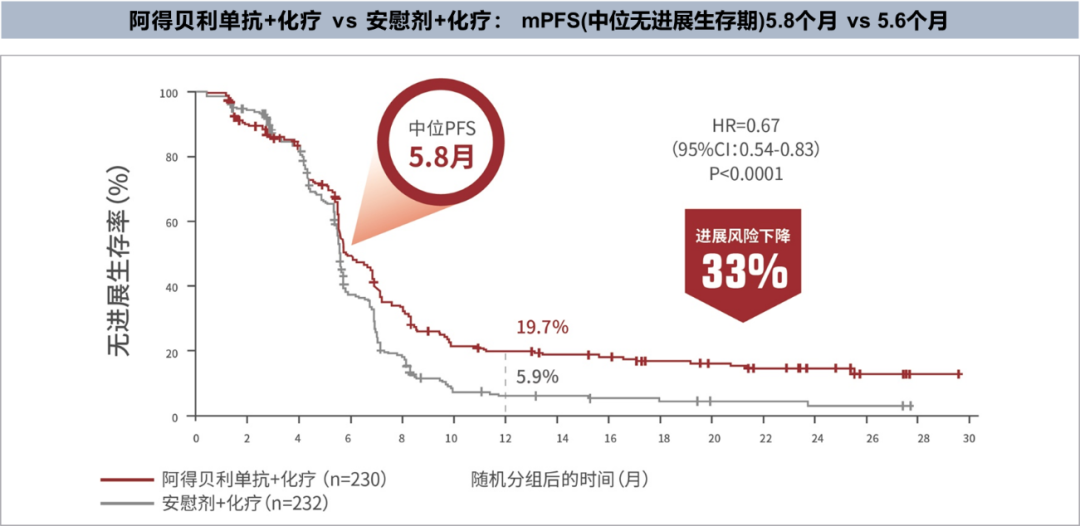
阿得贝利单抗联合化疗一线治疗ES-SCLC mPFS达5.8个月,显著优于化疗[5]
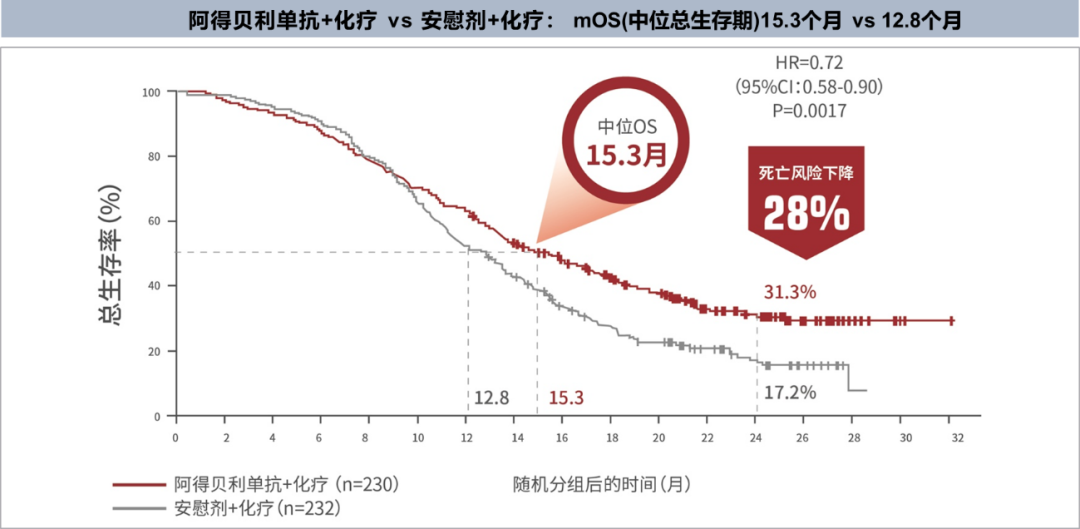
阿得贝利单抗联合化疗一线治疗ES-SCLC mOS达15.3个月,显著优于单纯化疗[5]
出身不凡,铸就安全
在免疫治疗应用过程中,临床医生更为关注的是免疫相关不良反应(irAEs)的发生情况。irAE的判定需要研究者进行鉴别诊断,考虑到不同研究irAE的鉴别诊断标准不同、开放标签试验的研究者判定偏移等因素,通常同一研究中试验组与对照组irAE的相对关系更能反映irAE的发生率。我们发现,经过精挑细琢的阿得贝利单抗显示出优异的安全性——在CAPSTONE-1临床研究中,试验组irAE发生率为27.8%,较对照组仅增加10.6%;≥3级irAE试验组发生率均不超过1.8% [5]。这充分印证了阿得贝利单抗在分子设计阶段蕴含的中国匠心,致力于为中国ES-SCLC患者带来利久长安的新选择。
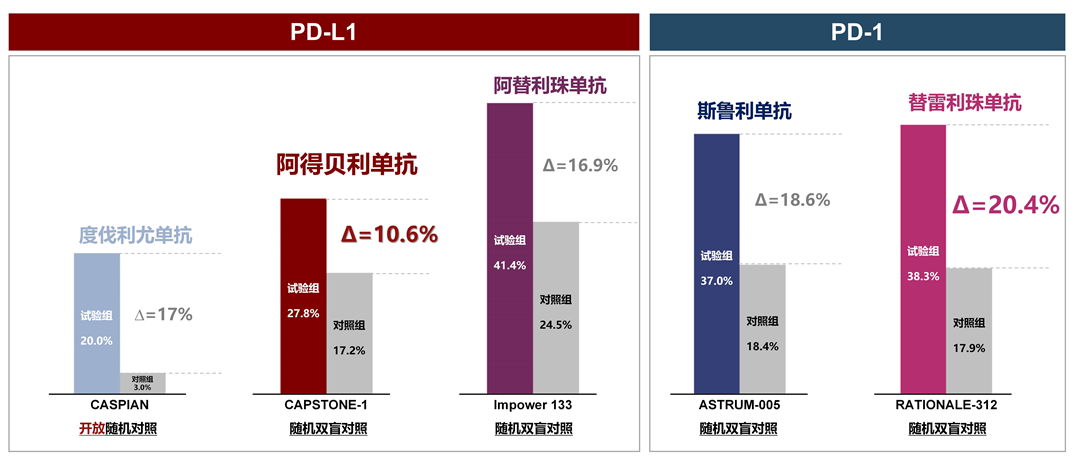
ES-SCLC研究中irAE发生率相关数据[5-9]
再入指南,规范实践
CAPSTONE-1研究首次在中国ES-SCLC患者中证实,国产原研PD-L1抑制剂阿得贝利单抗联合含铂化疗疗效可靠、安全性优异,提供了更切合中国患者的循证医学证据,更具有指导中国临床实践的意义。因此,基于CAPSTONE-1卓越的研究数据与中华医学会肿瘤学分会的认可,阿得贝利单抗联合含铂化疗一线治疗ES-SCLC于2023年7月18日正式纳入《中华医学会肺癌临床诊疗指南(2023版)》1类推荐证据。这也是继2023年4月纳入《CSCO小细胞肺癌诊疗指南(2023)》I级优选推荐(1A类证据)之后,阿得贝利单抗在ES-SCLC治疗领域再创佳绩,树立了ES-SCLC免疫治疗的新标杆[1,10]。
更强免疫,惠及各方
惠民保是在各地医疗保障局、银保监局等政府部门指导和监督下的一种普惠性补充医疗保险。随着阿得贝利单抗获批上市并进入两大指南推荐,多地惠民保将其纳入特药报销目录,充分体现了各地监管部门对于阿得贝利单抗疗效与安全性的充分认可。据统计,目前已有23个城市将阿得贝利单抗纳入惠民保报销目录。也相信随着阿得贝利单抗的纳入,更多中国患者能够用上国产原研且疗效可靠、安全性更优的全新一代PD-L1抑制剂。
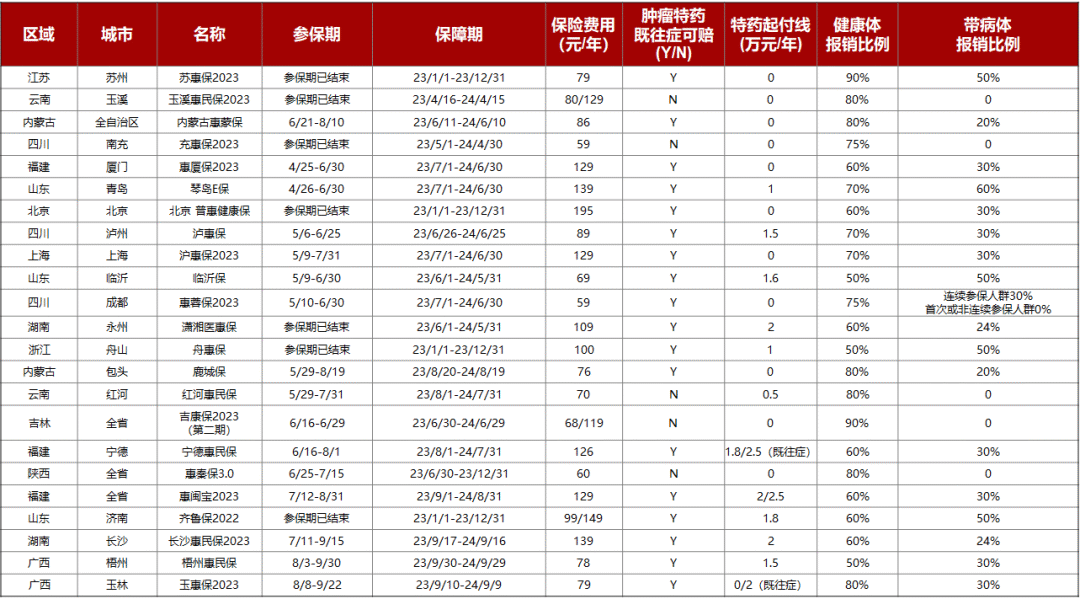
阿得贝利单抗全国惠民保纳入情况(数据截止时间:2023年8月9日)
大浪淘金始见金,沧海济帆终接云。阿得贝利单抗立足于中国人群,以强有力的中国证据助力中国患者获得长生存希望。相信随着阿得贝利单抗此次再入指南,定能惠及更多中国ES-SCLC患者。
1.中华医学会肿瘤学分会, 中华医学会杂志社. 中华医学会肺癌临床诊疗指南(2023版)[J]. 中华医学杂志, 2023, 103(27): 2037-2074.
2.Venetis K, et al. Eur J Cancer Prev. 2023 Jul 1; 32(4):364-369.
3.Gogesch P, et al. Int J Mol Sci. 2021 Aug 19; 22(16):8947.
4.Liu R, et al. Antibodies (Basel). 2020 Nov 17; 9(4):64.
5.Wang J, et al. The Lancet Oncology. 2022 Jun; 23(6):739-747.
6.Horn L, et al., N Engl J Med, 2018; 379:2220-2229.
7.Paz-Ares L, et al. Lancet. 2019; 394(10212):1929- 1939.
8.Cheng Y, et al, JAMA. 2022; 328(12):1223–1232.
9.Cheng Y, et al. WCLC, 2023, OA01.06.
10.中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)小细胞肺癌诊疗指南-2023[M]. 北京:人民卫生出版社,2023.
来源:肿瘤资讯


