广州医科大学李仕颖教授: 转铁蛋白受体靶向免疫刺激剂通过阻断β-catenin/CREB激活光动力肿瘤免疫治疗的研究
时间:2024-06-19 20:00:37 热度:37.1℃ 作者:网络
肿瘤转移是导致超过90 %肿瘤患者死亡的主要原因,然而传统疗法对转移肿瘤的疗效不佳,如何同时清除原位瘤和转移肿瘤是当前肿瘤治疗面临的重要问题之一。其中,免疫治疗是通过激活机体自身的免疫识别和杀伤作用以实现肿瘤细胞的清除,然而肿瘤细胞免疫原性较低,且肿瘤细胞呈现免疫抑制表型,极大的削弱了传统疗法的免疫激活效应。近期研究发现,传统的肿瘤疗法启动肿瘤细胞免疫原性死亡(ICD),促进肿瘤相关抗原(TAAs)的释放,具有改善肿瘤免疫原性并激活抗肿瘤免疫效应。与此同时,肿瘤细胞可以通过过度激活β-连环蛋白(β-catenin)通路,抑制C-C基序趋化因子配体4(CCL4)的分泌,减少树突细胞(DC)向肿瘤部位的募集和杀伤性T细胞的浸润,造成免疫抑制微环境和免疫响应率低下。
近日,广州医科大学李仕颖教授团队报道了一种转铁蛋白受体靶向免疫刺激剂(PTI),通过联合光动力学治疗和阻断β-catenin信号通路激活转移性肿瘤的光动力免疫疗法。其中,PTI能靶向肿瘤细胞高表达的转铁蛋白受体,提升药物向肿瘤细胞的靶向递送效率,通过光动力疗法破坏原发肿瘤,并引发免疫原性细胞死亡和释放肿瘤相关抗原。与此同时,PTI能阻断肿瘤细胞β-catenin信号通路,上调CCL4以募集树突状细胞呈递肿瘤特异性抗原,同时下调PD-L1抑制肿瘤细胞的免疫逃避,进而协同激活抗肿瘤免疫并实现肺转移肿瘤的免疫治疗。相关工作以“Transferrin receptor targeted immunostimulant for photodynamic immunotherapy against metastatic tumors through β-catenin/CREB interruption”为题发表在《Acta Pharm. Sin. B》期刊上,广州医科大学王涛教授、李仕颖教授为该论文的通讯作者,硕士研究生严梦依为第一作者。

【文章要点】
本研究设计了一种TfR靶向纳米免疫刺激剂(PTI),并用于阻断β-catenin/CREB通路激活转移性肿瘤的光动力免疫效应。PTI具有良好的稳定性、分散性和光动力特性,能够促进药物在TfR过表达的肿瘤组织和细胞处富集。首先,PTI的PDT效应能高效抑制原发瘤的生长,并触发肿瘤细胞ICD效应,促进CRT暴露和HMGB1释放。此外,PTI同时能阻断β-catenin与CREB的结合并调节肿瘤细胞基因转录,上调CCL4促进DC募集以呈递肿瘤特异性抗原并促进T细胞的活化和浸润,下调肿瘤细胞PD-L1促进免疫细胞的免疫识别和清除作用。通过靶向药物递送和抗肿瘤免疫调控作用,PTI能高效激活抗肿瘤免疫效应并协同抑制原发瘤和转移瘤的生长,为基于联合用药激活无抗体肿瘤免疫疗法提供了一种新的思路。
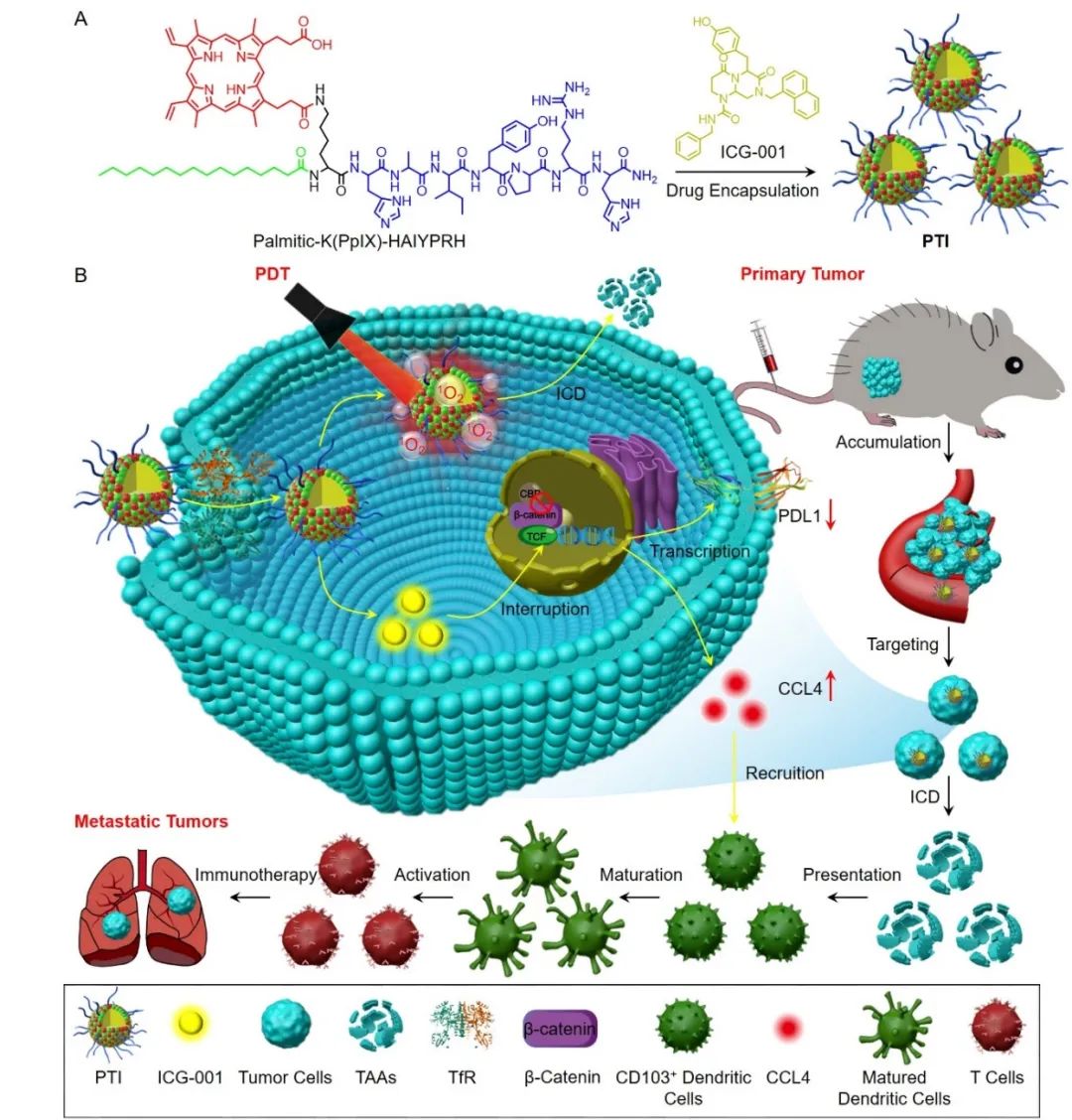
图1. PTI的设计及其激活光动力免疫疗法的机制。
原文链接:
https://doi.org/10.1016/j.apsb.2024.05.030


