IVD前沿丨实时基因组学可检测隐藏的抗生素耐药性
时间:2024-08-02 16:03:17 热度:37.1℃ 作者:网络
世界卫生组织已宣布抗生素耐药性是全球十大最严重的健康威胁之一,耐药性感染由于治疗延迟或不适当而导致更高的死亡率和发病率。快速和准确地识别耐药细菌病原体可以促进早期给予适当的治疗,降低死亡率和感染和治疗相关的发病率。
以纳米孔测序技术为动力的实时基因组学提供了在临床环境中直接加速病原体鉴定和抗生素耐药性分析的潜力。纳米孔测序产生长读数的能力可以用来创建高度精确的、接近完整的基因组组装,用于菌株水平的鉴定和细菌病原体及其抗生素耐药性的从头检测。这与复杂感染尤其相关,在这种情况下,快速的靶向治疗可能对患者的预后特别有益。
近日,杂志Nature Communications上发表了一篇题为“Detection of hidden antibiotic resistance through real-time genomics”的文章。在这里,作者通过肺炎克雷伯菌感染的例子,展示了实时基因组学在临床环境中的力量,与临床建立的诊断相比,基于实时基因组学的耐药预测可以识别位于低丰度质粒上的新型抗生素耐药基因变体。这一发现对临床决策和潜在的患者预后具有重要意义,说明了将实时基因组分析整合到临床实践中的变革潜力。

图片来源:Nature Communications
主要内容
实验内容概述
作者使用来自同一感染病例的细菌分离株对临床建立的诊断和基于实时基因组学的预测进行了比较分析。临床建立的诊断方法包括用于细菌分类鉴定的MALDI-TOF MS和用于抗生素耐药谱分析的VITEK2(如下图)。病例研究涉及一名免疫功能低下的患者,他出现发烧,最初使用碳青霉烯类抗生素美罗培南治疗。
这种比较方法能够在真实的临床场景中直接评估实时基因组预测与传统方法的准确性和速度,突出了基因组技术在快速准确的病原体鉴定和耐药性预测方面的潜在优势。
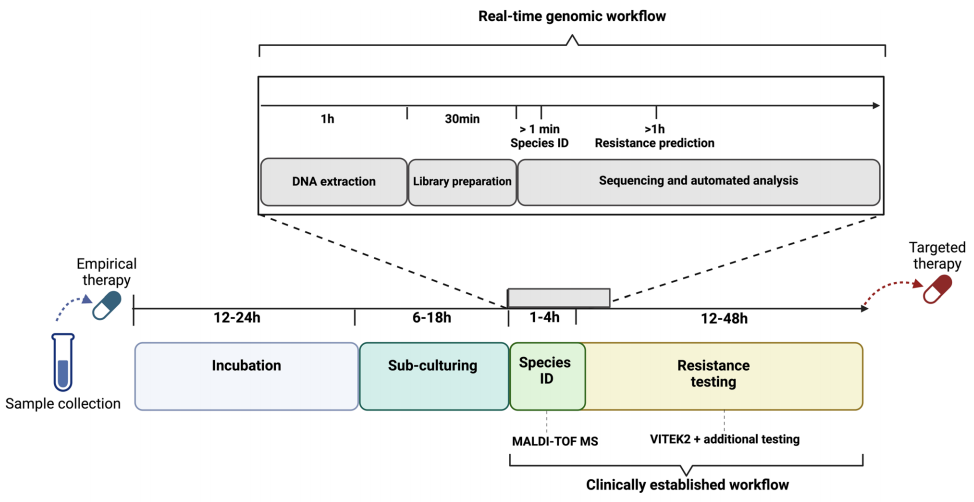
实时基因组和临床建立的病原体鉴定方法的工作流程概述。
图片来源:Nature Communications
临床诊断
最初,收集气管内抽吸样本(“治疗前”样本),临床建立的诊断方法从中鉴定出碳青霉烯耐药肺炎克雷伯菌。因此,立即将治疗从美罗培南切换到头孢他啶阿维巴坦CAZ-AVI(如下图)。刚开始临床有改善,但迅速恶化,随后从患者(“治疗后”样本)的血液中培养出肺炎克雷伯菌,其恢复了碳青霉烯类药物敏感性,但CAZ-AVI耐药,且未检测到任何碳青霉烯酶。因此,美罗培南被重新引入。尽管采取了这些措施,患者还是很快去世了。
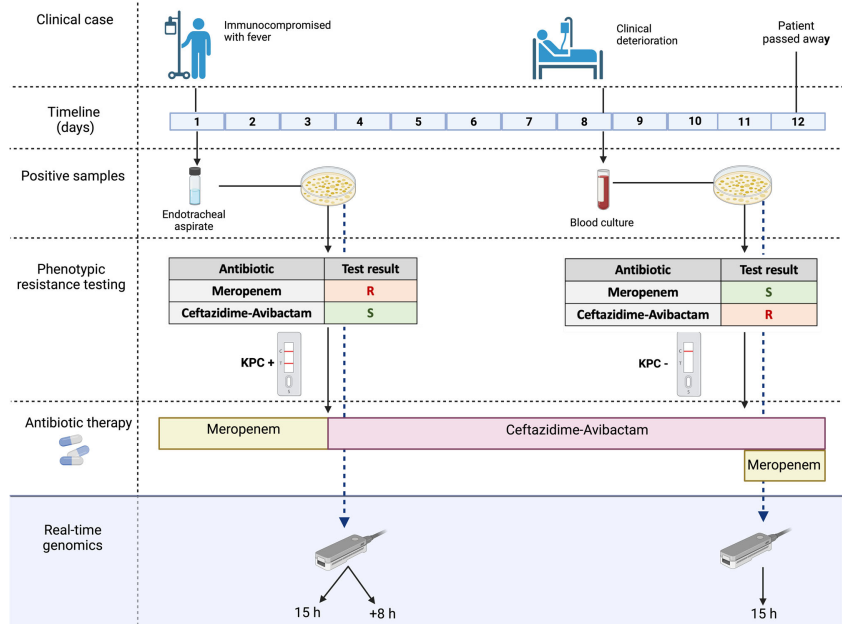
该感染病例的病程和治疗方法概述。
图片来源:Nature Communications
实时基因组学诊断
作者模拟了实时基因组学在该临床病例中的应用。对治疗前和治疗后的分离株进行了快速纳米孔鸟枪测序(如上图),并确定了肺炎克雷伯菌为致病病原体。在治疗前分离株中检测到blaKPC-2基因拷贝,证实了美罗培南耐药性。治疗后的分离株鉴定出了许多blaKPC-14拷贝,被认为赋予CAZ-AVI抗性,同时可能恢复体外碳青霉烯类敏感性。因此,基于基因组学的耐药预测不仅与传统诊断确定的耐药模式一致,而且还确定了blaKPC-14是假定的耐药机制(见下表)。
至关重要的是,实时基因组学方法还在治疗前分离株中检测到blaKPC-14抗性基因的单个拷贝。另外8小时的重复测序鉴定出四个更高准确性的blaKPC-14拷贝。在重复测序两个小时时,第二个blaKPC-14基因拷贝已经被检测到。
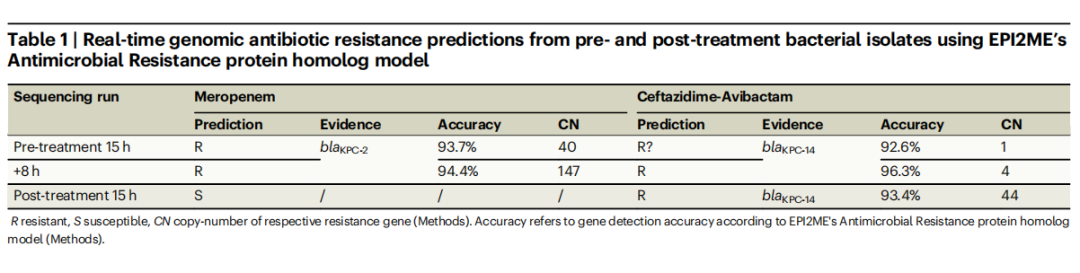
实时基因组学诊断结果。
图片来源:Nature Communications
流行病学和功能分析
作者成功地从治疗前后的分离株中从头组装了一个完整的染色体和三个完整的环状质粒(如下图)。cgMLST显示两株分离株均为高危序列型ST147,,在遗传上与全球已知的ST147基因组不同。blaKPC-2(治疗前)和blaKPC-14(治疗后)基因位于IncN质粒上。进一步推断,治疗前后的分离株中,相对于细菌染色体,IncN质粒的拷贝数分别为3和4。在CAZ-AVI暴露后,blaKPC-14的标准化丰度从0.56%增加到26.6%。
在治疗后分离株提交给德国革兰氏阴性菌国家参考中心后,最初定义为blaKPC-14的KPC耐药基因被鉴定为先前未记载的KPC亚型,随后被命名为blaKPC-159。
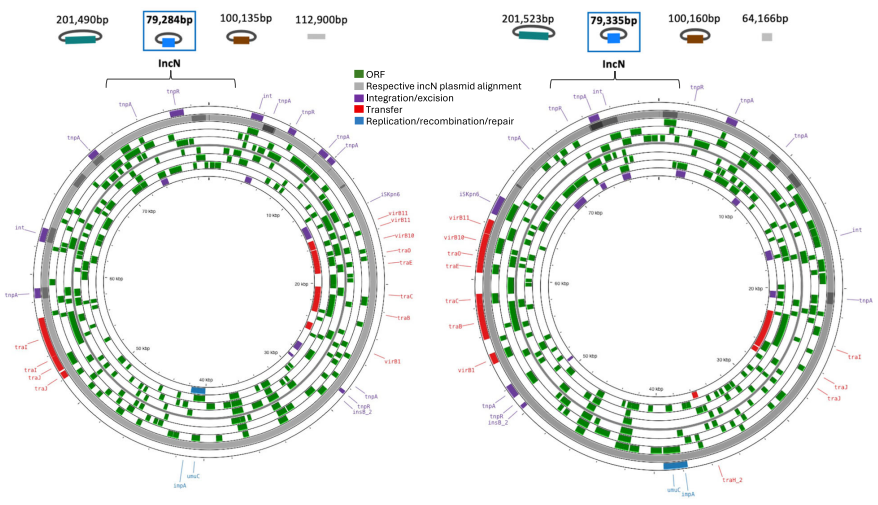
治疗前后分离株的基因组和质粒从头组装。
图片来源:Nature Communications
总结与讨论
实时基因组学在该患者病例中的应用强调了在临床环境中使用该技术快速准确地描述复杂细菌感染的巨大潜力。此研究结果表明,体外抗生素耐药性的转变可能是由于涉及相同肺炎克雷伯菌谱系的复杂感染,低丰度携带blakpc -14的IncN质粒由于其在CAZ-AVI暴露下的进化选择优势而成为优势。已经证明,纳米孔测序可以揭示表型方法未能检测到的CAZ-AVI耐药性,从而影响治疗方法。
但实时基因组学仍然存在两个重大限制。首先,专注于细菌分离可能限制了患者感染的微生物多样性的可能。其次,此分析仅限于同一患者的两种细菌分离株。不幸的是,由于本研究的回顾性,无法调整样本量或获得更频繁的采样样本。
总之,此研究展示了经济高效、快速的实时基因组学如何在预测抗生素耐药性的准确性方面优于现有的诊断方法。从表型抗性测试到完全基于基因组学的预测,需要进一步的研究。然而已经预见到将实时基因组技术的优势与医院环境中临床建立的抗生素耐药性分析方法相结合的巨大潜力。进一步设想,测序准确性的不断提高和纳米孔测序技术所需的相对较低的投资为管理世界范围内的复杂感染病例提供了有希望的前景,特别是在先进诊断设备可能不容易获得的中低收入环境中。


