长期使用抗生素抑制细菌感染
时间:2024-10-16 11:01:53 热度:37.1℃ 作者:网络
当患者的感染被假定为无法通过确定的疗程或病源控制治愈时,医生就会开具抑制性抗生素治疗。接受抑制性抗生素疗法的患者通常合并症较多,感染通常涉及残留的假体材料。部分由于缺乏关于明确的抑制性抗生素使用指南,部分由于相关感染的复杂性,医生通常会给患者开具极长的、甚至无限期的抑制性抗生素治疗。在这种情况下,长期抗生素暴露的风险尚未完全确定,但其中包括了从轻微到严重的药物不良反应、抗生素耐药菌的产生以及肠道微生物群的紊乱。在这篇叙述性综述中,我们介绍了4种常见适应症中使用抑制性抗生素疗法的现有证据,审视了当前文献中的空白,并探讨了这种疗法已知和潜在的风险。我们还就如何提高未来研究的证据质量提出了建议,特别是强调了需要一个标准化术语来描述使用长疗程抗生素来抑制难以治疗的感染。
抗生素是临床医生和许多患者熟悉的治疗药物。2021年,美国开出了超过2.11亿张抗生素处方。本综述侧重于抗生素使用的一个子部分:长期使用抗生素治疗被认为无法治愈的感染。虽然这只占抗生素总使用量的一小部分,但就其性质而言,它可能代表着抗菌药物管理的重要机会。
我们小组之前的一项研究发现,在长期使用抗生素的3大适应症中,使用抗生素来抑制被认为无法治愈的感染的证据最不充分。预防性和非感染性用途的其他广泛适应症不在本综述的讨论范围内。长期或无限期使用抗生素已被认为是一种治疗策略,适用于不适合采用侵入性手术方法的患者。这种方法通常不是为了治愈感染,而是为了改善症状,防止病情恶化或复发,从而达到具有临床意义的程度。我们之前的研究发现,在澳大利亚一家大型医院网络中,最常采用抑制性抗生素疗法(SAT)治疗的感染有四类:即假体周围关节感染(PJI)、血管移植物感染(VGI)和其他血管感染,包括感染性心内膜炎和霉菌性动脉瘤、心脏植入式电子设备感染(CIEDI),以及骨髓炎和其他骨科硬件相关感染。
针对这些广泛感染的指南通常建议采用药物和手术相结合的治疗方法。在某些情况下,不可能通过手术彻底控制感染源,并且/或者患者的合并症可能太严重而无法进行手术干预。在这种情况下,指南通常会提到SAT。然而,目前所审查的任何指南中,都没有关于使用SAT的具体建议。
治疗涉及假体材料的感染所面临的一大挑战是许多细菌能够形成生物膜。细菌生物膜是一种微小的基质,可粘附在活组织和假体硬件表面,并可以感染后迅速形成。嵌入假体材料生物膜中的细菌可以躲过传统显微镜和培养方法的检测。细菌生物膜的保护特性使其能够抵抗抗菌活性,从而使治疗假体硬件感染的工作变得越来越具有挑战性。很少有抗菌剂可以穿透生物膜;事实上,一些β-内酰胺类抗生素已被证明可以诱导生物膜。
SAT还可用于其他杂项感染。不过,这些适应症不在本次讨论范围内。
方法
2023年11月进行了文献检索。检索的数据库包括Ovid MEDLINE、PubMed和Cochrane。搜索策略将描述抑制性抗生素疗法(长期或长时间或持续或无限期或抑制*和抗菌素或抗生素)的术语与描述我们先前研究中描述的适应症的术语相结合:对于PJI:PJI或假体*或关节或关节成形术或置换;对于VGI:血管或移植物或血管内或内假体*或主动脉*或心内膜炎或霉菌性;对于CIEDI:植入物*或心脏或电子或除颤器*或心室*或设备;对于OM/其他植入物感染:骨髓炎中OM或骨或旋转*或金属器具。
搜索结果仅限于英语成人和人类研究。标题和摘要经人工筛选,以确保与SAT一致。排除了以治疗为目的而长期使用抗生素的研究。
假体周围关节感染
在文献中,金黄色葡萄球菌是PJI中最常见的感染病菌,其次是凝固酶阴性葡萄球菌。β-内酰胺类和四环素类是SAT最常用的抗生素。
从历史上看,SAT治疗PJI的效果不佳,但过去十年的成功率在60%到93%之间。许多研究缺乏对照组,但在那些有非SAT对照人群的研究中,SAT被证明可以降低感染复发的风险,尽管并不总是具有统计学意义。特别是在PJI伴有瘘的情况下,SAT并未显著改善植入物滞留的风险。
多篇已发表的文献综述探讨了SAT在PJI中的应用,通常作为外科清创和植入物保留(DAIR)后的后续治疗策略。这些综述通常发现成功率在66%到75%之间,但他们也承认由于目前文献的异质性,评估SAT的疗效存在困难——即在开始SAT之前,内科和外科治疗之间存在差异:什么治疗才真正构成SAT,以及治疗成功或失败的特征。
在SAT文献中,感染葡萄球菌(尤其是金黄色葡萄球菌)患者的预后似乎比非葡萄球菌感染患者更差。几项研究报告称,与其他细菌感染的患者相比,感染金黄色葡萄球菌引起的假体周围感染患者的预后更差。尽管没有直接可比性,但其他研究发现SAT对链球菌性PJI非常有效。2019年的一项针对链球菌引起的PJI患者的研究发现,使用SAT的治疗成功率为93%,而未使用SAT治疗的患者的成功率为57%(P=0.002),尽管一项较早的、样本量非常小的研究发现,50%(3/6)的β-溶血性链球菌感染患者治疗失败。然而,感染金黄色葡萄球菌的SAT患者的病情比感染其他病原体的患者更糟的趋势并不普遍。2020年和2022年的一项研究都发现,革兰氏阴性菌感染的SAT结果比革兰氏阳性菌感染更差。这一发现的原因尚不清楚,但2021年发表的一篇评论表明,这可能是由于针对革兰氏阴性菌的口服抗生素缺乏所致。
治疗PJI的理想SAT持续时间仍不明确。2020年的一项研究报告称,治疗持续时间超过12个月后,SAT失败的风险率并未显著下降。事实上,另一项研究发现,虽然SAT持续时间少于90天会增加失败风险,但较长的治疗持续时间(90-180天、180-365天和超过365天)与失败率的变化无关。文献中也有证据表明,患者在延长治疗时间后停止SAT,仍无症状出现。然而,目前尚无明确的指南来确定临床相关的停止点,也没有生物标志物可以表明停止SAT是安全的。红细胞沉降率(ESR)正常化等指标已被用于指导停止SAT或评估SAT作为一种治疗选择可能取得的成功。然而,文献中也有ESR正常的患者在停止SAT后3天至1个月内感染复发的案例。一些学者还建议使用C反应蛋白(CRP)水平、血清杀菌滴度大于1:8和放射性标记白细胞闪烁成像作为监测SAT反应的可能方法,但这些策略尚未在文献中得到广泛记录。
如前所述,研究间(甚至研究内)患者群体存在异质性,因此很难为临床实践提供建议。考虑到这一局限性,并根据最近一篇对PJI患者SAT的叙述性回顾,我们建议在管理接受SAT治疗的PJI患者时采取以下做法:
1. 如果炎症指标,尤其是ESR已恢复正常,则考虑在连续治疗1年后停止SAT。
2. 由于文献中葡萄球菌感染的预后明显较差,因此应对葡萄球菌感染患者进行更保守的治
疗,延长治疗时间,并更谨慎地停止SAT。
血管移植物感染
关于VGI的SAT的大部分文献来自病例系列和报告。这些病例报告之所以发表,大概是因为它们有独特的病因,不能反映大多数需要抑制性治疗的VGI。这些病例报告描述了由羊种布鲁氏菌、迟缓爱德华氏菌和犬二氧化碳嗜肺菌等病原体引起的VGI患者。在这种情况下,β-内酰胺类药物是最常用的抑制治疗抗生素。在许多研究中,用于长期抑制的抗生素并不明确。
回顾性研究报告的SAT治疗VGI的成功率各不相同,尽管计算机断层扫描(CT)/正电子发射断层扫描(PET)成像似乎可能有助于确定是否需要继续进行SAT。一项2021年的回顾性队列研究调查了32例未接受指定手术治疗的感染性心内膜炎患者的治疗效果。在这项研究中,24名患者接受了SAT,中位持续时间为277天,只有4名接受SAT的患者出现感染复发。9名患者根据CT/PET成像结果决定停止SAT,所有这些患者在随访期间均无症状。据估计,这项研究的总生存率为1年78%,3年总62%。2023年的一份关于3例人工瓣膜感染性心内膜炎患者的报告也发现,在PET结果的指导下,可以安全地停止SAT。
在识别SAT失败风险较高的患者方面,尚不清楚在SAT之前的手术治疗是否会改变预后。2014年发表的一项研究发现,所有10名接受SAT治疗而未接受手术干预的患者在治疗的第一年都没有出现再感染,但有3名患者在治疗的第一年后出现感染复发。早期一项针对主要因VGI和人工瓣膜感染而接受SAT但未进行手术治疗的患者的研究发现,51%的参与者在1年后仍在接受SAT。相比之下,2015年的一项针对霉菌性动脉瘤患者的研究发现,71%的患者在接受SAT治疗的同时接受了手术治疗,5年后仍然存活。另一项研究发现,5年生存率为59%±8%,与之略相似。本研究中的患者也接受了广泛的手术治疗,他们的主动脉移植物肠道侵蚀或瘘管在开始接受SAT治疗前已用利福平浸泡的移植物和大网膜覆盖进行了修复。
心脏植入式电子设备感染
大多数关于CIEDI的SAT文献都集中在左心室辅助装置(LVAD)感染患者身上。CIEDI中发现的需要长期抗生素抑制的病原体与PJI和VGI中的病原体相似;葡萄球菌是最常见的感染病原体。有趣的是,与β-内酰胺类药物相比,多西环素是最常见的SAT药物。
关于CIEDI中抑制性抗生素的文献主要针对使用心室辅助装置的患者。这些文献大多为小型回顾性队列研究。2020年对24名患者进行的一项回顾性队列研究发现,使用SAT治疗CIED驱动系统感染的成功率为50%。与此相反,2021年的一项回顾性研究对69名浅表性传动系统感染患者进行了研究,其中43名患者接受了SAT,研究发现SAT并未显著降低感染复发的风险。两项早期研究对接受SAT治疗LVAD相关感染的患者进行了研究,发现在平均治疗时间分别为5.8个月和1.6年之后,失败率分别为29%和31%。有趣的是,那项研究发现接受SAT治疗患者的失败率为29%,但未接受抑制性抗生素治疗的患者中只有11%出现感染复发。在这项研究中,接受SAT治疗的患者群体可能最初预后明显较差,被认为成功治疗的可能性较小,因此被开具了长期抗生素。
就存活率而言,2017年的一项研究发现,接受SAT治疗的CIEDI患者平均存活时间仅为1.43年。这项研究中的患者并未移除CIED。相比之下,2022年的一项研究发现,接受SAT治疗直至心脏移植的LVAD感染患者的总体5年存活率为92%。在这项研究中,因LVAD感染而接受SAT治疗的患者,与那些LVAD感染已解决或没有LVAD感染的患者相比,心脏移植后的预后并没有更差。这项回顾性研究仅调查了接受过心脏移植的患者,因此,那些不适合移植的患者(由于合并症或积极结果的可能性低)被排除在外,这可能解释了与以往研究相比,SAT相关成功率异常高的原因。
接受SAT治疗的LVAD感染患者的死亡率很高。目前,我们还无法确定何时以及是否可以安全地停止SAT,尤其是对于保留装置的患者。装置保留与高死亡率相关,但SAT可能会延缓治疗失败。对于预期寿命有限的合并症多的患者,延长无复发间隔期可能是一个重要的考虑因素。
考虑到这些证据,我们建议对CIEDI的SAT患者进行个体化的随访和管理,密切监测生物标志物并监测复发情况。
骨髓炎和脊柱硬件感染
除了PJI之外,在骨髓炎中使用抑制性抗生素的证据非常有限。2022年发表的一篇综述为急性和慢性骨髓炎的诊断和治疗提供了一般性建议。这篇综述表明,超过3个月的SAT可改善植入物相关骨髓炎患者的治疗结果。在综述的文献中,金黄色葡萄球菌是最常见的感染病菌,β-内酰胺类、多西环素和甲氧嘧啶-磺胺甲恶唑是SAT最常用的抗生素。
抑制性抗生素治疗似乎与早期脊柱植入物相关感染的良好治疗效果相关。一项回顾性队列研究发现,与患有DAIR但未接受SAT的患者相比,SAT提高了接受DAIR治疗的脊柱硬件感染患者的2年生存率(80% vs 33%)。作者还发现,SAT降低了脊柱植入后30天内发生感染患者的治疗失败风险,但对晚发型感染无益。同样,2016年的一系列病例发现,早发性耐多药脊柱手术部位感染患者在清创、静脉注射和长期口服抗生素后,感染在临床和生化方面均得到缓解。该系列病例中的患者通常在初次脊柱手术后3周内出现感染,并在感染诊断后3天内接受清创术。
延长SAT治疗时间似乎并不会提高生存率。一项回顾性队列研究调查了SAT在各种骨科假体患者(55%的患者患有脊柱硬件感染)中的使用情况,发现持续3个月的SAT与治疗成功有关,但持续6个月的SAT与治疗成功无关。有趣的是,2020年的一项回顾性队列研究发现,持续使用抑制性抗生素超过12个月与治疗成功呈负相关。事实上,一项研究发现,在最初接受SAT治疗的22名患者中,有10名患者在接受平均468天治疗时间,在随访872天后没有出现感染复发。其余12名患者中,有5名在治疗期间失败,并且在最后一次随访时仍在接受SAT治疗。从这些研究中可以看出,SAT有可能在感染后的最初几个月提高患者生存率,但尚不清楚继续SAT超过6个月到1年是否有益。
与脊柱植入物感染相比,在其他亚型骨髓炎中使用抑制性抗生素的文献更为有限。2015年发表的一项回顾性队列研究调查了SAT在足部或长骨骨髓炎患者中的使用情况。该研究报告称,60%的患者通过长期抗生素成功抑制了感染。研究中SAT持续时间为30至466天不等。该研究中的大多数感染都是多种微生物感染,大多数患者接受了多西环素治疗。
根据这些文献,我们提出以下建议:有以下情况的患者可以考虑停止SAT:在进行了清创和保留植入物的治疗后,如果治疗持续了6个月到1年,可以考虑停止抑制性抗生素治疗(SAT)。与其他适应症一样,在停止SAT后的最初几个月内应对患者进行密切随访。

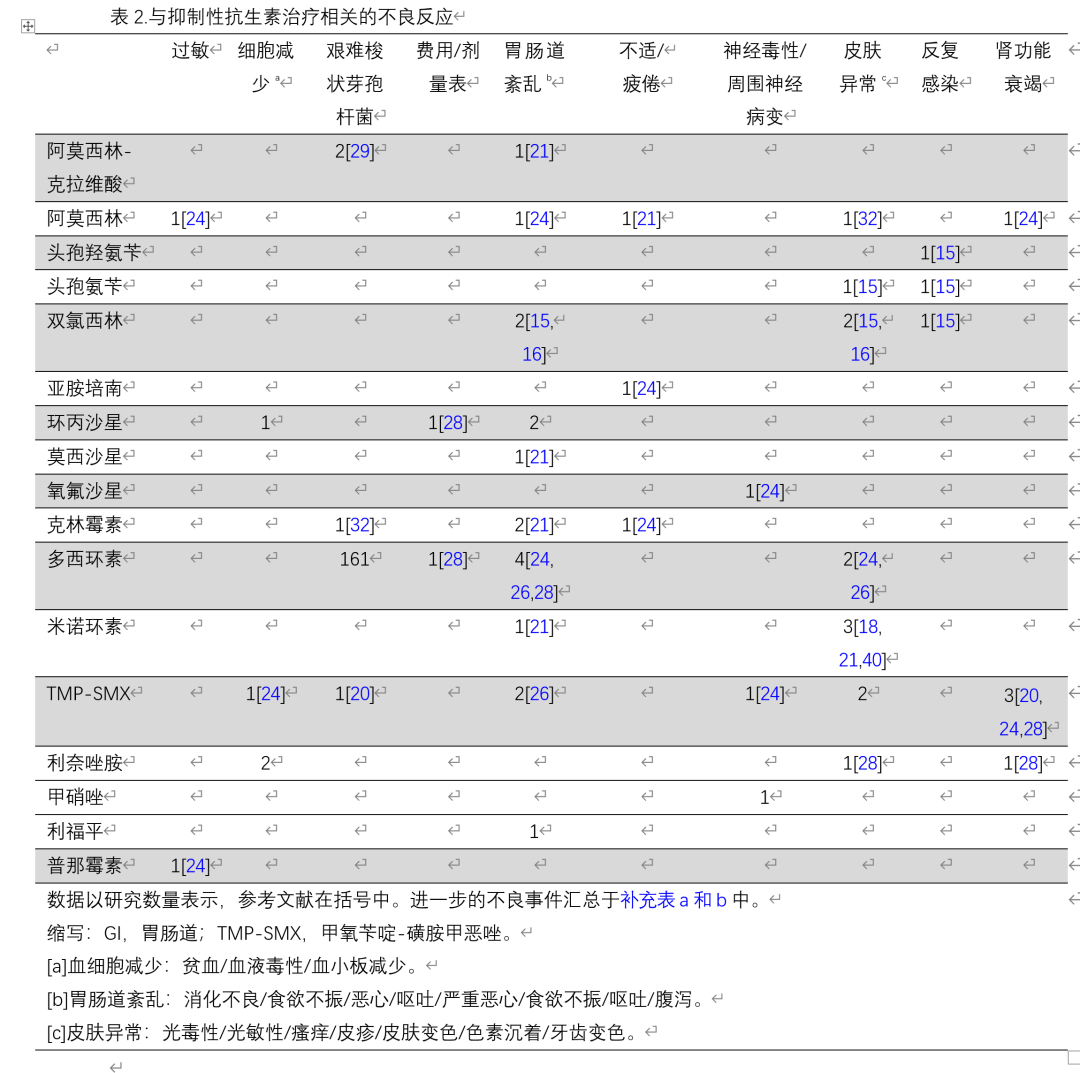
抑制性抗生素治疗相关的不良反应
横断面队列研究通常发现SAT患者队列中的不良反应发生率较高。最近两项针对不同适应症的SAT研究发现,不良反应发生率分别为41%和52%。最常见的不良反应是胃肠道功能紊乱和无症状菌尿。回顾性研究中的不良反应发生并不总是得到细节,有时只是罗列出致病药物和不良反应,却没有阐明导致特定不良反应的是什么药物。了解抗生素及其相关的不良反应,这对于临床医生和接受SAT的患者来说是有益的。
一项横断面队列研究评估了长期抗生素治疗的的患者(其中大多数正在接受抑制性治疗)的经历,结果发现,尽管41%的患者经历了不良反应,但72%的参与者表示完全坚持了抗生素治疗。这表明,尽管有副作用,但对严重感染复发的恐惧迫使患者仍继续使用抗生素,或者副作用并不严重。有许多报告称患者由于不良反应而更换或停止SAT治疗方案,但一般都没有描述其对生活质量的影响。
抑制性抗生素治中的抗生素耐药性和微生物
早在1998年,文献中就已指出SAT可能促进抗生素耐药性的发展,这是一个值得关注的问题。在现有文献中,对SAT人群中存在的抗生素耐药性最准确的描述可能来自2022年的一项为期5年的纵向队列研究。这项研究发现,56%的SAT患者存在多重耐药细菌定植,其中30%是在SAT开始后出现的。回顾性研究发现,四种SAT适应症的耐药率在3%至40%之间。多项研究描述了对环丙沙星、甲氧苄啶-磺胺甲恶唑、利福平和四环素的耐药性。
SAT的另一个潜在不利影响是破坏肠道微生物群——寄居在体表和体内的微生物(主要是细菌)的生态系统。短期抗生素对胃肠道微生物群的影响此前已有描述,而长期抑制性抗生素的后果尚未得到广泛研究。2020年的一项研究发现,接受SAT治疗的部分参与者的微生物群多样性低于预期,但未达到统计学意义。尽管这项研究没有证明这一点,但SAT促进个体微生物群中抗生素耐药性发展或丰富的可能性仍然令人担忧。随着对微生物组组成与健康之间关系的研究越来越深入,SAT导致的微生物群紊乱的相关性将随着时间的推移而得到阐明。尽管并不常见,但因SAT而导致艰难梭菌感染的报道已在文献中广泛出现。
提高未来抑制抗生素治疗研究临床适用性的建议
许多SAT评论论文提出的一个共同主题是,当前主要证据的质量难以为临床实践提供建议。未来研究的一些潜在策略包括以下内容:
1. 分层分析,以便对具有不同因素(例如SAT之前接受过手术或药物治疗)的患者分别进行分析。研究严格定义的特定人群(例如特定年龄标准或既往多次进行假体相关手术)的研究通常会发现成功率较低。
2. 尽可能选择未接受SAT治疗的患者作为对照组。这样可以更真实地了解SAT的疗效。我们认识到,非SAT组的患者可能与接受SAT治疗的患者不完全具有可比性——如果他们的合并症与SAT队列一样,那么他们可能也会被开具SAT处方。
3.设计具有更大队列规模的研究,以提高结果的统计效力。更大队列规模的研究通常是多中心的或使用全国可用的数据库来识别患者。
4.包括未接受最低时长SAT的患者,通常是由于感染或其他原因死亡作为一个单独的早期失败组。完全排除这些患者的做法很可能会高估SAT的成功率,因为这种做法构建了一个初始预后更好、更具弹性的队列来进行分析。
由于抑制性抗生素文献中缺乏明确的说明,临床医生和患者可能会谨慎行事并无限期地继续SAT,从而使患者和社会都暴露于这种治疗的已知和潜在风险。
关于抑制性抗生素治疗的一般实践建议
筛选接受抑制性抗生素治疗的患者
有两大类患者可以开始接受SAT治疗。第一类是初始治疗失败的患者。失败的特点是经过手术和静脉注射抗生素治疗后,临床感染或感染性生物标志物持续存在。
第二类是不适合进行手术(静脉注射抗生素)的患者。这些患者通常体质虚弱、合并症严重、预期寿命有限。在这些患者中,要权衡抑制性抗生素疗法的作用与积极手术干预的风险,以便为患者提供更满意的治疗效果。
从延长口服治疗疗程到抑制性治疗方案的转变并不总是很清晰;在我们之前的研究中,我们认为最初处方的口服疗程预期持续时间超过1年,被视为抑制性治疗。
监测接受抑制性抗生素治疗的患者
我们建议在开始治疗后的第一年对接受SAT治疗的患者进行更频繁的监测,一旦患者的临床和生化感染症状恢复正常,则每6个月或每年进行一次监测。有证据表明,患者在治疗早期更有可能失败;因此,在此期间有必要进行更频繁的监测。
抑制抗生素治疗的持续时间
一些学者已经证明,继续进行SAT超过1年并不会继续降低治疗失败的风险。根据我们的经验,如果满足以下标准,可以考虑停止SAT。患者的炎症标志物(例如白细胞计数、ESR和CRP)应稳定在正常参考范围内至少1年,没有感染的临床症状,例如持续疼痛或假体关节部位分泌物。如果存在适当的基线影像,应重新对感染部位进行成像以比较疾病活动性。最后,患者偏好应该是决定停止SAT的首要考虑因素。需要考虑的患者因素包括患者对SAT的耐受程度、患者的预期寿命以及感染复发对该患者的影响有多大。对于体质虚弱、预期寿命有限且感染复发可能致命的患者,无限期地继续进行SAT可能是合理的。
结论
目前,使用的术语范围很广,包括“长期抑制疗法”、“无限期慢性抑制疗法”和“无限期口服抗菌药物抑制”。我们建议使用“抑制性抗生素治疗”作为标准术语,准确而简洁地描述了长期服用抗生素来无限期地抑制细菌感染的实践过程,以便相关数据不会无意中被排除在系统评价之外。随着全球范围内抗菌药物耐药性和人群合并症的增加,被处方SAT的患者数量可能会增加。因此,患者和临床医生都掌握有关治疗策略的准确信息非常重要,以促进以患者为中心的安全护理。

