【Blood】高危套细胞淋巴瘤的识别和治疗
时间:2025-02-20 12:10:35 热度:37.1℃ 作者:网络
高危套细胞淋巴瘤
套细胞淋巴瘤(MCL)是一种罕见的侵袭性B细胞淋巴瘤,具有显著的临床异质性,在确定MCL的分子起源和耐药机制方面取得的显著进展(这些因素对MCL患者的预后影响也很大)改善了对疾病临床多样性的理解。MCL的治疗选择也从化疗免疫治疗(联合或不联合自体干细胞移植,SCT)转变为多种无化疗方案的组合,包括共价BTK抑制剂(BTKi,如伊布替尼、阿可替尼、泽布替尼和奥布替尼)和非共价BTKi(如匹妥布替尼[pirtobrutinib]),以及抗CD20单克隆抗体(如利妥昔单抗、奥妥珠单抗)联合/不联合BCL2抑制剂(如维奈克拉)或来那度胺。
鉴于MCL克隆的动态变化和疾病演变,诊断和复发时识别高危预后因素至关重要。临床因素包括高MCL国际预后指数(MIPI)评分、高Ki-67增殖指数;一线治疗后24个月内早期进展(POD24);复发时>3线既往治疗;以及侵袭性(母细胞或多形性)组织学。分子异常包括cyclin D1失调、SOX11-CD70轴异常、Musashi-2上调、MYC重排、代谢重编程和表观遗传学变化。其他高危MCL因素包括免疫耗竭的微环境和具有克隆适应性的复杂染色体异常及体细胞突变(TP53、NSD2、CCND1、CDKN2A、BIRC3、SP140、KMT2D、NFkBIE、SMARCA4和NOTCH2等基因)。超高危MCL表现为复发时多种高危预后因素共存,可能导致非常短的无进展生存期。随着MCL治疗向细胞治疗发展,CAR-T治疗的耐药性也有报道。
上述发现促使重新审视高危因素的预后影响、当前管理策略、新的双/三特异性T细胞衔接器、联合疗法、新的治疗靶点以及高危MCL患者的下一代临床试验。
《Blood》近日发表MD安德森癌症中心Preetesh Jain和Michael Wang教授的综述,提供了关于识别和管理高危MCL的最新进展,涵盖当前实践和未来方向。现整理主要内容供参考。

识别高危MCL
高危MCL患者可以通过以下因素进行识别:
临床因素
-
高MCL国际预后指数(MIPI)评分:MIPI是一个综合评估MCL患者预后的工具,包括患者的年龄、体能状态、白细胞计数和乳酸脱氢酶(LDH)水平等因素。高MIPI评分通常提示患者的预后较差。
-
高Ki-67增殖指数:Ki-67是一种细胞增殖标志物,其阳性细胞百分比越高,表示肿瘤细胞的增殖活性越强。高Ki-67增殖指数(通常≥50%)与疾病进展和不良预后相关。
-
一线治疗后24个月内早期进展:如果患者在接受一线治疗后的24个月内出现疾病进展,这通常提示疾病具有侵袭性,预后不良。
-
复发时既往治疗线数超过3线:经过多线治疗后复发的患者,往往对治疗的耐受性和反应性较差,预后不佳。
-
侵袭性组织学(母细胞或多形性):具有母细胞或多形性特征的MCL组织学类型通常提示疾病具有更高的侵袭性和更差的预后。
分子学异常
-
Cyclin D1失调:Cyclin D1在MCL细胞中的过表达是MCL的一个标志性特征,其失调可能导致细胞周期失控,促进肿瘤细胞的增殖。
-
SOX11-CD70轴异常:SOX11基因的过表达可通过上调CD70的表达,促进肿瘤细胞的增殖和存活,同时诱导免疫抑制微环境,影响预后。
-
Musashi-2上调:Musashi-2是一种干细胞相关基因,其上调与MCL的侵袭性疾病过程相关,提示疾病进展风险增加。
-
MYC重排:MYC基因的重排可能导致其异常激活,促进细胞的快速增殖和疾病进展,是高危因素之一。
-
代谢重编程:肿瘤细胞的代谢重编程可为其快速增殖提供能量和物质基础,与疾病进展和耐药相关。
-
表观遗传学变化:表观遗传修饰的改变可影响基因表达,促进肿瘤的发生和发展,是高危MCL的潜在因素之一。
其他因素
-
免疫耗竭的微环境:肿瘤微环境中的免疫细胞功能耗竭,如T细胞功能衰竭,可导致肿瘤细胞逃避免疫监视,促进疾病进展。
-
克隆适应性:具有复杂染色体异常和体细胞突变(如TP53、NSD2、CCND1、CDKN2A、BIRC3、SP140、KMT2D、NFkBIE、SMARCA4和NOTCH2等基因突变)的克隆可能具有更强的适应性和生存能力,导致疾病进展和耐药。
超高危MCL定义为同时存在多种高危特征(如母细胞样转化、CNS受累、原发BTKi耐药),其中位无失败生存期(FFS)<12个月。
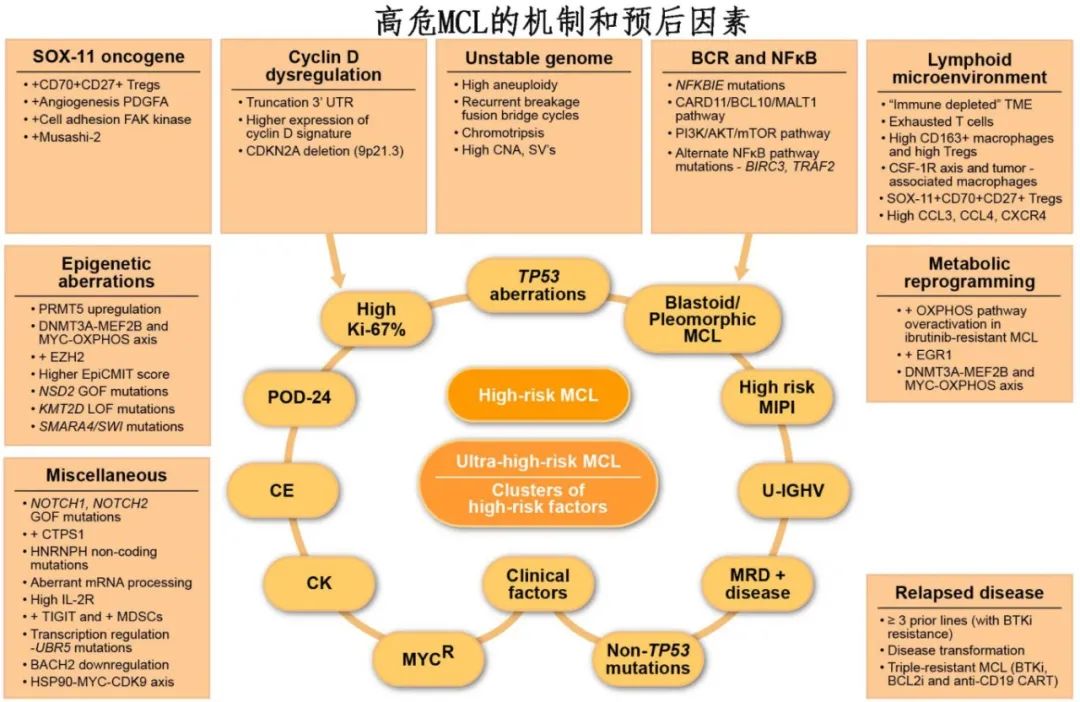
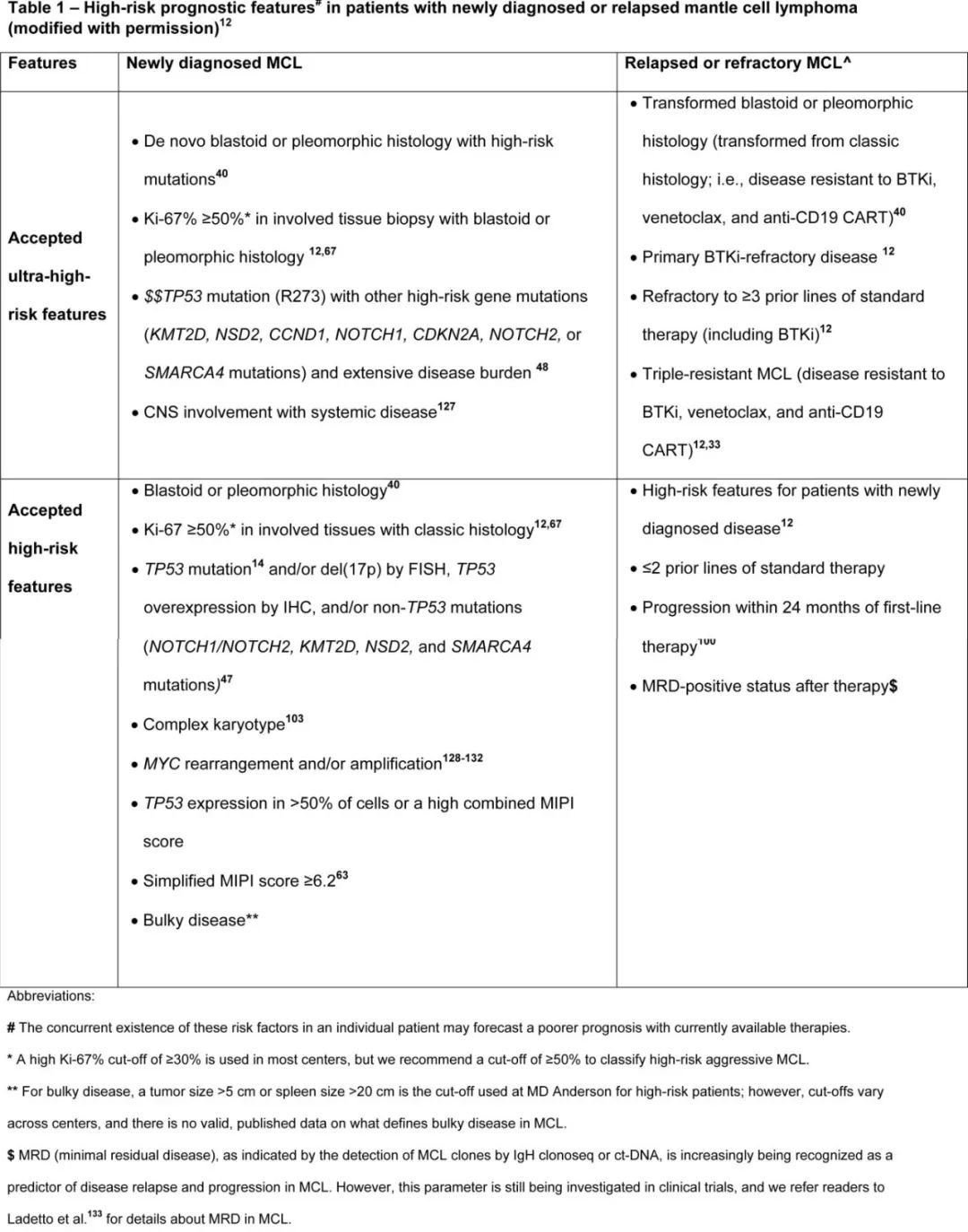
当前治疗对高危因素的影响(不含CAR-T)
一线化学免疫治疗后,高危患者PFS仅1-4年。BTKi虽改善复发患者生存,但多线治疗或高危患者仍易进展并获得性耐药。维奈克拉±抗CD20单抗挽救治疗的ORR为50%,中位生存期约12个月。非共价BTKi匹妥布替尼对共价BTKi耐药患者的ORR为50-60%,高危亚组为40-45%,且安全性更佳。SYMPATICO研究显示,伊布替尼+维奈克拉可延长PFS,且TP53突变与野生型患者获益相似。
特定高危亚组分析
老年/衰弱患者:合并症增加治疗不耐受风险,伊布替尼+利妥昔单抗一线治疗的房颤发生率达34%。
母细胞样/多形性MCL:占MCL的10-30%,Ki-67%常达60-70%,CNS复发率高,一线治疗后中位生存期仅14个月。BTKi(如泽布替尼)在此类患者中PFS与经典型MCL相当。
高Ki-67%+MIPI评分/TP53异常:Ki-67%≥50%患者OS显著缩短(20 vs 118个月)。TP53突变占新诊断MCL的10-40%,与17p缺失、复杂核型、MYC重排相关,中位OS仅1.8年(非突变患者12.7年),TP53突变的类型也可能影响预后。
早期进展(一线治疗后6-24个月内进展):24个月内进展的患者中位OS<12个月,BTKi可改善生存。
共价BTKi耐药:匹妥布替尼可用于BTKi耐药的MCL,ORR为40-50%且安全性良好。匹妥布替尼亦可用于CRA-T失败的患者。
复杂核型:复杂核型(CK)定义为存在≥3个不相关的染色体异常,不含t(11;14)。接受化疗后,有CK的患者中位OS低于没有CK的患者(4.5年 vs 11.6年)。继发性获得CK比原发性CK的患者更差。
高危MCL的治疗
目前克服高危MCL的努力集中在一线治疗的三种方案:BTKi联合化疗免疫治疗(联合或不联合自体SCT),随后BTKi和抗CD20单抗维持;BTKi联合或不联合维奈克拉和抗CD20单抗作为诱导和维持;BTKi联合CAR-T,随后BTKi维持。这些方法可以早期缓解克隆进化,抵消基线高危因素的负面影响。
CAR-T治疗高危MCL
brexucabtagene autoleucel:ZUMA-2研究中,母细胞样、TP53突变、Ki-67%≥50%患者的ORR分别为82%、100%、89%,中位PFS分别为14.5个月、未达到、46.6个月。真实世界研究中,TP53突变、简化MIPI评分较高和POD24患者的CR率较低,母细胞表型和TP53突变患者的PFS较差。BTKi联合CAR-T也在探索中。
Lisocabtagene maraleucel:ORR 83%(CR 73%),在高危患者中,母细胞或多形性组织学、高Ki-67%和TP53突变的ORR分别为70%(CR, 63%)、85%(76%)和89%(58%)。安全性优于brexucabtagene autoleucel。
新型CAR-T:双靶点CD19/CD20 CAR-T(LV20.19)在复发MCL中ORR达100%(CR 76%),1年PFS 77%。匹妥布替尼联合LV20.19 CAR-T以及异基因CD19 CAR-T、CD19 CAR-NK、现货型CAR-T和人源化CD19 CAR-T(Hu19-CD828Z)也在研究中,此外靶向ROR1、CD79b,CD22、CD20和BAFF的CAR-T也在研究中。
CAR-T耐药的挑战
进展后中位生存仅4个月,具有TP53突变和母细胞或多形性组织学的复发性MCL患者可能获得CAR-T耐药。耐药机制包括TIGIT过表达、T细胞耗竭、髓源性抑制细胞增多等。联合TIGIT抑制剂或BTKi或可改善疗效。
其他治疗手段
由于CAR-T的获批,使用异基因SCT治疗高危MCL在某种程度上受到限制。但也有很多回顾性系列报道了异基因SCT在一线巩固或复发的高危TP53突变MCL患者中的结果。建议保留异基因SCT用于适合移植且具有超高危特征和全相合供者的患者巩固治疗。
格菲妥单抗(单药或联合维泊妥珠单抗、维奈克拉、匹妥布替尼、来那度胺)和莫妥珠单抗+维泊妥珠单抗等双特异性抗体方案在高危MCL中也有探索,但尚未获批。
如何治疗高危MCL
新诊断或复发性高危MCL患者的管理算法如下图。首选参加临床试验。局部高危疾病可以放疗,联合或不联合全身治疗。在缺乏临床试验的情况下,建议使用BTKi和CD20单克隆抗体诱导治疗(联合或不联合维奈克拉),然后化疗巩固和/或BTKi和利妥昔单抗维持。在BTKi-R诱导中加入维奈克拉的获益尚未在一项随机一线研究中得到证实。TRIANGLE方案也用于一线治疗。老年患者的低侵袭性治疗可包括阿可替尼+利妥昔单抗或苯达莫司汀+利妥昔单抗。
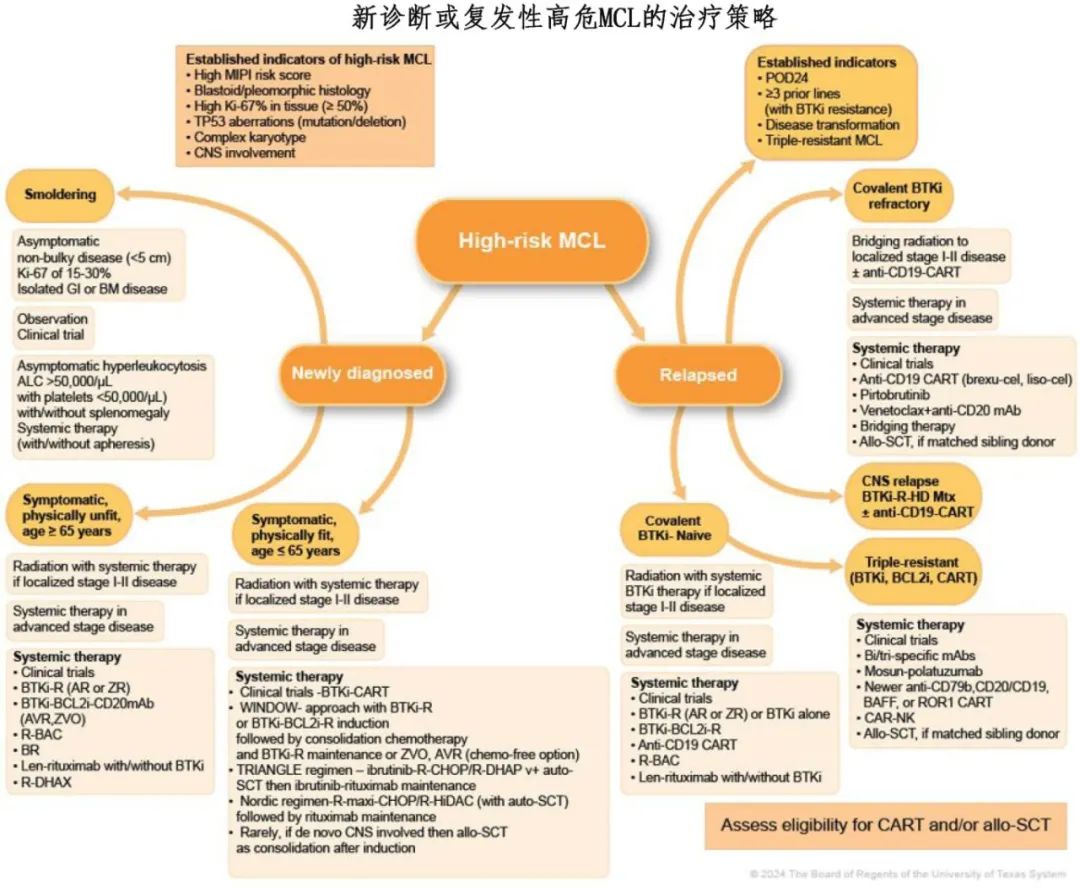
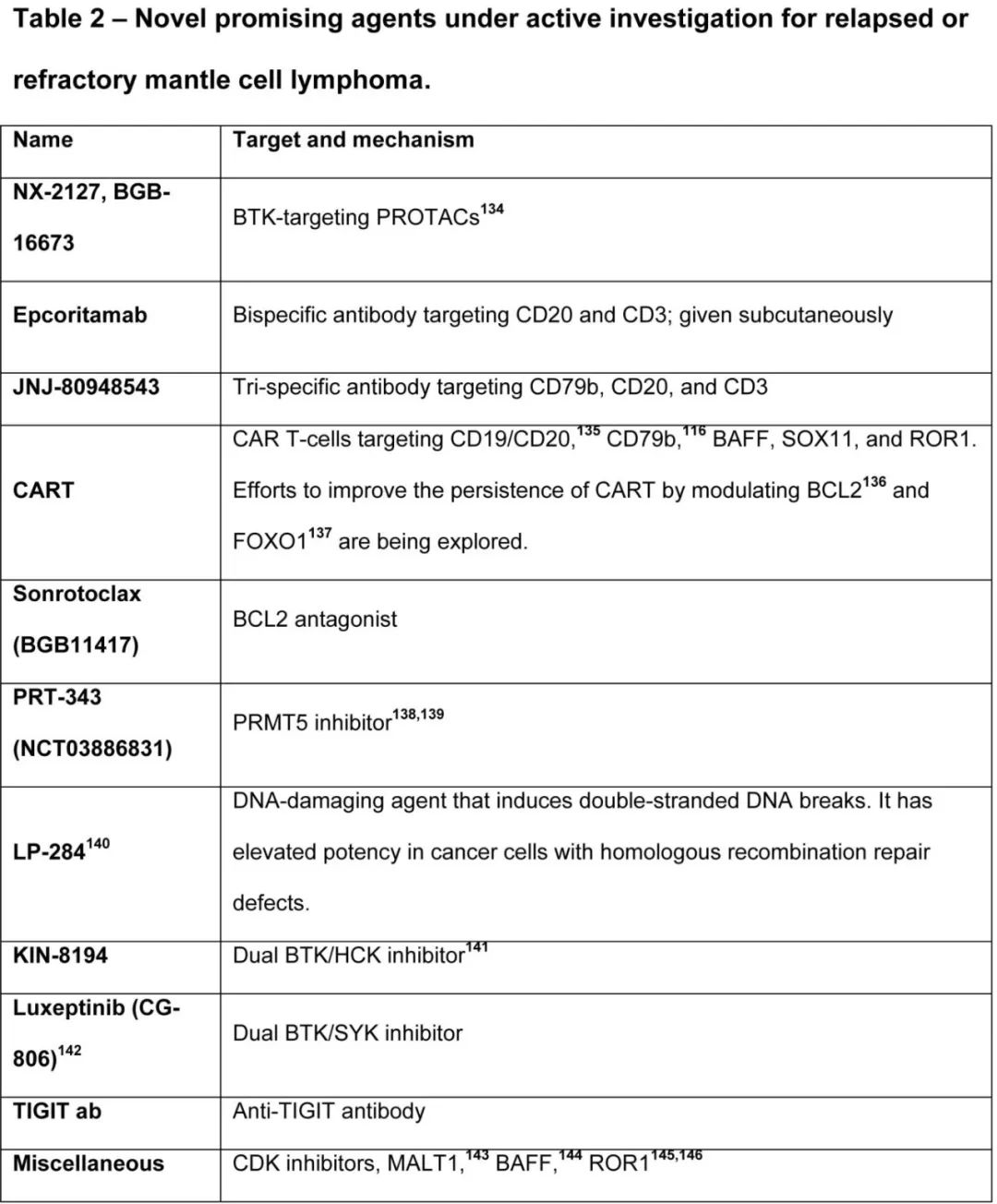
二线BTKi后复发性患者受益于早期转诊CAR-T。在这种情况下,推荐CAR-T(首选)或匹妥布替尼。对于CAR-T的桥接,可以使用放疗、匹妥布替尼或挽救化疗。考虑到与CAR-T相关的毒性和后勤,在确定患者是否有资格接受CAR-T之前,必须评估患者的健康、既往苯达莫司汀暴露和临床状况;仔细的患者选择可以降低并发症和非复发死亡率的风险。对于fit且有全相合供者的患者,可以考虑异基因SCT。对于CNS复发的患者,在CD20单克隆抗体和甲氨蝶呤(全身或鞘内)的基础上添加伊布替尼可以改善预后;泽布替尼表现出CNS穿透性,也可以使用。CAR-T可用于随后的CNS复发。关于MCL患者常规CNS预防的数据尚无定论。
总结
虽然进步明显,但高危MCL的治疗仍存在挑战。招募高危患者参加临床试验仍然至关重要。基于BTKi的诱导和维持是早期缓解的首选,早期使用CAR-T令人鼓舞。自体SCT作为巩固的作用正在减弱,对于BTKi复发性和CAR-T难治性患者的选择较为有限。T细胞衔接器和新型CAR-T的试验带来希望。需要关注的关键领域包括超高危MCL、新出现的耐药机制、化疗vs基于BTKi的诱导以及一线环境中使用CAR-T。可以乐观地认为,在未来3-5年内,持久、长期缓解将成为可能。

参考文献
Preetesh Jain, Michael L Wang; High-Risk MCL: Recognition and Treatment. Blood 2024; blood.2023022354. doi: https://doi.org/10.1182/blood.2023022354


