JIM:索拉非尼联合VAH治疗FLT3-ITD R/R AML的中国2期研究
时间:2023-11-02 11:40:51 热度:37.1℃ 作者:网络
索拉非尼联合VAH
约25%的新诊断急性髓系白血病(AML)患者携带 FMS 相关酪氨酸激酶3-内部串联重复突变 (FLT3-ITDmut)。FLT3ITDmu与 AML 较高的复发率、对挽救治疗的反应降低和较短的总生存期 (OS) 相关;难治性或复发性 AML(R/R AML) 采用传统化疗方法的中位 OS 约为半年,强调了新治疗策略改善结局的重要性。
南方医科大学南方医院刘启发教授团队开展的一项2期研究中,维奈克拉、阿扎胞苷和高三尖杉酯碱 (VAH) 方案96例在R/R AML 患者中的复合完全缓解(CRc)率达到70.8%、客观缓解率(ORR)达到78.1%,且既往接受与未接受过去甲基化药物(HMA)患者的CRc和ORR均没有显著差异。所有患者的中位OS为22.1个月,中位无事件生存率(EFS)为14.3个月,1年OS率为61.5%,1年EFS率为51.0%。在CRc患者中,14例(20.6%)复发,缓解至复发的中位时间为5.4个月,1年累积复发率为19.4%,1年无病生存率(DFS)为69.4%。
初步数据显示,接受索拉非尼+VAH方案治疗的17例 FLT3-ITD 患者的CRc率为76.5%。作为VAH研究的扩展,刘启发教授团队进一步研究了索拉非尼+VAH方案在伴FLT3-ITD 的 R/R AML 患者中的疗效和耐受性,《Journal of Internal Medicine》近日报道了该研究中位随访17.7个月的结局。

研究方法
该研究是一项多中心、单臂、2期研究,有中国12家中心参与,旨在评估索拉非尼联合 VAH 治疗FLT3-ITD 成人R/R AML患者的疗效和安全性,它是一项2期研究(VAH方案作为 R/R AML 挽救治疗的疗效和安全性,NCT04424147)的一部分。纳入18-65岁、ECOG PS为0-2、诊断时为 FLT3-ITD 野生型但复发时发生突变或诊断时即携带 FLT3-ITD 突变(无论复发或难治时是否携带FLT3-ITD 突变)的R/R AML患者。
治疗方案包括连续索拉非尼、14天维奈克拉、7天阿扎胞苷和高三尖杉酯碱,28天为一个周期。如果第28天 BM 为再生障碍则允许延长周期。维奈克拉从第1天的 100 mg 开始,在3天内逐渐增加剂量以达到 400mg 的目标剂量(100、200和400mg);从第4天至第14天,继续每日 400mg 给药。第1-7天皮下注射阿扎胞苷 (75mg/m2) 和高三尖杉酯碱 (1mg/m2)。索拉非尼剂量为400mg,口服每日2次,每疗程第1-14天,维持期间连续服用,直至疾病进展、出现不可接受的毒性、严重并发症、医生决定或患者依从差。
主要终点为2个周期后的CRc。次要终点包括ORR、安全性、CRc持续时间 (DOC)、OS和EFS。
研究结果
患者基线特征
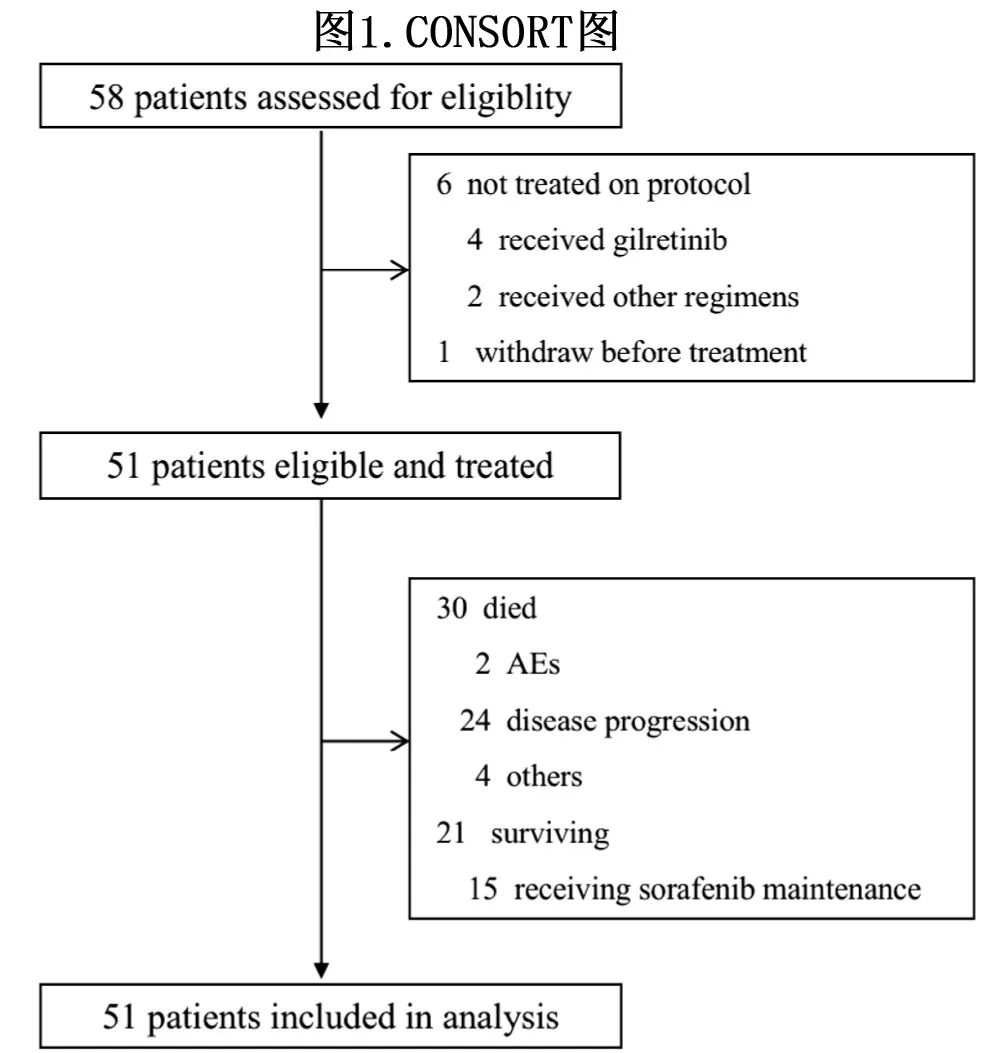
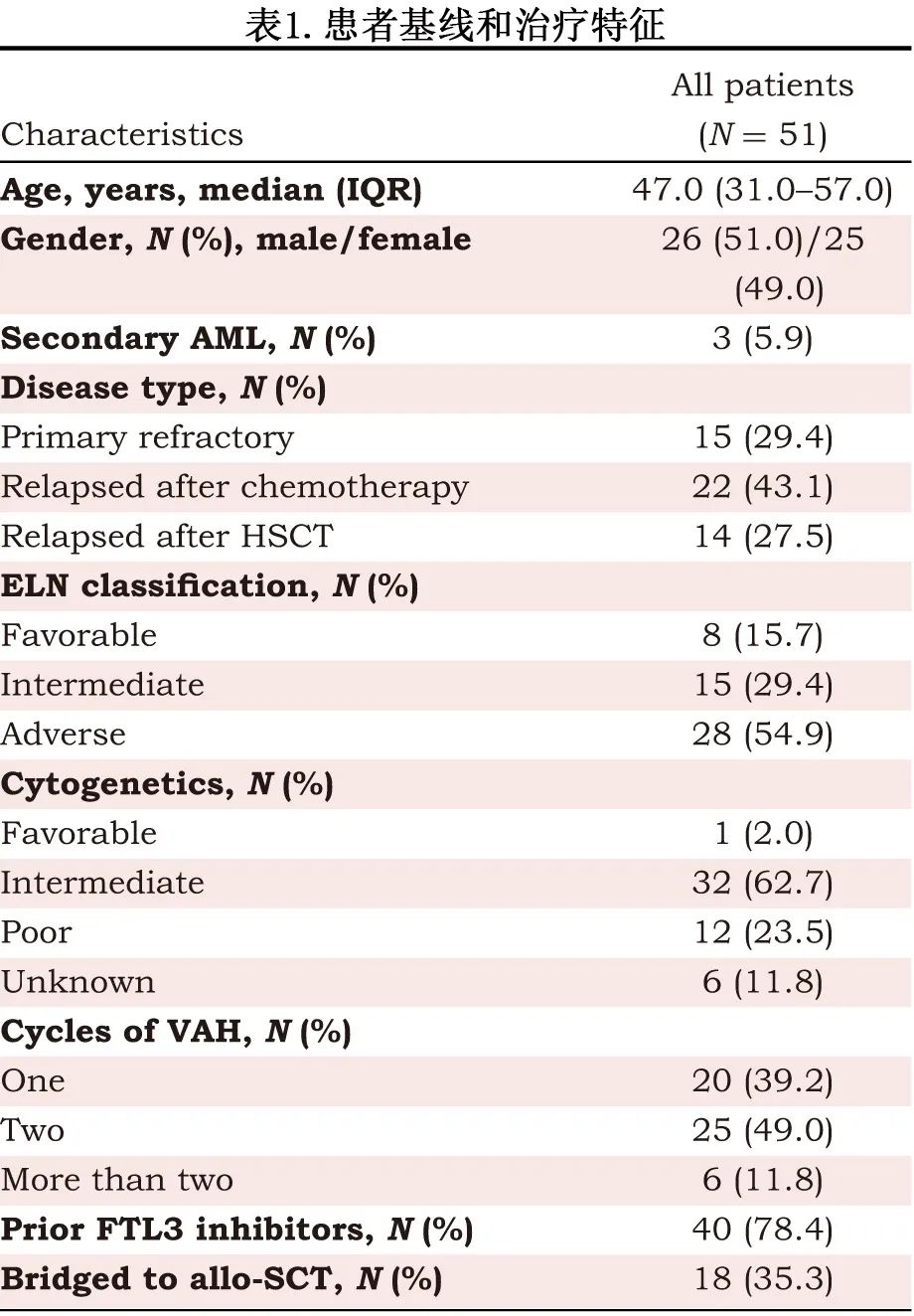
共筛选58例 FLT3-ITD R/R AML 患者,其中51例患者入组 (图1);包括难治性患者15例 (29.4%)和复发性患者36例 (70.6%)(化疗后22例,allo-SCT后14例)。患者包括26例 (51.0%) 男性和25例 (49.0%) 女性,入组时的中位年龄为47岁。在15例难治性 AML 患者中,6例 (40.0%) 在1次诱导治疗后骨髓(BM)原始细胞减少低于50%,9例 (60.0%) 接受≥2个周期的诱导治疗。在化疗后复发的 22例AML 患者中,18例 (81.8%) 为首次复发,4例 (18.2%) 为第二次复发。36例复发性 AML 患者中,31例 (86.1%) 初诊时为FLT3-ITD,17例复发时失去突变,其中8/19例(42.1%)是化疗后复发,9例/12例(75.0%)是allo-SCT 后复发;5例 (13.9%)为复发时检测 FLT3-ITD 突变阳性。40例 (78.4%) 患者既往使用过 FLT3 抑制剂(索拉非尼和吉瑞替尼分别为35和6例)。2例患者携带 FLT3-ITD 和 FLT3-TKD 共突变,包括1例难治性 AML 和1例复发性AML。4例初诊为 FLT3-ITDmut的患者在复发时获得继发性FLT3mut,包括3例 TKD 患者和1例新发 ITD 患者。患者的基线特征见表1。
疗效
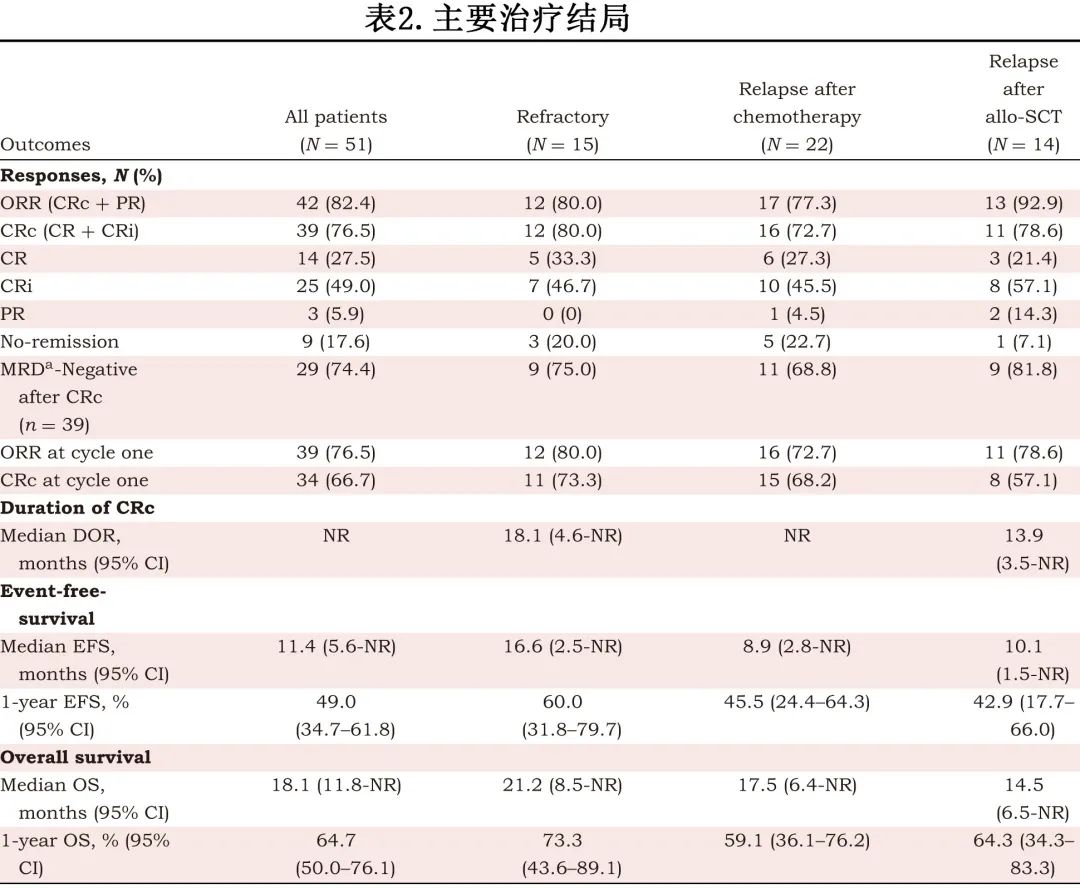
主要结局总结见表2。CRc率为76.5%,MRD-为74.4%(阈值为0.01%),ORR为82.4%(CR,27.5%;CRi,49.0%;PR,5.9%)。亚组分析显示,难治性AML、化疗后复发性 AML 和 allo-SCT 后复发性 AML 患者的 CRc 率分别为80.0%、72.7%和78.6%(p=0.857),对应的 MRD-分别为75.0%、68.8%和81.8%,ORR分别为80.0%、77.3%和92.9%(p=0.745;p=0.470)(表2)。第1周期结束时的 CRc 率和 ORR 分别为66.7%和76.5%,三个亚组之间无显著差异 (CRc p=0.857;ORR p=0.639)(表2)。
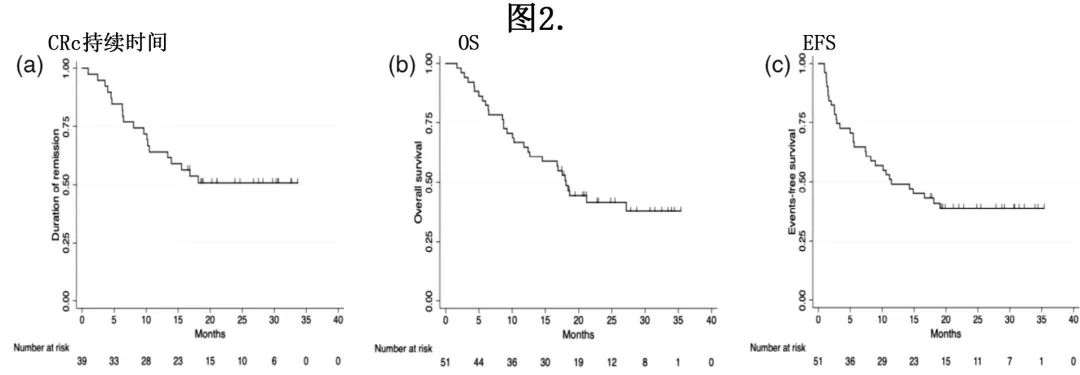
中位随访17.7个月,未达到(NR)中位DOC(图2A),中位 OS 为18.1个月,EFS为11.4个月(图2B、C)。难治性 AML 和化疗或 allo-SCT 后复发性 AML 患者亚组之间的中位DOC、OS和 EFS 相当(DOC的p=0.801,OS的p=0.756,EFS的p=0.899)(表2)。
既往暴露于 FLT3 抑制剂的患者 CRc 率为77.5%,既往未暴露于 FLT3 抑制剂的患者为72.7%(p=0.741),对应的中位 OS 分别为17.5个月和18.6个月 (p=0.588)。在36例复发性 AML 患者中,19例复发时 FLT3-ITDmut患者的 CRc 率为78.9%,17例无 FLT3-ITDmut患者的 CRc 率为70.6%(p=0.563),对应的中位 OS 分别为18.1个月和12.4个月 (p=0.484)。
在39例达到 CRc 的患者中,17例接受了allo-SCT,22例接受了中位3个疗程的巩固化疗。在12例未达到 CRc 的患者中,5例患者接受了其他挽救治疗(4例化疗和1例allo-SCT),7例中止治疗或死亡。allo-SCT 后复发的14例患者中,11例患者接受了中位2个疗程的DLI。在18例接受 allo-SCT 的患者中,16例接受索拉非尼作为移植后维持治疗。达到 CRc 的39例患者与未达到 CRc 的患者相比,接受 allo-SCT 的患者的中位 OS 延长(NR vs. 18.0个月,p=0.044),MRD-患者的 OS 长于MRD+患者(NR vs. 16.9个月,p=0.009)。
遗传特征对缓解和生存期的影响
基因全景图如图3所示。
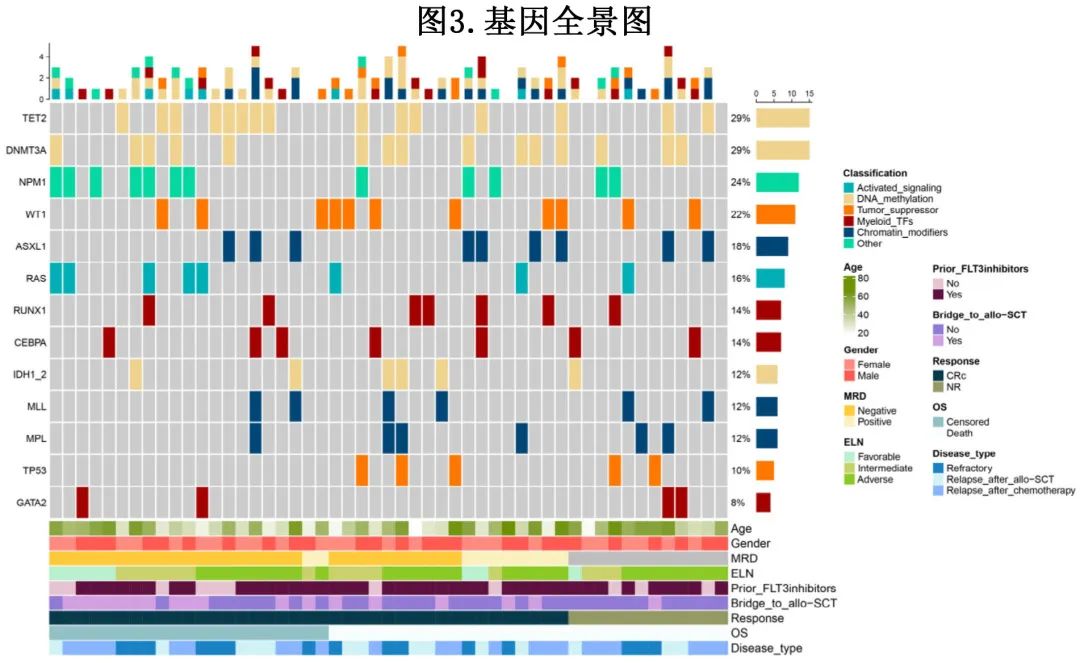
ELN低危、中危和高危组的 CRc 率分别为85.7%、80.0%和71.4%(p=0.594)。在细胞遗传学亚组中,低危、中危和高危组的 CRc 率分别为100%、81.3%和59.3%(p=0.382)。关于分子突变,探索性单变量分析显示,所有基因对 CRc 均无显著影响,而 TP53 突变对 OS 有不良影响 (HR=3.712;p=0.012));5例 TP53 突变患者中3例获得CRc,但末次随访时均复发且死亡。
为评估临床特征和遗传变量的预后影响,作者拟合了随机生存森林。对于CRc,GATA2和 TP53 突变的 VIMP 最高,其次是细胞遗传学(低危vs.其他)、MPL突变、MLL重排和IDH1_2突变,按降序排列。仅P53 突变和allo-SCT 对 OS 有预测价值。
耐受性和毒性
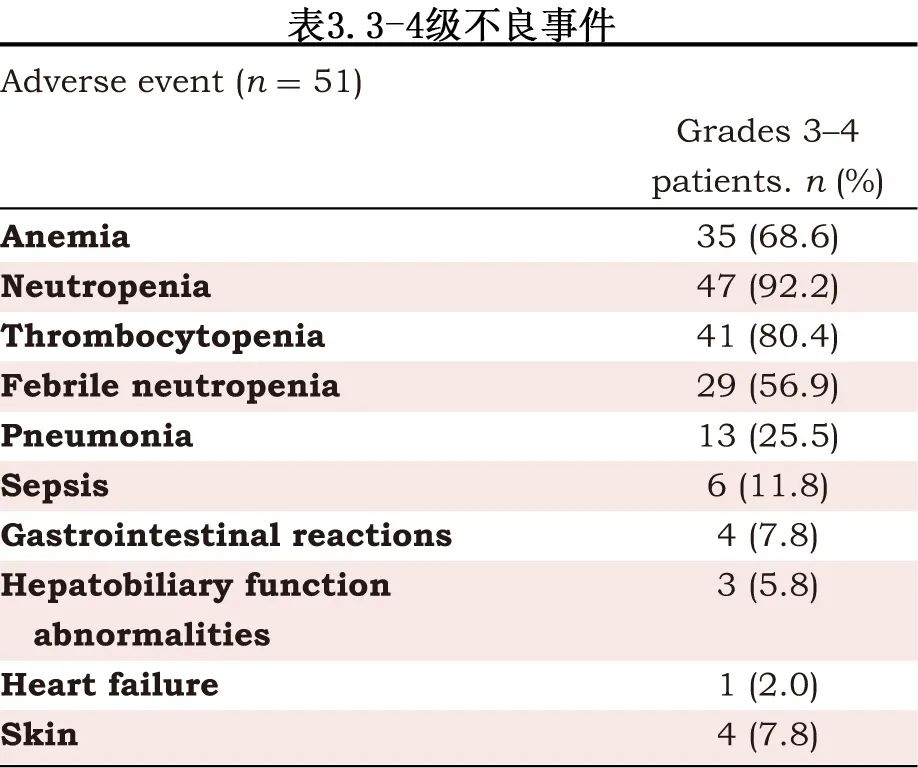
3-4级 AE见表3。≥10%患者发生的3-4级 AE 包括47例 (92.2%) 中性粒细胞减少、41例 (80.4%) 血小板减少、35例 (68.6%) 贫血、29例 (56.9%) 发热性中性粒细胞减少、13例 (25.5%) 肺炎和6例 (11.8%) 脓毒症。在疗程1(n=51) 期间,只有2例 (3.9%) 患者因感染停用维奈克拉和索拉非尼,而所有接受治疗≥7天且在 BM 评估时存活≥28天的患者均纳入疗效分析。在疗程2(n=28) 中,1例 (3.6%) 患者在第4天因心力衰竭中止所有治疗,1例 (3.6%) 患者在第12天因肺炎中止维奈克拉和索拉非尼治疗。治疗相关死亡占3.9%,包括脓毒症 (n=1) 和心力衰竭 (n=1)。
总结
该多中心、单臂、2期研究入组51例R/R FLT3mut AML患者,患者中位年龄为47岁。CRc 为76.5%,ORR为82.4%。中位随访17.7个月,未达到中位 CRc 持续时间,总生存期为18.1个月,无事件生存期为11.4个月。≥10%患者发生的3-4级不良事件包括47例 (92.2%) 中性粒细胞减少、41例 (80.4%) 血小板减少、35例 (68.6%) 贫血、29例 (56.9%) 发热性中性粒细胞减少、13例 (25.5%) 肺炎和6例 (11.8%) 脓毒症。2例 (3.9%) 患者发生治疗相关死亡。
R/R FLT3mut AML的治疗尚无共识。该研究首次报道了索拉非尼联合三药VAH方案治疗FLT3-ITD突变R/R AML,获得高CRc且中位 OS 令人鼓舞;此外治疗相关死亡率低,耐受性好。因此可将其视为FLT3-ITD突变R/R AML患者的一线治疗选择,当然还需要更大规模的人群试验进一步探索。
参考文献
Yu S, Zhang Y, Yu G, Wang Y, Shao R, Du X, et al. Sorafenib plus triplet therapy with venetoclax, azacitidine and homoharringtonine for refractory/ relapsed acute myeloid leukemia with FLT3ITD: A multicenter phase 2 study. J Intern Med.2023;00:1–13.


